专家论证降压药物是否增加癌症风险
目前,虽有研究报道提示降压药物可致癌症风险,但临床医生与患者尚不可盲目、草率停服降压药物,因为降压药物防止心血管病的获益已被广泛证实。由此,降压药物治疗的价值毋庸置疑,对于潜在不良事件风险,医生应在处方降压药物时给予相应重视。
争议焦点 降压药物是否增加癌症风险
自报道萝芙木衍生物致50 岁以上女性患乳腺癌风险增加以来,降压药物是否导致癌症风险增加一直饱受争议。
大量的前瞻性干预试验和病例对照研究都致力于探讨两者的相关性。但是所得结果是降压药物治疗与癌症风险增加并无确切的相关性。该结论可能与研究随访时间较短或高血压本身即是癌症危险因素所致混杂效应有关。
研究初证 降压药物与癌症风险呈一定关联
近年,相 继 发表 在《 柳叶 刀· 肿瘤学》杂志的两项M e t a 分析一致表明, 降 压药物与癌症风险增加有一定相关性。
证据 1
美国 Bangalore 等通过 Pubmed、Embase 和 Cochrane 临床对照试验资料库,检索对降压药物治疗至少随访1
年的随机对照试验,纳入 70 项随机对照试验(148 个对照组)、共计 324168
例受试者,应用的降压药物包括血管紧张素受体拮抗剂(ARB)、血管紧张素转换酶抑制剂(ACEI)、β
受体阻滞剂、钙拮抗剂(CCB)和利尿剂。采用直接比较荟萃、多重比较荟萃和试验序贯评价常用降压药物与癌症风险的相关性。结果表明,ARB 与ACEI
联合治疗可显著增加患者的癌症风险。
证据 2
2010 年发表于《柳叶刀》杂志的一项美国研究对数项相关随机对照临床试验行 Meta 分析,旨在评价 ARB类降压药物使用与癌症发生率的关系。
结果提示,与对照组相比,ARB治疗组的癌症风险增加明显(6.0% 与7.2%)。对实体器官癌症患者进一步实施分层分析表明,相比对照组,ARB 治疗组仅肺癌发生率稍高(0.7%与 0.9% )。
分析
ARB是一类广泛应用的降压药物。第一代 ARB 洛沙坦于 1995 年用于临床,随后缬沙坦、厄贝沙坦、奥美沙坦和坎地沙坦等广泛应用于临床。ARB可通过阻断血管紧张素 1 型(AT1)受体激活从而降低血压。
体外实验表明,肾素 - 血管紧张素系统可调节细胞的增殖、肿瘤的生长以及血管生成和转移。现有证据显示,ARB 可选择性阻断 AT1
受体,同时反馈性间接激活 AT2 受体使 AT2 受体水平升高,而这将刺激可导致体内肿瘤的血管生成增加。但是,这一体外实验观察结果与 ARB
引起人类癌症风险的确切相关性,以及 ARB 导致癌症风险增加的机制至今仍不得而知。
循证进展 钙拮抗剂或可增加绝经女性乳腺癌风险
CCB是一类重要的临床降压药物,我国高达半数以上高血压患者应用CCB治疗。但是,长期使用 CCB的安全性、耐受性问题越来越受到关注与质疑。
证据 1
今年8月5日在线发表于《美国医学会杂志·内科学》杂志的一项病例对照研究表明,长期服用 CCB 类降压药物可导致绝经女性的乳腺癌风险增加。
该研究是第一个观察长期使用CCB 降压治疗与乳腺癌风险的研究。研究纳入自西雅图-普吉特海湾地区、55——74 岁的绝经女性 2763 例,其中 880例患有乳腺浸润性导管癌,1027 例患有乳腺浸润性小叶癌,856 例无癌症受试者作为对照。
结果表明,持续服用 CCB 降压治疗长达 10 年以上患者的乳腺浸润性导管癌、乳腺浸润性小叶癌风险显著增加(OR 分别为 2.4 和 2.6)。与之相比,服用利尿剂、β 受体阻滞剂以及 ARB降压药物治疗与癌症风险增加并无相关性。
证据 2
1996 年,发表于《柳叶刀》杂志的一项美国研究表明,服用降压药物治疗可使老年人癌症风险增加 72%.
今年,由 Saltzman 等报道的一项降压药物与乳腺癌风险关联的前瞻性队列研究,纳入 3201 例年龄大于
65岁的女性,均使用降压药物治疗并连续随访 2 年以上。结果显示,相比于未使用降压药物治疗女性,在过去 2年间服用 CCB
类药物女性罹患乳腺癌风险增加 1.6 倍;近期服用速释型CCB 降压治疗女性罹患乳腺癌风险增加 2.4 倍。(Cancer Causes
& Control.2013,24:365)
分析
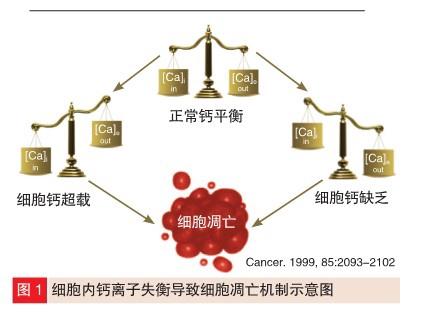
CCB 主要通过阻断钙离子经过细胞膜钙离子通道进入细胞,使细胞内钙离子水平降低而引起心血管等组织、器官功能改变,达到降压作用。
钙通道阻断可以抑制细胞凋亡(图 1),而细胞凋亡是限制肿瘤细胞生长的有效机制。因此使用
CCB降压治疗可能使恶性肿瘤细胞的存活期延长、肿瘤细胞数目增多、肿瘤体积增大,故存在癌症风险。但是,有关 CCB
与乳腺癌风险关系及相关生物学机制还需进一步确证。
如果长期使用 CCB 确实能引发乳腺癌风险增加,可能导致现有长期CCB 降压策略变革,也可能为临床乳腺癌防止提供新的干预靶点。
剂型选择 选缓释舍速释 CCB ?
Saltzman 等发表在《癌症病因与控制 》杂志的研究提示速释型 CCB 治疗患者将蒙受更高的乳腺癌风险。长期随访还发现,速释型 CCB 使用率大幅降低,从 44% 减至 10%,而缓释型CCB 制剂的临床使用率不断增加且渐被普遍认可。
针对循证研究结论的出入,或可如此理解:部分早期研究入选患者速释型 CCB 使用率偏高,结果显示 CCB
治疗与乳腺癌风险有相关性,且呈强关联;一些近期研究对象应用缓释型 CCB 的比例更高,分析表明 CCB 治疗与乳腺癌风险的相关性较弱。以上或是
CCB 类药物与乳腺癌风险的各项研究结果不相一致的个中原因之一。这也许能让高血压女性更有信心地选择缓释型 CCB
作为降压药物治疗组合之一,而不必过分顾虑乳腺癌风险。CCB,尤其是缓释型CCB 可能引起乳腺癌的生物学机制尚不清楚。有人推测,CCB
可能通过细胞间钙离子水平升高而抑制细胞凋亡,但未获得相关研究文献支持。事实上,地尔硫卓、氨氯地平和维拉帕米等CCB
类药物因有抗增殖效应而常与传统化疗药物用于治疗耐药的乳腺癌患者。
但是,CCB 具有广泛的生理作用,尚有众多至今仍未阐明的效应,可能因某一种或多种未知效应最终导致乳腺癌风险。与缓释型 CCB
相比,速释型 CCB 的血药浓度波动幅度更大。因此,速释 型 CCB 治 疗 的 血 药
浓度可能逾越了肿瘤生长所需达到的阈值浓度,进而导致服用者临床乳腺癌风险增加。
临床治疗 理性评估风险 切莫轻易停药
最新统计数据显示,我国高血压患者逾 3.3 亿,CCB 和 ARB 是临床最广泛使用的降压药物,二者的市场份额占有率最高。
尽管一些临床研究结果表明,降压药物可导致癌症风险增加,但是迄今关于降压药物相关癌症风险尚无法盖棺定论。主要因为现有多项研究还存在缺陷与不足,如有些研究得出的关联性结果基于小样本且原因解析欠完整,加之相关生物学机制亦不明确。因此可以预见,未来亟需更多学者致力于降压药物与癌症风险的机制与临床研究,这对于医生安全、合理用药与公众健康都有深远意义。
目前,尚不能确证临床常用降压药物可以增加癌症风险,亟需更多学者、医生致力于相关领域的基础和临床研究。此前,临床医生切不可盲目停用降压药物治疗。
-
科技前沿









