离子迁移谱技术检测食品中甲基丙烯酸甲酯的迁移量
聚甲基丙烯酸甲酯(PMMA)作为一种典型的食品接触材料, 具有透光率高、 性能优良及价格适宜等优点, 被广泛用于制作餐具、 外包装盒等食品接触制品. 当此类制品与食品接触时, 其残留的甲基丙烯酸甲酯单体可能迁移释放到食品中. 甲基丙烯酸甲酯有一定的毒性, 可引起轻度皮炎和结膜炎, 并对人的神经系统有损害作用, 严重者可能引起中毒性脑病. 因此, 欧盟规定甲基丙烯酸甲酯的特定迁移量须低于6 mg/kg; 日本厚生省卫生告示第370号规定其迁移量要小于15 mg/L.
目前, 对丙烯酸及其酯类聚合物中丙烯酸酯类单体的测定大多采用气相色谱法或气相色谱-质谱法, 但这2种方法操作繁琐且耗时长, 不适合现场快速检测的需求. 而且由于气相色谱柱的限制, 导致水基食品模拟物无法直接进样, 通常采用有机溶剂萃取后进样、 固相萃取、 顶空或吹扫捕集等方式. 有机溶剂萃取后进样灵敏度不高, 固相萃取操作繁琐耗时长, 顶空或吹扫仪器则成本较高.
相对于传统的分析技术, 离子迁移谱(IMS)技术具有分析速度快、 灵敏度高、 无溶剂和气体等消耗的优点. 高场非对称离子迁移谱(FAIMS)技术是在传统的IMS技术基础上发展起来的, 其最大特征是通过各种高低电场作用形成一个离子过滤器, 可将干扰气体分子与待检测的目标分子高效率地分离, 提高了检测的选择性, 同时也可显著提高检测的信噪比, 从而提高检测的灵敏度. FAIMS 技术不仅可应用于传统的爆炸物、 毒品和危险品等分析领域, 近年来也被应用于生物医药、 环境、 食品及化妆品检测等新兴领域. 此外, FAIMS还可以与质谱、 液相色谱-质谱以及气相色谱等技术联用来进一步拓展其应用范围. FAIMS 可以连接在质谱(MS)检测器的前端, 为MS检测提供几乎专一的待检测离子, 从而提高检测的选择性和灵敏度; 也可以单独使用FAIMS 技术来开发便携式、 小型化的高性能气体及生物分子的检测器. 迄今, FAIMS技术在食品接触材料污染物分析领域中的应用尚未见报道.
本文采用FAIMS技术识别水基食品模拟物中甲基丙烯酸甲酯的特征离子信号, 并通过对实验参数的优化, 建立了快速检测甲基丙烯酸甲酯迁移量的定量分析方法.
1 实验部分
1.1 仪器与试剂
英国OWLSTONE公司Lonestar型便携式气体分析仪(高场不对称离子迁移谱仪); 美国Milli-Q公司Integral 10型纯水制备系统; 德国Sartorius公司R200D型电子天平; 上海安谱公司ANPEL LGA-5000W空气发生器.
甲基丙烯酸甲酯(MMA, 纯度≥ 97%)购自德国Dr. Ehrenstorfer GmbH公司; 实验用水为超纯水; 乙醇为色谱纯; 其它试剂均为分析纯. MMA标准储备液(1000 mg/L)的配制: 准确称取0.1 g MMA(精确到0.0002 g)置于100 mL容量瓶中, 用水稀释至刻度, 充分摇匀. MMA标准工作溶液的配制: 移取适量MMA标准储备液, 用水稀释成适用浓度的标准工作溶液.
1.2 离子迁移谱参数
样品室温度40 ℃; 样品盖温度70 ℃; 样品过滤器温度110 ℃; 载气为零级空气; 样品载气(MFC1)流速0.15 L/min, 分流载气(MFC 2)流速0.13 L/min, 补偿气(MFC 3)流速1.6 L/min. 甲基丙烯酸甲酯(MMA)的检测流程如Scheme 1所示. 空气发生器产生的载气经净化后, 通过流量控制器(Split flow box)控制流速及进样量, 其中MFC 1为样品载气, MFC 2用于控制分流出的样品气的量, MFC 3为补偿气. 样品通过顶空方式进样, 在载气推动下进入FAIMS芯片进行检测. 取样体积4 mL; 加入磁搅拌子搅拌.
Scheme 1
 | Scheme 1 Schematic diagram of the experiment procedure |
1.3 食品接触材料迁移实验
根据欧盟塑料食品接触材料法规(EU)No.10/2011要求, 将样品在80 ℃下用食品模拟物浸泡8 h. 食品模拟物包括水、 20%(体积分数)乙醇、 50%乙醇和95%乙醇.
2 结果与讨论
2.1 MMA的FAIMS谱定性识别
采用热解析法进样, 在样品加热温度为40 ℃, 流速1.6 L/min条件下, 对10 mg/L MMA标准水溶液在不同场强下进行补偿电压值和离子电流强度值的连续扫描, 得到其FAIMS谱图(图1), 信号区域颜色深度代表相应的离子流强度. 结果表明, MMA只在正离子模式下有响应.
在FAIMS体系中, 正离子的形成过程如下:

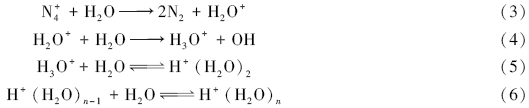
正的水基离子团(水合氢离子, 蓝色)非常稳定, 构成了活性离子峰. 当分析物(M)进入活性离子峰后, 可以取代其中的1个或2个水分子(取决于分析物种类)形成单体离子[MH+(H2O)2]或二聚离子[M2H+(H2O)1], 同时也降低了活性离子峰内的离子浓度.

因此, 对于MMA的FAIMS谱(图1)中出现的3组特征峰, 可判断左边的是活性离子峰, 中间的是待测物离子峰, 右边的为待测物二聚体离子峰.
Fig.1
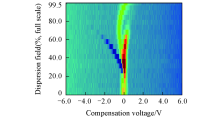 | Fig.1 FAIMS spectrum of 10 mg/L MMA in aqueous solution(positive ion mode) |
在分散场强分别为65%和85%时, MMA的离子流强度(IC)随补偿电压(CV)的二维变化如图2所示. 可见, 65%场强下其单体及二聚体离子峰强度最高处的CV值分别为-0.46和0.21 V, 而85%场下其单体离子峰的CV值为-0.35 V. 在高分散场强(> 80%)区域, 二聚体离子峰消失, 仅存在待测物离子峰. 从定性鉴别的角度, 选择分散场强为65%可得到较多的特征峰, 利于识别. 从定量测定的角度, 选择分散场强为85%可达到较好的选择性.
Fig.2
 | Fig.2 Variation of ion current intensity(IC) of MMA with compensation voltage(CV) in positive ion mode under dispersion field strengths of 65%(A) and 85%(B) |
2.2 扫描次数的选择
实验采用的进样方式类似于顶空, 但又有差异. 用样品载气以固定的流速连续吹扫样品, 进样是一个动态的过程, 每一次吹扫的浓度都可能不同, 因此会造成重现性较差. 以100 μ g/L MMA水溶液为研究对象, 扫描11次, 以85%分散场强下的单体离子峰强度对扫描次数作图(图3).
Fig.3
 | Fig.3 Influence of scanning times on the determination of MMA |
结果表明, 扫描次数由1次增至4次时, 响应值逐渐升高, 扫描4~7次时响应值较稳定, 扫描8次以后响应值开始下降. MMA的沸点为101 ℃, 初始加热温度为40 ℃, 需要扫描4次使其蒸气浓度达到动态平衡, 随着吹扫的继续进行, 溶液中目标物浓度降低, 因而响应值随之降低. 综合考虑实验稳定性和分析时间的要求, 选择扫描5次的数据用于定量计算.
2.3 样品加热温度的选择
以200 μ g/L MMA水溶液为研究对象, 分别在40, 50和60 ℃ 的加热温度下测试了样品离子流强度随温度的变化, 结果如图4所示. 结果表明, 温度由40 ℃升高至50 ℃时, MMA单体离子峰强度降低约10%, 二聚体离子峰强度下降约30%; 当温度升至60 ℃ 时, 单体离子峰强度急剧降低约70%, 而二聚体离子峰则基本保持原来的降幅. 本实验体系中存在MMA和水2种物质, 沸点分别为101和100 ℃, 十分相近. 随着温度的升高, 2种物质的蒸气浓度均提高, 但水蒸汽增加比例更高, 从而导致MMA的浓度比例反而下降, 使形成的二聚体离子峰强度降低. 进一步升高温度, 水蒸气浓度进一步升高, 而待测物浓度比例进一步降低, 导致其单体离子峰和二聚体离子峰同时降低. 因此, 选择样品加热温度为40 ℃ .
Fig.4
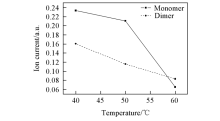 | Fig.4 Variation of ion current intensity(IC) of MMA with sample temperature under 65% dispersion field strength |
Fig.5
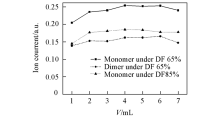 | Fig.5 Influence of different sampling volumes on the monomer ion intensity of MMA |
2.4 取样体积的选择
以200 μ g/L MMA水溶液为研究对象, 考察了取样体积在1~6 mL范围内变化时对其离子流强度的影响. 结果(图5)表明, 取样体积由1 mL增至2 mL时, MMA单体离子峰及二聚体离子峰强度均明显增加; 随着取样体积由2 mL逐渐增加时, 离子强度缓慢增加; 当取样体积达到4 mL, 离子强度达到平衡, 并随着体积增大略有下降. 因此, 选择取样体积为4 mL.
2.5 载气流速的选择
以200 μ g/L MMA水溶液为研究对象, 考察了载气流速(MFC 3)在1.5~2.0 L/min范围内变化时其离子流强度(85%分散场强下)随补偿电压及载气的变化, 结果如图6和图7所示. 可见, 当载气流速由1.5 L/min增加至1.6 L/min时, MMA单体离子峰强度明显增加, 同时在85%分散场强下观察不到二聚体离子峰. 随着载气流速增至1.8 L/min, 在85%分散场强下可观察到二聚体离子峰; 同时单体离子峰的CV值左移, 伴随峰形变宽并出现肩峰; 当载气流速继续增加至1.9 L/min时, 二聚体离子峰的强度明显加强, 同时单体离子峰离子强度略有增加, CV值继续左移, 峰形变宽加剧; 当载气流速继续增至2 L/min时, 二聚体离子峰进一步加强, 同时单体离子峰的峰形进一步变宽, 峰高反而有所降低.
Fig.6
 | Fig.6 IC-CV diagrams of MMA at different flow rate of
carrier gas under 85% dispersed field strength Flow rate/(L· min-1): a. 1.5; b. 1.6; c. 1.7; d. 1.8; e. 1.9; f. 2.0. |
Fig.7
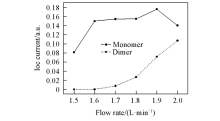 | Fig.7 Variation of ion current intensity(IC) of MMA with carrier gas flow rate under 65% dispersion field strength |
通常, FAIMS系统需要干燥洁净的空气流有2个原因: 一是离子团需要被气流载入离子通道并到达检测极板; 二是需要通过空气来引入样品的离化过程. 穿透因子(到达检测极板的离子比例)随着流量的增加而增加, 穿透因子越高灵敏度就越大. 但是高流量同样意味着更大的离子电流峰的半高宽, 而这降低了 FAIMS 的分辨率. 这很好地解释了上述实验现象. 考虑到既要追求灵敏度, 又要保证足够的分辨率, 故选择载气流速为1.6 L/min.
2.6 乙醇掺杂的影响
考虑到MMA的溶解规律, 并参考欧盟塑料食品接触材料法规EU No.10/2011的相关规定, MMA溶出风险较高的食品模拟物除水外, 还包括体积分数分别为20%, 50%及95%的乙醇. 以1 mg/L MMA溶液为研究对象, 考察了掺杂乙醇对其离子流强度及峰形(65%分散场强下)的影响, 结果见图8. 结果表明, 掺杂20%乙醇时, MMA的单体及二聚体离子峰均完全消失, 取而代之的是乙醇的离子峰; 掺杂50%乙醇及95%乙醇的现象与20%乙醇一致, 即均观察不到MMA的离子峰.
在以Ni63为离子源的FAIMS系统中, 化学灵敏度与物质的质子/电子亲和能呈正相关. 醇类的质子亲和能通常略低于酯类, 但本实验所研究的样品中存在20%乙醇, 而目标物MMA仅有1 mg/L, 巨大的浓度差使乙醇的离化占主导, 从而完全抑制了MMA的电离. 因此, 目前的实验条件并不适于含醇的食品模拟物的检测.
Fig.8
 | Fig.8 Effect of ethanol doping on IC-CV diagram of MMA
under 65% dispersed field strength a. 20% Ethanol; b. 1 mg/L MMA in 20% ethanol; c. 1 mg/L MMA in water. |
Fig.9
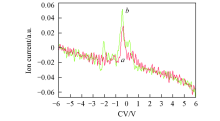 | Fig.9 IC-CV diagrams of 10 μ g/L MMA in aqueous solution at
different dispersed field strength a. DF85%; b. DF65%. |
2.7 检出限的确定
在选定的最佳实验条件下, 测试了不同浓度MMA水溶液在不同分散场下的离子强度变化. 结果表明, 在85%的分散场强下, 10 μ g/L的MMA水溶液的信噪比S/N=3(图9). 虽然样品在65%的分散场强下响应值更高, 但峰拓宽且裂分, 分辨率较低. 因此, MMA水溶液的检出限为10 μ g/L.
2.8 MMA浓度与其离子强度的相关性
对不同浓度的MMA标准溶液进行检测, 获得了一系列FAIMS谱图. 图10示出了分散场强85%、 补偿电压-0.35 V处单体离子强度峰值对其浓度的作图. 结果表明, MMA单体离子峰强度随其浓度增大而增强, 在低浓度(0.01~0.05 mg/L)范围内呈线性关系. 当浓度超过0.1 mg/L时, 单体离子峰强度增速减缓, 浓度达到5 mg/L后, 强度不再增大. 这与样品分子的离化率有关, 较低浓度时, 样品分子离化率不变, 当超过一定浓度时, 离化率随着浓度的增加而降低. 这与陶羽宇等[16]采用FAIMS技术检测二乙醇胺时发现的规律一致.
Fig.10
 | Fig.10 Variation of ion intensity of MMA with concentration in range of 0-10 mg/L(A) and 0.01-0.05 mg/L(B) |
Fig.11
 | Fig.11 Variation of ion intensity of MMA with concentration of 0-10 mg/L under 65%dispersion field strength and CV of 0.21 V |
选择分散场强为65%, 提取MMA的IC-CV图(图2), 可观察到在补偿电压为0.21 V处出现了MMA的二聚体离子峰. 以二聚体离子强度对其浓度作图, 得图11. 结果表明, MMA二聚体离子峰强度随浓度的变化规律与单体离子类似, 不同的是, 当浓度超过2 mg/L时, 二聚体离子强度的增速显著高于单体离子强度, 并且在浓度超过5 mg/L时, 二聚体离子强度仍有明显增强.
2.9 回收率精密度
选择某品牌聚甲基丙烯酸甲酯塑料水杯, 进行3水平加标回收实验. 结果表明, MMA在水基食品模拟物中的加标回收率为80.3%~92.7%, 相对标准偏差(n=6)在5%以内, 可见方法的准确度和精密度完全满足分析要求.
2.10 实际样品测定
采用FAIMS法对8个聚甲基丙烯酸甲酯水杯的水基食品模拟物迁移量进行了测试, 结果均为未检出. 由于乙醇对测试的干扰, 无法实现对含醇食品模拟液的定量测定.
3 结 论
与GC-MS法检测水基食品模拟物中MMA相比, 所建立的FAIMS检测法具有灵敏度高、 分析速度快、 操作便捷、 仪器及运行成本低、 便携等优点; 但同时具有线性范围较窄, 无法排除部分高浓度基体如乙醇的干扰, 选择性较差而限制其应用等缺点. 为了排除基体干扰, 扩大方法的应用范围, 今后将在仪器接口方面进行改造, 探索FAIMS与其它分离手段联用的可能性.
-
焦点事件













