中国科研成果首登《柳叶刀·血液病学》封面
“这是我国第一篇刊登在《柳叶刀·血液病学》上的封面论文。”据该封面文章的第一作者和通讯作者、国家癌症中心/中国医学科学院肿瘤医院石远凯教授介绍,《柳叶刀》是世界顶级医学期刊,其子刊《血液病学》为月刊,2014年9月创刊,在国际同行中具有广泛影响力。科技界再传好消息:我国科学家的科研论文首次作为封面文章,刊发在2019年第一期《柳叶刀·血液病学》上。

2019年第一期《柳叶刀·血液病学》封面文章,其中的恶龙象征复发或难治经典霍奇金淋巴瘤。
研究专家
该封面文章介绍的是石远凯教授牵头开展的国产PD-1抑制剂信迪利单抗(商品名“达伯舒”)的临床研究ORIENT-1。研究结果显示,信迪利单抗治疗复发难治霍奇金淋巴瘤(cHL)的客观缓解率高达80.4%,安全性良好,有望成为复发难治cHL患者新的治疗选择。
该杂志邀请国际权威淋巴瘤专家美国梅奥诊所(Mayo Clinic)淋巴瘤组主任Stephen M Ansell教授撰写述评,认为:信迪利单抗为肿瘤患者提供了创新且高度有效的治疗模式,提升了患者用药可及性,从而改善治疗结果。

石远凯教授
据石远凯教授介绍,复发难治cHL国际上通用的标准治疗是自体造血干细胞移植(ASCT)和本妥昔单抗(brentuximab vedotin),但由于受到药物不可及或经济条件的限制,中国绝大部分患者无法接受标准治疗。cHL的特征是恶性R-S细胞散布于免疫细胞之间,染色体9p24.1改变导致PD-1的配体PD-L1在R-S细胞中过度表达,这使得PD-1抑制剂在cHL的治疗中前景广阔。
研究概况
石远凯教授介绍说,该研究是一项2期多中心单臂临床试验,共有18家来自中国的医学中心参与,患者入组要求包括年龄≥18岁,接受过≥2线治疗的复发难治经典cHL。静脉给予信迪利单抗 200mg,每3周一次,直至疾病进展、死亡、出现不可接受毒性或撤出研究,主要研究终点是客观缓解率,治疗结果由独立的影像学委员会评价(IRRC)。
据介绍,ORIENT-1是迄今为止中国入组人数最多的复发或难治性cHL的临床试验,一共招募了96位包括放疗与ASCT在内的≥2线治疗失败的中国cHL患者,使用信迪利单抗注射液治疗,剂量200mg/人,每三周一次。临床试验患者的入组时间为自2017年4月19日至2017年11月1日,96例患者中有4例患者的诊断未经病理中心确认,故未纳入分析。
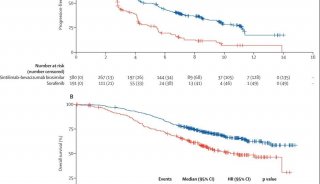
研究结果显示,纳入分析的92例患者中,74例患者(80.4%)获得客观缓解;90例患者疾病控制(97.8%);其中,完全缓解31例(34%),部分缓解43例(47%),疾病稳定16例(17%)(如下表)。

关于不良反应,研究结果显示:信迪利单抗的安全性结果与纳武利尤单抗和帕博利珠单抗既往研究中的安全性数据相符,未发现预期以外的副反应。发热是最常见的副反应,多为1-2级轻度反应;发热多发生于治疗的24小时内,并于24小时内缓解,不需要特殊处理,下次治疗时不需药物预防,也不会反复发生。研究中只有3例患者因为不良反应而停用治疗,无不良反应导致的死亡。
关于生活质量,研究结果表明:随着治疗的进行,患者总体生活质量明显改善。
“ORIENT-1研究结果充分显示了信迪利单抗治疗复发难治cHL的疗效,同时也显示了该药良好的安全性和耐受性。”石远凯教授告诉记者,研究结果表明,不论既往接受过何种治疗,所有类型患者均可从信迪利单抗治疗中获益,这与纳武利尤单抗和帕博利珠单抗研究得出的结果一致。“换句话说,国产的信迪利单抗治疗复发或难治性cHL的疗效与进口的同类药物不相上下。”
其他
据悉,基于ORIENT-1研究,信迪利单抗已经于2018年12月24日正式获得国家药品监督管理局的上市批准。
据介绍,除了复发或难治性cHL,信迪利单抗还开展了20多项其它临床试验,包括一线非鳞非小细胞肺癌、一线肺鳞癌、二线肺鳞癌、EGFR-TKI治疗失败的EGFR突变阳性的非小细胞肺癌、一线胃癌、一线肝癌、一线食管癌、二线食管癌等。截至目前,已有超过1000例中外肿瘤患者参加了信迪利单抗的相关临床试验。
-
科技前沿

-
科技前沿
-
项目成果

-
焦点事件