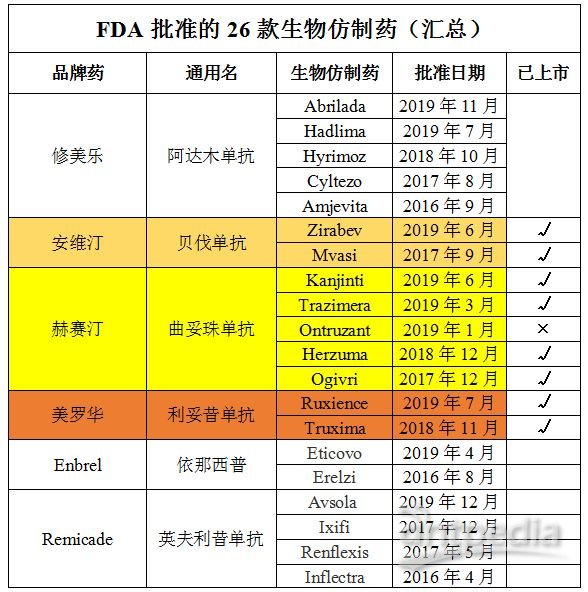
罗氏三大王牌全面沦陷 美国FDA已批准的9个生物仿制药
以色列制药巨头梯瓦(Teva)与合作伙伴韩国生物制药公司Celltrion近日联合宣布,在美国市场推出曲妥珠单抗生物仿制药Herzuma(trastuzumab-pkrb),该药所针对的品牌药为罗氏的王牌生物制剂Herceptin(赫赛汀,通用名:trastuzumab,曲妥珠单抗)。
Herzuma于2018年12月获得美国FDA批准,符合FDA严格的生物仿制药标准。该药批准基于对基础分析相似性数据、非临床数据、临床药理学、免疫原性、临床疗效和安全性数据的综合数据包的审查。临床开发项目结果表明,Herzuma和赫赛汀在纯度、效价、治疗HER2高表达乳腺癌的疗效和安全性方面没有临床意义的差异。
Herzuma与Herceptin具有相同的适应症,包括:(1)辅助治疗HER2过表达的淋巴结阳性或淋巴结阴性(ER/PR阴性或具有一个高危特征)乳腺癌;(2)一线或多线治疗HER2过表达转移性乳腺癌。(3)治疗HER2过表达的转移性胃或胃食管交界腺癌患者。在这些适应症中,患者肿瘤应采用FDA批准的曲妥珠单抗产品的伴随诊断试剂盒进行筛查。
梯瓦与Celltrion于2016年10月达成独家合作关系,开发多款重磅生物制剂的生物仿制药。梯瓦将在美国和加拿大对Herzuma进行商业化。价格方面,Herzuma 150mg和420mg的批发采购成本(WAC)分别为1402.5美元、3927美元,较罗氏品牌药Herceptin的WAC低10%。由于WAC价格不包括额外的回扣和折扣,因此患者和医疗服务提供者的Herzuma实际成本预计将低于WAC。此外,根据患者的保险以及是否有资格参与援助计划,自付费用可能有所不同。
经查询美国FDA生物仿制药数据库,截至目前,共有26个生物仿制药获得了FDA批准,其中9个针对罗氏三大王牌生物制剂:赫赛汀(5个)、安维汀(2个)、美罗华(2个)。
根据公开信息,针对罗氏三大王牌生物制剂的9个生物仿制药中,8个已经在美国上市,包括:
——4个赫赛汀生物仿制药:安进/艾尔建Kanjinti(2019年7月上市)、迈兰/百康Ogivri(2019年12月上市)、辉瑞Trazimera(2020年2月上市)、梯瓦/Celltrion公司Herzuma(2020年3月上市)。
——2个安维汀生物仿制药:安进/艾尔建Mvasi(2019年7月上市)、辉Zirabev(2019年12月31日上市)。
——2个美罗华生物仿制药:梯瓦/Celltrion公司Truxima(2019年11月上市)、辉瑞Ruxience(利妥昔单抗,美罗华、2020年1月23日上市)。
特别值得一提的是,9个生物仿制药中唯一获FDA批准但无上市消息的默沙东/三星Bioepis的Ontruzant(赫赛汀生物仿制药),该药于2019年1月获批,目前尚未查到上市相关消息。2020年2月,默沙东宣布剥离女性健康产品、成熟产品和生物仿制药成立新公司NewCo。
-
项目成果

-
项目成果
-
焦点事件

-
招标采购