《Science》:探索人类大脑疾病的生物学基础
发表在《Science》杂志上的这项研究整合了广泛的基因组学数据,以帮助发现精神分裂症、自闭症和其他神经精神疾病的分子基础,北卡罗来纳大学教堂山分校的Hyejung Won博士是本文的共同第一作者。

Hyejung Won, PhD
研究小组开发了一个空前复杂的模型,将DNA与基因活性变化以及大脑疾病风险联系了起来。
该模型取材于数千名健康人和患有大脑疾病的志愿者,现在,科学家们把它们变成了一个探索精神分裂症和自闭症等无法治愈疾病生物学基础的工具。
“为了理解大脑,我们创建了迄今为止最全面的功能基因组资源,它整合了不同类型的基因组数据库,以建立深入了解大脑疾病的生物学框架,”文章共同一作、北卡罗莱纳大学医学院遗传学助理教授、神经科学中心成员Hyejung Won博士说。
在过去几十年里,科学家们进行了数百项研究,收集了大量人群的DNA序列和相关数据以确定DNA突变和疾病相关的基因组联系。基因组学研究为许多疾病的生物学原因提供了重要线索。
然而,传统的基因组学似乎对精神疾病和许多常见的脑部疾病没那么有用。例如,精神分裂症在基因组上有100多个风险位点,但这些位点中的大多数不包含任何基因,因此我们不清楚它们是如何与疾病产生联系的。此外,许多精神分裂症相关基因突变对疾病的风险影响极其微弱,科学家一致认为,许多大脑疾病太复杂了,以至于无法用传统的一维基因组学方法来加以理解。
为了寻求更复杂的方法。几年前,一队基因组学专家成立了PsychENCODE共同体,开始汇集各种基因组学研究数据,并设计工具挖掘不同类型数据之间的关系。
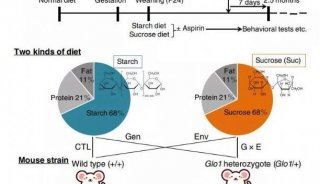
采样人群包括不同类型的精神分裂症、双相情感障碍和自闭症谱系障碍患者,基因组数据类型包括DNA序列、特定类型脑细胞的基因表达数据、促进基因表达的DNA区域地图,以及影响基因活性的基因组特征。
Won还提供了她自己的染色体构象,染色体构象是指细胞核内环状DNA的三维组织,位置不同的环足以影响基因表达。Won还建立了一个研究染色体构象和其他基因组因子如何调节脑细胞基因表达的复杂模型。
研究小组使用基因调控网络模型评估了之前有报道的142个精神分裂症风险位点,这些风险位点不包含基因,因此怀疑它们是通过影响基因表达的方式导致疾病。模型筛选出321个风险位点的可能调控靶基因,其中包括了一些已知的精神分裂症风险基因。Won等人发现,这些基因影响突触、乙酰胆碱受体、离子通道和其他相关通路功能。更重要的是,他们指出,精神分裂症主要是神经元紊乱,而不是其他脑细胞紊乱。
这是一个人工智能驱动的“深度学习”模型,基于基因变异和基因表达数据估计精神病症状风险。科学家将其与现行的一个简单的基于个体基因组预测精神病的模型进行了比较。
“深度学习模型更复杂,但更精确,我们认为用它来评估患者患病风险更有意义,”Won说。
她与PsychENCODE的同事们正在继续拓展模型,整合更多类型的基因组数据,并将分析结果扩展到精神分裂症以外的其他脑部疾病。
-
科技前沿