抗体药研究的渐变之路(一)
20世纪90年代末,治疗药物主要由小分子化药主导。而在近几十年里,人类生命健康领域基于抗体药物疗法的使用呈现了指数级增长,并成为了治疗药物的一大组成部分。抗体已被证明在治疗包括癌症、自身免疫、传染病甚至神经退行性疾病在内的多种疾病方面具有广泛的用途[1]。FDA仅在2018年就批准了59款新药,创造了历史新高(图1)[2]。截止到目前,已有超过550种有希望的候选抗体处于不同的临床试验阶段。它们目前占全球100强药品销量的20%,而2007年这一比例仅为1%。[1,2]
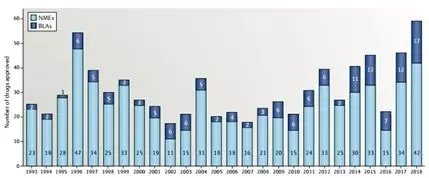
图1. 自1993年FDA批准的创新药物[2]
抗体治疗药物的发展如此气势磅礴,小编在这里得给大家提两位大师,美国的生物学家Gerald Edelman 和英国的生物化学家Rodney Porter,因他们研究发现了抗体片段的原子分辨率结构,在1972年被授予了诺贝尔奖(图2)随后GeorgesJ. F. Kohler和Cesar Milstein两位科学家以此为基奠,利用杂交瘤技术获得了单克隆抗体(mAb),进而开启了现代抗体的工程时代。


Gerald Maurice Edelman Rodney Porter
图2. 1972年诺贝尔奖获得者[3,4]
单克隆抗体制备经典流程
单克隆抗体的产生得益于杂交瘤技术的发展,那么单克隆抗体是如何制备的呢?下面小编给大家简单概括一下,如图3所示:
①将抗原注射到小鼠体内,几周后取出脾脏并提取脾细胞;
②,③,④将小鼠的脾细胞与骨髓细胞融合以产生杂交瘤细胞,每个杂交瘤细胞无限地产生相同的抗体,然后使用抗原/抗体测定法筛选杂交瘤细胞,锁定那些能产生预期抗体的细胞;
⑤细胞也可以冷冻并保存以备后用。这种制备流程很好用,可以比较容易地产生大量相同的特异性抗体;
⑥将产生优选抗体的杂交瘤细胞再集合重新筛选多次,直至分离出纯系;
⑦,⑧这些细胞还可以在培养物中生长或注射到小鼠体内以诱导肿瘤。
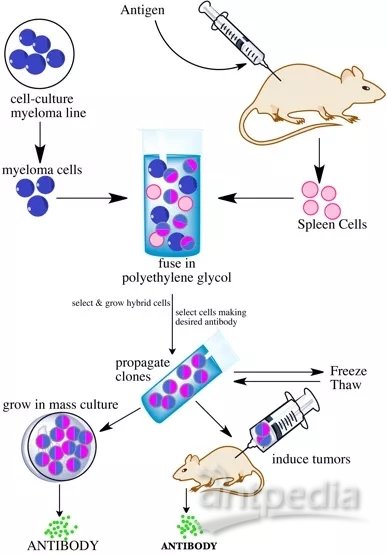
图3. 杂交瘤法生产单克隆抗体流程图[5]
虽然上述方法已证明是稳健的并且仍广泛用于产生单克隆抗体,但在临床应用上却出现了一定限制。
别急,别急,小编来告诉你。
因为早期使用的B淋巴细胞和骨髓瘤细胞来自小鼠,所产生的抗体来自小鼠的基因组(称为“鼠抗体”),它们在人体中具有免疫原性,人体免疫系统会将鼠的mAb识别为外来抗原并产生免疫应答(称为HAMA效应)。
进入人体内的小鼠单克隆抗体很快就会从循环中排出,在某些情况下也会发生过敏反应。此外,小鼠mAb的恒定区(部分免疫细胞识别部分)不能正常与负责抗体作用的人类细胞上的受体相互作用。因此,小鼠单克隆抗体很少产生对人体所需的治疗效果,并且可能不安全。此后,科学家们纷纷开始向着mAb具备“人性化”的方向而努力。有一个很简单的解决方案就是使用人的B淋巴细胞代替小鼠的B淋巴细胞,但这并不奏效,因为一方面,来自人细胞的杂交瘤是不稳定的,人B细胞不会产生针对人体组织的抗体;另一方面,用一些抗原来免疫人类会带来安全与伦理道德问题。[6]
人鼠嵌合,人源化与全人单克隆抗体的开发
为了得到能够应用于临床上的mAb,科学家们坚持不懈的开发抗体。到目前为止,已开发出三个关键类型的抗体(图4):人鼠嵌合抗体(小鼠的可变区+人的恒定区),人源化抗体(小鼠CDR区+人的Igscaffold)和全人单克隆抗体(全人氨基酸)。[7]