Cell:内质网应激与退行性疾病
加州大学旧金山分校(UCSF)的科学家们对内质网应激(Endoplasmic reticulum stress)进行深入研究,揭示了细胞中的一个关键质控网络。他们在此基础上开发了一种抑制剂,并用它来处理ER应激的动物模型。研究显示,这种抑制剂能够为细胞提供保护,治疗退行性的失明和糖尿病。
ER应激会通过内质网跨膜蛋白IRE1α,触发未折叠蛋白反应(UPR)。UPR是一个决定细胞生死的信号传导网络,当未折叠蛋白在内质网上增多时,UPR会帮助它们正确折叠,使细胞适应压力条件。但如果ER应激的水平过高或者时间过长,IRE1α就会促使细胞凋亡。
这项发表在Cell杂志上的研究,不仅有助于人们进一步理解UPR机制,也为多种相关疾病开辟了新的药物开发途径。
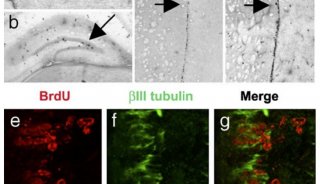
研究人员采用了两种疾病模型,视网膜色素变性(retinitis pigmentosa)的大鼠模型和Akita小鼠。在视网膜色素变性中,眼部感光细胞出现进程性死亡,最终可能致盲。Akita小鼠携带的遗传突变,会使胰腺中的胰岛素生产细胞(beta细胞)的现退化,进而引发糖尿病。
研究显示,激酶抑制剂KIRA6能够阻止眼部感光细胞的死亡,保持细胞数量和视觉功能。而在Akita小鼠中,KIRA6成功避免了beta细胞的死亡,使胰岛素生产增加了两倍,大大改善了机体的血糖控制。
“这是一个重大的进展,”文章的资深作者之一,UCSF的副教授Scott A. Oakes说。“视网膜色素变性和糖尿病表面上看来是两种截然不同的,但我们的研究指出,IRE1诱导的细胞死亡是它们共同的根源。”
文章的另一位资深作者UCSF的副教授Feroz Papa介绍道,这是一项浩大工程所结的硕果,由7个实验室的24名研究者耗时四年才得以完成。研究人员首先解析了IRE1通路与退行性疾病之间的关系,然后设计化合物对其进行干涉。他们合成了一系列化合物,KIRA6是最优化得一个,KIRA是Kinase-Inhibiting RNase Attenuators的缩写。
“尽管KIRA6在动物实验中很有效,”Papa说。“但它还需要进一步的优化,之后才能进入临床试验阶段。”
-
焦点事件

-
焦点事件

-
技术原理

-
精英视角