CRISPR技术如何带火了基因编辑小鼠?
2013年,一种名为的“CRISPR”的基因编辑技术出现后,“基因编辑”这个词汇不经意间火了,传遍了整个学术圈、生活圈,甚至是朋友圈。它的出现让“编辑生命”变得触手可及,它似乎可以斗过癌症(白血病)和艾滋病,还有各种遗传病。
我们知道,目前这些人类疾病都没有办法从根本上治疗,而它们几乎都和基因突变相关。基因编辑的出现为我们人类健康带来巨大的福音,与此同时,基因编辑的小鼠日渐成为不可忽视的大明星,为人类疾病临床前研究作出了不可估量的贡献。本期的内容就是一起看看基因编辑小鼠如何一步步成长并成为我们必不可少的研究工具。
一、基因编辑小鼠定义
基因编辑小鼠:利用基因编辑的方法改变小鼠目的基因片段,实现对特定基因片段进行敲除,引入突变或外源基因等,从而获得基因修饰的小鼠,主要分为基因敲除(KO)、基因敲入(KI)、条件性敲除小鼠(CKO)等。
二、基因编辑小鼠重大意义
由于疾病包括癌症、罕见病(β-地中海贫血、肌肉萎缩症等)都与基因突变有关,基因编辑构建的疾病模型已经成为现代生命科学基础研究和药物研发领域不可或缺的工具。
1.基因功能研究
基因编辑的小鼠,被广泛应用于研究基因在小鼠中的功能,由于小鼠与人有90%同源基因,因此这些基因功能可以类推至人类身上。比如对于P53基因敲除鼠的研究让我们确认了这一著名的抑癌基因的功能。
2.疾病机理研究
利用基因编辑在小鼠身上模拟人类疾病,是一条研究疾病机制的捷径。苯丙尿酮症是一种苯丙氨酸代谢障碍导致的常染色体隐性遗传病,有较高发病率,且对患儿有极大伤害。在PAH基因第12外显子敲除2bp(PAH416STOP)或将PAH蛋白序列408位精氨酸替换为色氨酸(PAHR408W)可以构建典型的苯丙尿酮症小鼠,多用于发病机制与治疗手段的研究。如下图为敲除鼠毛色减退,并且血苯丙氨酸含量高于野生型小鼠。

3.药物研发的重要工具
通过基因改造使基因敲除或添加的小鼠,成为癌症、动脉粥样硬化、骨关节炎、肌肉萎缩症和帕金森氏症等一系列人类疾病的关键研究模型。我们利用基因修饰的疾病模型,开发药物或者采用基因编辑技术修复突变基因,从而治愈疾病成为可能。2016年刘明耀教授课题组就利用CRISPR/Cas9技术治愈了F9突变小鼠的B型血友病。
三、基因编辑技术小鼠变得日益简单
自首个转基因小鼠在1974年由Rudolf Jaenisch培育出后,Jackson Lab和其他实验室一直在致力于基因小鼠的构建,然而其步骤繁琐,辛苦费力,涉及利用基因工程技术改变小鼠的胚胎干细胞,将其注射进胚胎,并且培育若干代小鼠。即便是JAX最好的团队,也要用2年时间才能成功改造一只小鼠。而CRISPR的出现,颠覆了所有的一切,它能在6个月内就产生基因修饰的的小鼠。
基因编辑技术小鼠发展历程
1.ES基因打靶技术
出现时间:1987年,Capecchi和Smithies根据染色体同源重组的原理,在小鼠胚胎干细胞(mES)水平首次实现了外源基因的定点整合,这就是广为人知的ES基因打靶技术。
原理:利用基因打靶获得的阳性ES细胞再经过胚胎显微注射,最终就可以得到基因敲除/敲入小鼠。
优势:作为早期的基因编辑技术,克服了随机整合的盲目性和危险性,是一种理想的修饰、改造生物遗传物质的方法。尤其是条件性、可诱导性基因打靶系统的建立,使得对基因靶位点在时间和空间上的调控更加精确。
缺点:基因打靶依赖于DNA同源重组修复机制,效率非常低(1/106);并且通过ES基因打靶获得目的基因修饰的小鼠周期很长。
2.人工锌指核酸酶—ZFN
出现时间:1996年,Kim等人利用锌指蛋白融合FokI核算内切酶,成功构建了人工锌指核酸酶(zinc Finger Nucleases,ZFNs)。
原理:如下图,ZFN的DNA识别域由3至4个Cys2-His2锌指蛋白串联组成,每个锌指蛋白识别并结合一个特异的三联体碱基。当DNA识别域特异结合到目的基因时,核酸内切酶就能够切割目标DNA序列。
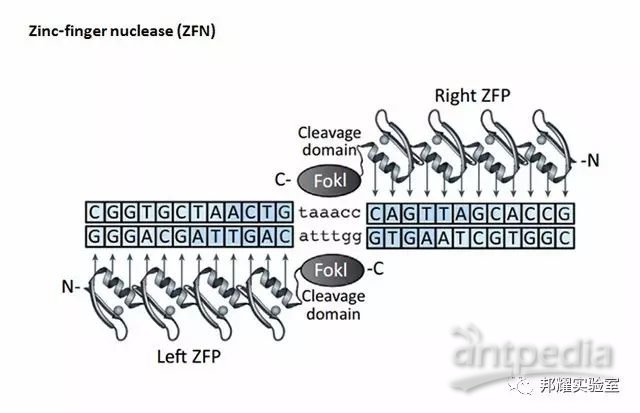
优点:同传统的打靶技术相比较,其效率提高了100倍以上。同时,可通过受精卵显微注射直接获得基因修饰小鼠,节省了大量时间。
缺点:费用高昂,工作量大,并且最终产生的ZFNs会产生细胞毒性。
3.转录激活因子样效应物核酸酶-TALEN
出现时间:2011年科学家首次把TALE 与FokI 结合在一起组成转录激活因子样效应物核酸酶(TALENs),并证实了TALEN能够对目标基因进行切割。
原理:如下图,TAL效应子可被设计识别和结合所有的目的DNA序列。对TAL效应子附加一个核酸酶就生成了TALENs。TAL效应核酸酶可与DNA结合并在特异位点对DNA链进行切割,从而导入新的遗传物质。

优点:相比于ZFNs,TALEN的获取更加简单方便,花费较低,细胞毒性相对ZFNs较低,因此自出现起就获得了广泛应用。
缺点:依然有一定的细胞毒性,且模块组装过程复杂繁琐,难以实现多基因和多位点的修饰。
4.规律间隔的短回文重复序列(CRISPR)
出现时间:CRISPR/Cas9系统是细菌或古生菌防御外源核酸(如噬菌体和质粒DNA)入侵的一套防御机制,于2013年被发现应用于基因组修饰。
原理:如下图,通过设计向导RNA(Guide RNA,gRNA) 序列并将Cas9蛋白引导到基因组的特定位点上,然后通过Cas9 的核酸酶切割活性造成DNA 断裂。
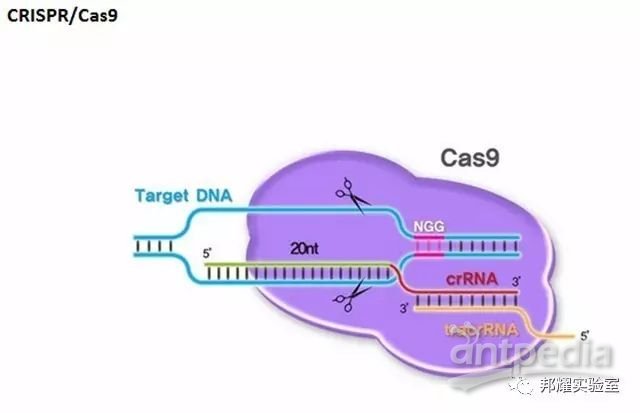
优势:被喻为“魔术剪刀”,可以高效定点的实现基因编辑。相比于ZFN和TALEN,CRISPR/Cas9技术具有二者无法比拟的可操作性,构建时间成本大大降低,并且简便高效的特点极大地推动了生命医学领域的研究,并为根治诸多遗传疾病带来了新的希望。
近年来,随着CRISPR/Cas9技术的出现,使基因编辑小鼠似乎变得唾手可得,构建一只基因编辑小鼠仅需要4-6个月。因此,越来越多的高分文章开始采用该小鼠模型进行相关疾病和基因功能的研究。
所以说,目前不仅仅是牛人开始谈论起基因编辑小鼠,身边的同学们也纷纷涌入这类小鼠的研究。所以,想想你的课题需要构建此类疾病模型吗,需要研究某个基因功能吗?如果需要,那就赶紧撸起袖子干吧,因为一切已变得前所未有的简单!
参考文献
1.Thomas KR, Capecchi MR.Site-directed mutagenesis by gene targeting in mouse embryo-derived stem cells. Cell. 1987;51(3):503-12.
2.Kim YG, Cha J, Chandrasegaran S.Hybrid restriction enzymes: zinc finger fusions to Fok I cleavage domain. Proc Natl Acad Sci U S A. 1996;93(3):1156-60.
3.Porteus MH, Carroll D. Gene targeting using zinc finger nuclease. Nat Biotechnol. 2005 ;23(8):967-73.
4.Cathomen T, Joung JK. Zinc-finger nucleases: the next generation emerges. Mol Ther, 2008, 16(7): 1200-7.
5.Kay S, Hahn S, Marois E, et al. A bacterial effector acts as a plant transcription factor and induces a cell size regulator. Science, 2007, 318(5850): 648-51.
6.Boch J.TALEs of genome targeting.Nat Biotechnol. 2011;29(2):135-6.

























