单细胞检测技术在肿瘤研究中的新挑战和新方向(二)
三.残留病变和复发:利用单核分析(冰冻材料)
在许多癌症类型中,初始治疗后通常伴随着具有增强的侵袭性和抗药性的复发,突出了残留病变及其进展和生长对于建立复发性肿瘤的重要性。已有的研究比较了原发性和复发性肿瘤,并揭示耐药性的各种遗传原因。未来的研究将扩展这种方法,通过scRNA-seq进行比较,并提供更详细的复发肿瘤视图及其与相应原发肿瘤的区别。但是,一个重要的挑战是,目前的scRNA-seq方案需要新鲜肿瘤样本,在给定复发时间的情况下,为处理匹配的原发和复发样本就比较困难了。不过,已有多种方法可以实现冷冻样品的分析,如最近已有报道,可以通过单细胞核(而不是单细胞)的分离和测序来分析冷冻或固定的样品。除了复发性肿瘤外,scRNA-seq还直接发现通过治疗而存活的罕见残留细胞,而它们正是最终成为肿瘤复发的基础。
这种罕见细胞,通常被称为微小残留病变(MRD),可以在动物模型中进行分析,通过与原发性和复发性肿瘤进行比较,为其逃避治疗的能力,保持休眠状态,最后引起复发性肿瘤的过程提供了解释。
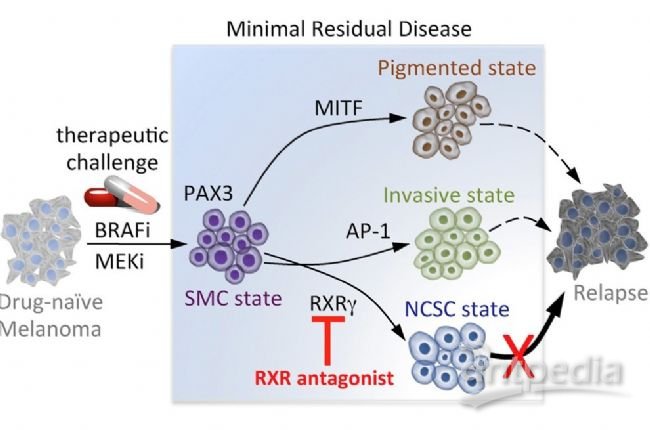
来源:Rambow et al., 2018
四.肿瘤亚群:它们的检测,功能意义和起源
肿瘤进展是一个进化过程,因此,只有少数细胞得以通过选择而逐渐形成新的表型。所以,关键亚群,如癌症干细胞,耐药细胞和构成转移的迁移细胞,可能反映了一种非常罕见的亚群(例如,小于0.1%)。然而,这种亚群大多数方法是检测不到的,包括目前的scRNA-seq。不过,随着目前单细胞检测通量的不断提高,像以微滴微流控为代表的技术,使得每批次检测的细胞数据可以达到成千上万。当然,未来的技术肯定会进一步地将这种能力提高到数万甚至数百万个细胞,这将大大地提高发现非常罕见亚群的可能。
当然,即使发现了这些独特的亚群,它们的功能和临床意义也是很难确定的。不过,有两种重要的方法可以进一步分析这些亚群:1.大型列队的研究可以揭示亚群存在和频率与临床特征(例如存活,转移和药物反应)之间的统计关联。但是考虑到大样本进行scRNA-seq的成本问题,目前相对可行的方法是利用已有可用的测序数据集(常规RNA测序或者单细胞测序),利用计算方法来找到数据特征和肿瘤的关联;2.利用scRNA-seq数据,结合这些亚群的详细细胞表型来鉴定能够区分这些亚群的标记,同时在动物或者模型中做进一步的功能研究。最新的一些scRNA-seq研究就发现肿瘤表达谱与正常发育细胞之间的相似性,提出了关于肿瘤起源和其中发生的持续分化过程的具体假设。像人类图谱计划(HCA)这样的对肿瘤,正常组织和发育过程进行scRNA-seq的研究,在未来将会做的更多更广,也将有更多的发现。比如,对H3-K27M
midline胶质瘤的scRNA-seq发现恶性细胞与少突胶质细胞前体细胞(OPCs)之间的相似性,与之前文献报道的OPCs是该肿瘤的起源候选细胞结论一致。此外,恶性细胞和正常细胞之间的比较不仅突出了它们之间的相似性,还提供了肿瘤细胞和其假定的起源细胞之间差异的详细数据,增进了我们对致癌过程的理解。

来源:Filbin et al., 2018
五.独特的肿瘤表型和特殊反应群体:N = 1组的单细胞分析
尽管常规的治疗决策是基于大群体的统计结果,但是异常值也是非常常见的,而且具有非常重要的作用。例如,“特殊反应者”表明了我们对治疗反应和理论疗效的局限性认识。在过去,我们通过对这些病例的bulk测序进行遗传分析,但很难去理解他们的表型独特性。随着scRNA-seq等相关技术的发展,为我们理解这些独特表型提供了可能。当我们发现特有表型时,针对这样的N=1样本进行scRNA-seq可能对于理解其表型的分子基础非常有用。
长期以来,由于缺乏准确测量肿瘤中单个细胞的分析工具,肿瘤异质性使得肿瘤生物学家和临床医生感到困惑。而肿瘤单细胞检测技术的发展使得困惑可能得以一一解开。通过检测单细胞转录组数据,有可能为我们重新定义肿瘤起始和进化奠定理论基础。通过对肿瘤中单细胞的全面分析,将有助于我们对肿瘤的了解和个性化治疗。目前,人类肿瘤单细胞基因组学研究才刚刚兴起,但随着技术的发展,研究的不断深入,将为我们更多的发现铺平道路。
文献来源
Suva, M. L. and I. Tirosh (2019). "Single-Cell RNA Sequencing in
Cancer: Lessons Learned and Emerging Challenges." Mol Cell 75(1): 7-12.