蛋白质组发现明星分子KRAS为胰腺癌“充电”新机制
来自德州大学的Giulio Draetta教授及其同事发现胰腺癌细胞表面的一种名为syndecan-1(SDC1)的蛋白质可以响应胞内KRAS的信号,并促进巨噬细胞的破坏作用。这项研究发表于最新的《Nature》杂志。

Letter | Published: 27 March 2019
Syndecan 1 is a critical mediator of macropinocytosis in pancreatic cancer
原文链接:https://www.nature.com/articles/s41586-019-1062-1
肿瘤细胞有恶性无限增殖能力,而这种能力需要大量的能量来支持。很显然,常规的能量代谢频率并不能满足贪婪的肿瘤细胞,它需要借助巨噬破坏其他正常细胞才能满足其自身的能量供应。这种调控巨噬获得能量的机制尚不明确,是目前研究热点之一。

胰腺导管腺癌(PDAC)是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤。90%胰腺导管癌中存在Kras突变。这种突变会通过尚不明确的机制激活肿瘤微环境的巨噬细胞,并促进巨噬细胞的胞吞作用。
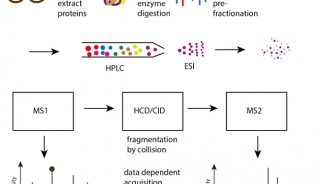
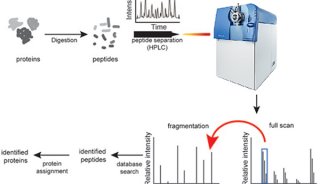
为了准确地找到胰腺导管腺癌的代谢,Giulio Draetta团队发起了挑战。他们构建了Kras开放和关闭状态下的模型,并通过蛋白组学技术,广泛筛选与研究KRAS相关的细胞表面蛋白,以期寻找治疗胰腺癌的新靶点。
探索攻略
实验材料:PDAC小鼠模型细胞-- Kras OFF vs Kras ON
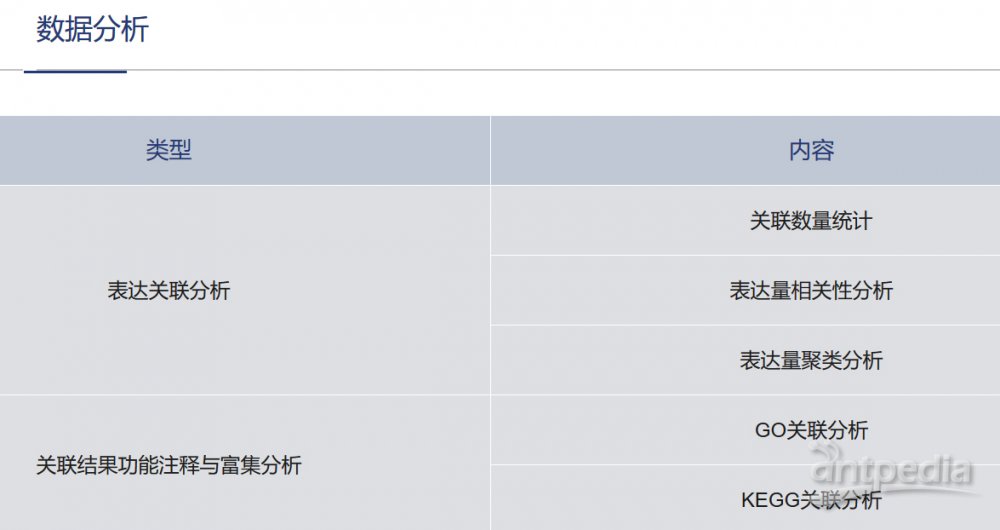
1、定量蛋白组分析Kras信号传导带来的变化
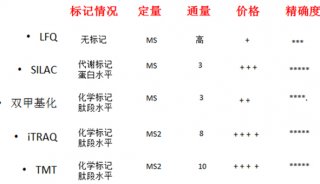
为了探讨Kras信号传导带来的细胞表面蛋白表达变化,研究团队利用SILAC定量蛋白质组技术比较了Kras OFF与Kras ON差异。此次分析共获得221个差异表达的蛋白,其中196个蛋白上调,25个下调。
2、生信分析讨论功能与通路
IPA(Ingenuity pathway analysis)分析显示,许多上调表达蛋白参与PDAC被激活的生物过程,包括轴突导向信号通路,这个结果支持了KRAS*是PDAC分子重编程的主要驱动因素的观点。
3、锁定关注蛋白
研究人员选择了在人源PDAC细胞系中同样存在的110个蛋白,以及37个在细胞表面高表达的基因,构建了一个shRNA文库,并以此构建小鼠模型。
进一步分析发现硫酸肝素蛋白聚糖家族中的SDC1在Kras表达过程中,在质膜上显著富集。
而在蛋白组分析结果中,SDC1也同样高度富集。因此,研究人员在后续研究中,锁定了SDC1作为关注蛋白。
4、关注蛋白功能验证
后续验证实验表明,SDC1的缺失可以显著抑制皮下异种移植瘤的生长,也会抑制肿瘤细胞的克隆形成和致瘤性。
种种实验结果均说明了iKras*肿瘤细胞表面的SDC1对疾病进展至关重要。而它的工作方式则是通过调控巨胞饮为肿瘤细胞的生长提供能量。

小结
该研究利用蛋白组学技术广泛检测了因Kras状态改变而引起的细胞表面蛋白变化。
在差异蛋白中层层筛选,获得关注蛋白,并进行了大量的功能验证,最终在KRAS*信号传导和PDAC中驱动营养回收通路的靶分子之间建立了一种机制联系。
也为后续的肿瘤研究提供了通过分析表面蛋白表达差异,寻找癌症特异性弱点的策略。