冠状病毒是一种自然界普遍存在的单股正链RNA病毒,电镜下呈日冕状或皇冠状,故命名为冠状病毒。在本世纪初短短20年中,共爆发了三次冠状病毒疫情,即2003年SARS-CoV、2012年MERS-CoV和2019年SARS-CoV-2,极易引起呼吸道系统感染并在人与人间传播,严重威胁人类生命。其中,SARS-CoV-2如今更是造成了全球300多万人死亡,1.4亿人感染,再次刷新了人们对于冠状病毒危害性的认识。因此,准确、深入地研究冠状病毒及其感染宿主细胞过程的生物学特征,并开发高效地防治药物及疫苗,成为了全世界科学家迫在眉睫的挑战。
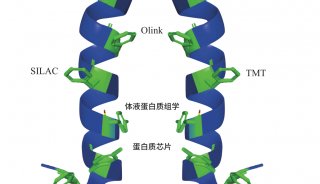
基于生物质谱的蛋白质组学是精准研究冠状病毒侵染宿主细胞动态过程的重要手段,通过对SARS-CoV-2感染样本(细胞系、组织、血液、尿液等)进行高通量的蛋白质组学研究,已经成功帮助生命科学家在短短两年之内迅速扩展了对SARS-CoV-2生理、病理学调控机制的了解。其中,2020年9月,运用景杰生物的4D蛋白质组学对新冠肺炎病毒患者的肺组织石蜡切片进行超高深度的蛋白质定量分析,华中科技大学同济医学院联合哈佛医学院研究团队揭示了SARS-CoV-2感染后,肺组织免疫应答以及炎症反应调控机制与关键蛋白质【1】。然而,目前尚未有研究利用组学同步比对SARS-CoV-2与SARS-CoV之间的差异性。近日,来自慕尼黑工业大学的病毒免疫病理学主席Andreas Pichlmair教授联合蛋白质组学资深教授Matthias Mann等人,在Nature上发表了题为“Multilevel proteomics reveals host perturbations by SARS-CoV-2 and SARS-CoV”【2】的文章,他们通过进行转录组、蛋白质组、泛素化修饰组和磷酸化修饰组学研究,系统地检测了1200多个细胞感染SARS-CoV-2和SARS-CoV前后的蛋白质功能变化,分析了这两种病毒蛋白质与宿主蛋白质的相互作用,确定了这些密切相关的冠状病毒独特以及共有的关键蛋白质,最终筛选得到两种具有显著抗病毒效果的候选药物。
首先,作者分别在A549肺癌细胞表达了24个SARS-CoV-2蛋白和27个SARS-CoV病毒蛋白。通过亲和纯化质谱(AP-MS)分析共确定了宿主1086种宿主蛋白质与病毒蛋白质间存在相互作用,其中,有293个SARS-CoV-2特异性互作蛋白,169个SARS-CoV特异性互作蛋白。细胞相互作用分析显示SARS-CoV-2和SARS-CoV调节多种细胞功能,如先天免疫调节通路、胆固醇代谢等。

图1 SARS-CoV-2和SARS-CoV的病毒-宿主蛋白相互作用网络随后,研究者用SARS-CoV-2、SARS-CoV分别感染A549肺癌细胞,分析了病毒对宿主细胞转录组、蛋白组、泛素化和磷酸化修饰组的影响。在转录和蛋白质水平上,病毒感染造成I型干扰素反应下调并激活促炎信号,其中SARS-CoV显著激活NF-κB通路;而SARS-CoV-2感染导致FN1和SERPINE1高表达,进一步说明SARS-CoV-2对TGF-β信号的调节作用。为了更好地了解病毒干扰细胞信号传导的机制,研究者比较了A549细胞在感染病毒不同时长后的蛋白质泛素化、磷酸化修饰水平,发现1108个泛素化位点 (共16541个) 和 4643个磷酸化位点 (共16399个) 在病毒感染后出现显著变化。另外,生信分析还揭示了单个宿主蛋白上的磷酸化和泛素化修饰之间的相互作用。比如,波形蛋白是冠状病毒侵染和致病的重要辅助因子,在感染的早期晚期具有不同的磷酸化和泛素化修饰水平,这些发现强调了研究不同翻译后修饰的重要意义。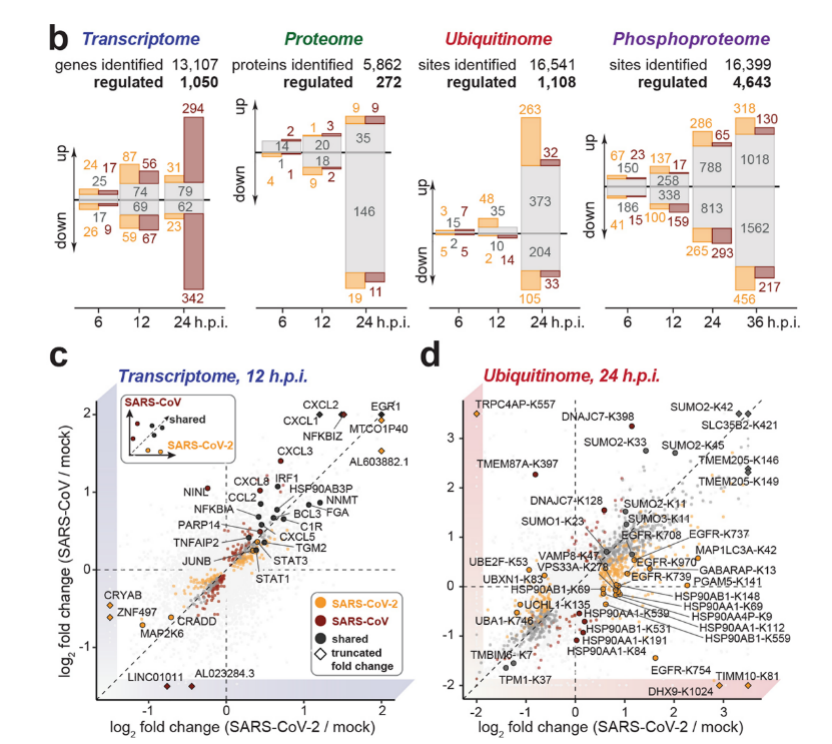
三、分析病毒-宿主蛋白相互作用和途径,指导筛选新冠病毒治疗药物
最后,作者针对新冠病毒感染涉及的主要通路,选取了48种相应的药物进行了药理学实验,这些药物通过调控病毒干扰细胞的通路,从而影响SARS-CoV-2的复制。最终,作者发现Gilteritinib,Ipatasertib,Prinomastat和Marimastat这4种药物具有显著的抗病毒效果。
总的来说,作者通过对病毒侵染细胞过程的多组学分析,多角度全面描绘了冠状病毒侵染细胞后的细胞应答过程。通过分析蛋白质相互作用和修饰水平,可以筛选冠状病毒潜在的药物靶点,从而指导候选药物的开发,加速对SARS-CoV-2乃至其他冠状病毒的防治工作。
1. Meng Wu, et al. 2020. Transcriptional and proteomic insights into the host response in fatal COVID-19 cases. PNAS. 2. Alexey Stukalov, et al. 2021. Multilevel proteomics reveals host perturbations by SARS-CoV-2 and SARS-CoV. Nature.
本文由景杰学术团队报道,欢迎转发到朋友圈。如有转载、投稿等其他合作需求,请文章下方留言,或添加微信ptm-market咨询。#关注领取新人福利,下载最近三年影响因子(后台发送关键词“新人”)