项目文章Cell Research(IF 25.617) |脂质组学技术助力靶向生物分子药物开发

脂滴(liquid drops,LDs)是一种普遍存在的脂质储存结构,LDs的异常积聚与许多疾病有关,如肥胖、心血管疾病、脂肪肝和神经退行性病变等。因此,增强LD降解可以用来治疗一些相关疾病。目前利用小分子化合物(如蛋白水解靶向嵌合体PROTACs)选择性降解致病性蛋白质已成为一种有潜力的治疗策略,但对非蛋白的致病性分子如脂滴的降解一直面临挑战。
2021年7月8日,Cell Research(IF=25.617)杂志在线发表了题为《Degradation of lipid droplets by chimeric autophagy-tethering compounds》的研究成果,利用其课题组于2019年发表的原创ATTEC(AuTophagy-TEthering Compounds)技术,将自噬体蛋白LC3的结合分子与LD检测探针(已知的LD特异性结合分子)连接来设计LD·ATTECs,首次实现了非蛋白类生物分子的靶向降解,完成了靶向降解技术从蛋白向非蛋白物质的突破,为药物研发开辟了新的途径。中科新生命提供了脂质组绝对定量技术服务。

中科新生命脂质组组学产品优势

• 全脂质分子数据库(170万脂质分子)
• 高分辨质谱平台,精确解析脂质分子
• 覆盖20+脂质亚类
• 同位素内标法绝对定量每种脂质分子含量/浓度

【研究材料】
db/db小鼠肝脏组织:DMSO组、C3组、C4组、SIII组
【技术方法】
脂质组绝对定量、蛋白质组
实验方法
步骤1:化合物设计合成与工作原理;
步骤2:LD·ATTECs通过自噬清除LD;
步骤3:体外研究:LD·ATTECs将LDs靶向自噬体而不影响整体自噬;
步骤4:体内药效研究:脂质组+蛋白质组。
研究结果
1. 化合物设计合成与工作原理
研究人员选择GW5074(GW)和5,7-二羟基-4-苯基香豆素(DP)作为LC3结合分子,使用Sudan IV或Sudan III作为LD检测探针(LD特异性结合分子),使用化学连接剂将LC3结合分子与LD检测探针连接来设计LD·ATTECs。LD·ATTECs通过疏水作用与LDs或中性脂质(以TAG为典型例子)结合,同时与自噬体蛋白LC3结合,形成LD/TAG–LD·ATTEC–LC3三元复合物。该复合物被自噬体吞噬,LD/中性脂质进而自噬降解,最后由线粒体将其转化为能量。

图1 化合物结构及其设计/工作原理
2. LD·ATTECs通过自噬清除LD
为验证LD·ATTECs效能,作者进行了验证实验。在油酸(OA)诱导6小时后,分别用LD·ATTEC1(C1)或LD·ATTEC2(C2)处理野生型(WT)小鼠胚胎成纤维细胞(MEFs);24小时后发现LDs的数量和大小均呈剂量依赖性减少。而在缺乏自噬的Atg5敲除(Atg5–/–)MEFs中这些化合物的作用被消除,说明观察到的LDs降低是自噬依赖性的。有趣的是,通过饥饿或氯化铵处理增强或抑制细胞整体自噬水平仅仅微弱改变了脂滴的水平,表明在OA诱导的模型中,选择性靶向LDs的自噬比增强LDs降解的整体自噬更有效。进一步分析确定LD检测探针和嵌合化合物中的LC3结合部分之间的连接对于LD降低是必需的,因为这两部分都不能单独诱导LD降低。

图2 LD ·ATTECs以自噬依赖的方式显著降低 LDs
3. 体外研究:LD·ATTECs将LDs靶向自噬体而不影响整体自噬
在细胞水平上,通过微尺度热泳法(MST)测定了LD·ATTECs与重组纯化的LC3B蛋白的亲和力,确认LD·ATTEC–LC3相互作用需要LC3B结合“弹头”。通过改进的ELISA分析证实了TAG–LD·ATTEC–LC3三元复合物的形成,表明合成的LD·ATTECs在体外将TAG栓系到LC3B。进一步通过共定位染色、代谢流等实验在细胞中证实LD·ATTECs通过将LDs与LC3连接而靶向增强自噬体对LDs的吞噬,且不影响整体自噬及质膜或核膜的完整性。

图3 LC3B-ATTEC-LD三元复合物的形成及LC3B与LD的共定位
4. 体内药效研究:脂质组+蛋白质组
(1)LD·ATTECs减轻代谢性疾病的表型
分别在肥胖(db/db)和非酒精性脂肪性肝炎(NASH)小鼠模型上研究LD·ATTECs在体内的作用。与对照相比,两种小鼠模型在注射两周内引起约15%的体重减轻,脂肪/瘦肉比和肝脏重量显著降低,小鼠肝脏和血清中的TAG、TC、FFA水平显著降低,LD数量和大小显著减少,证实了这些化合物在体内的作用。此外NASH小鼠肝组织间质纤维化也显著减轻,进一步表明LD∙ATTECs的潜在有益作用。

图4 LD·ATTECs减轻db/db和NASH小鼠模型的疾病表型
(2)脂质组:LD·ATTECs显著影响脂质水平
通过对db/db小鼠模型的肝脏样品进行了绝对定量脂质组学分析,发现处理组肝脏总脂质浓度显著降低,其中大多数甘油脂质、甾醇脂质和中性鞘磷脂均显著下降,对关键脂质分子进行重点分析发现,具有不同碳链长度或饱和键数的TAG和ChE均被降低,而PE和PI不受影响。这表明LD·ATTECs主要靶向降解中性脂质,对极性脂质,如甘油磷脂基本不影响,这与LD·ATTECs不损害细胞膜完整性的事实一致。


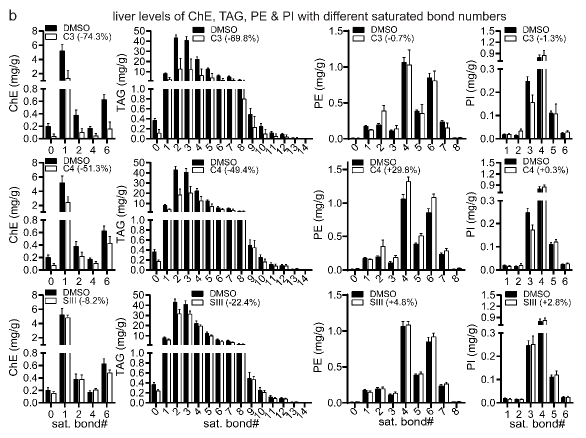
图5 LD ·ATTECs显著影响脂质水平
(3)蛋白质组:LD·ATTECs不直接干扰蛋白质水平
除脂质外,作者对小鼠的肝组织进行蛋白质组学分析,以研究LD·ATTECs在体内治疗对哪些蛋白质产生影响,并观察到LD·ATTECs治疗显著降低LD标记蛋白Plin2,但不降低SIII。脂质合成酶或脂肪酶或其辅助因子没有发生显著变化,自噬底物或核心通路基因也不受影响。上述结果表明LD·ATTECs基本上不直接干扰蛋白质水平,但不能完全排除对蛋白质水平的间接和连锁效应。
总结
本项研究以脂滴这一细胞内储存脂肪的细胞内结构为降解目标设计ATTEC化合物(LD·ATTECs),证明了组装拼接型ATTEC可将非蛋白类生物物质直接特异性靶向至自噬-溶酶体途径降解,首次实现了非蛋白类物质的靶向降解技术,并在细胞和两个独立的肝脏脂质沉积小鼠模型中拯救了LDs相关表型,脂质组学绝对定量技术的应用从多个层面上反应了LD·ATTECs对小鼠肝组织脂质的影响。这种策略为新药研发开拓了一条新的原创路径。
中科优品推荐



我知道你
在看
哦

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章

-
微信文章
-
微信文章
-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章

-
微信文章
-
微信文章