TIMS离子淌度质谱技术助力代谢物的深度空间组学表征

代谢组学是用于研究生物体内的氨基酸、糖类、脂质等内源性小分子代谢物的变化的技术。与DNA、RNA和蛋白质等大分子不同,小分子代谢物的变化更接近于生命体的表型信息,因此代谢组学研究对于理解各项生命活动、病变的产生和发展等都具有重要的意义。传统的代谢组学技术如GC-MS、LC-MS等,在对固态生物组织分析之前、常常要先做“匀浆化”处理。这样的分析策略会导致代谢物分子的空间信息的缺失。为了弥补这样的问题,人们提出了基于质谱成像的“空间代谢组学”的研究策略。
作为质谱成像市场的领跑者,布鲁克于2019年推出了timsTOF fleX,它是一款离子淌度质谱仪,同时配备了ESI和MALDI双离子源。MALDI源采用了10000Hz的SmartBeam 3D固体激光器、可以进行高速度和高空间分辨的成像数据采集;ESI源连接液相色谱分离技术并配合TIMS离子淌度分离技术、可以执行高覆盖的分子鉴定流程。以上的诸多优点将使timsTOF fleX质谱仪成为推动空间代谢组学研究长足发展的“科研利器”[1][2]。
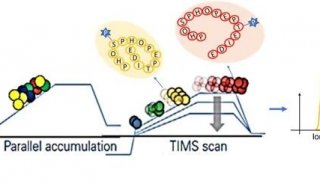
timsTOF fleX配备了布鲁克的核心专利技术 —— TIMS(捕集离子淌度分离技术)。如图1b展示了它所包含的两个TIMS分离器:气态的离子首先在Analyzer1中被“捕获”、从而累积起来,一段时间之后,这些气态离子同时进入到Analyzer2中,由于其碰撞截面积(CCS)的差异、进而以不同的迁移速度在Analyzer2中运动、从而被分离开。该设计的优势是将分散在离子传输路径中的气态离子在空间维度 “收拢”起来,并将离子的洗脱时长“压缩”在较短的离子迁移时间尺度内,从而实现了空间、时间的双聚焦效果,使气态离子的检测灵敏度得到了前所未有的提升。
图2中展示的是timsTOF fleX质谱仪分别在关闭TIMS和开启TIMS的情况下、采集小鼠鼠脑组织切片的MALDI成像数据。图2a显示的是两组成像数据的总离子流图,图2b显示的是m/z 385-387质量段的平均质谱图;蓝色代表开启TIMS获得的总离子流图和平均质谱图,黑色代表关闭TIMS获得的总离子流图和平均质谱图。通过对比两种情况下的总离子流图和平均质谱图,可以看到开启TIMS可以检测到更多信号峰,并且部分离子的信号强度也有了明显的提升。离子信号强度的提升来源于timsTOF fleX独特的空间、时间双聚焦效应。以图2b中m/z 386的离子为例,开启TIMS使的信号强度产生了5倍的提升。除此之外,信号强度的提升还带来了更好的谱峰分辨效果,图2b中m/z 386处两个邻近质谱峰在开启TIMS后、几乎实现了“基线分辨”的效果,这对于后期、数据处理软件对这两个质谱峰的分辨和检出是非常有利的。

图2:timsTOF fleX质谱仪在小鼠鼠脑组织切片上采集的(a)总离子流图(TIC);(b)平均质谱图。
TIMS技术的引入,不仅能提高离子的信号强度和检出数量,由TIMS所获取的CCS值(碰撞截面积)还为气态离子的分离提供了一个额外的分离维度。

图4展示的是timsTOF fleX成像数据的处理流程。MALDI成像数据首先导入至布鲁克SCiLS Lab软件中,建立感兴趣的目标区域(ROI)。接着将原始数据和ROI区域导入至布鲁克的MetaboScape软件之中,对目标区域的成像数据做有效信号(feature)的提取。

表1:通过MetaboScape从小鼠鼠脑成像数据中所提取的feature数目。
分别从鼠脑的小分子成像数据和鼠脑的脂质成像数据中进行有效feature提取,初步的提取结果在表1中给出。无论是小分子MALDI成像、还是脂质MALDI成像,开启TIMS所获得的feature数目呈现数倍、乃至数十倍的提升。正如前文所述。timsTOF fleX独特的双TIMS设计,一方面能极大地提高生物分子的检测灵敏度,另一方面TIMS淌度分离为信号的分辨提供了额外的分离维度,有助于数据处理软件对复杂信号的辨认和识别。
面对生物组织中数量庞大、结构繁杂的代谢物分子,布鲁克的timsTOF fleX质谱仪将TIMS离子淌度分离与MALDI质谱成像技术进行了有机结合,布鲁克顶级配置的MALDI离子源能提供高速度、高空间分辨的成像数据;布鲁克独有的TIMS离子淌度分离技术,有效地解决了生物分子中同重素和同分异构体分子在MALDI成像时出现的信号堆叠、难以有效辨别的问题。两大技术有机地结合,可以实现高空间分辨率下、代谢分子的高覆盖表征。timsTOF fleX质谱仪必将对空间代谢组学的进一步发展起到至关重要的推动作用。参考文献: [1] Resolving the complexity of spatial lipidomics using MALDI TIMS imaging mass spectrometry, Anal. Chem. 2020, 92, 13290−13297. [2] Spatial metabolomics of the human kidney using MALDI trapped ion mobility imaging mass spectrometry, Anal. Chem. 2020, 92, 19, 13084–13091.