4D-DIA蛋白组+磷酸化修饰组,临床大队列蛋白组研究“黄金搭档”

景杰生物 | 报道





4D-DIA磷酸化修饰组技术结合了以捕集型离子淌度(Trapped Ion Mobility Spectrometry, TIMS)为特征的4D蛋白质组学,及DIA策略的优势,克服DDA和传统DIA技术原有的一些劣势,真正意义上实现了优势互补。研究发现,相比4D-DIA磷酸化修饰组学定量技术可实现更大的定量动态范围、更高的鉴定重复性,并提高了定量的灵敏度和准确性,尤其适合于临床大队列蛋白质组学研究等应用,已成为细胞信号研究、临床癌症组织的蛋白质基因组学、抗病毒药物发现研究的一项强大技术。

技术优势
DIA相比于DDA的技术而言,最大的挑战就在于其混合谱图难以可靠解析。在定量的时候,主要依据色谱洗脱时间(retention time)来进行匹配。但是,由于共洗脱现象的普遍存在,仅仅依靠色谱洗脱时间是不够的,存在很多的干扰信号,而影响了检测结果的准确性。4D技术代表性的离子淌度分离,提供了额外维度的校准信息。能够更准确从DIA的混合谱图中解析出具体的肽段信号,有效降低了谱图的复杂性,全面提升了DIA检测的准确性和可靠性。

4D-DIA技术中与离子淌度相关的CCS值和m/z之间有一定的相关性,因此四级杆可以利用这个特征逐步扫描来采集近乎100%的离子信号,极大提升检测的灵敏度和深度。

4D-DIA相比于传统DIA能够更加准确的识别出低丰度的修饰肽段,进而提高磷酸化修饰鉴定深度。测试数据显示4D-DIA磷酸化从小鼠脑组织中可定量到20000+修饰位点,相比传统DIA技术提升25%。
磷酸化组分析的另一大难题是同分异构现象,4D中新增的离子淌度能够区分和识别这些共洗脱的磷酸化修饰肽段信号,尤其有利于翻译后修饰位点的精确分析。

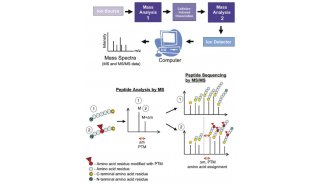
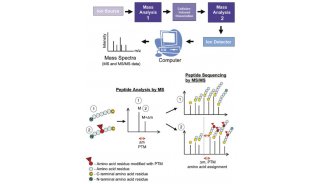
图 离子淌度对于同分异构磷酸化肽段的分离。如图所示,5号和6号肽段其保留时间和质荷比完全一样,但是通过离子淌度可以很好的分离鉴定。同时,6号和7号肽段离子淌度和质荷比一致,但可以通过保留时间进行区别。全部7个肽段中有5个可以通过离子淌度进行准确鉴定,但是保留时间只能鉴定2个。

Cell:新冠病毒侵染的磷酸化蛋白质组全景图

图 SARS-CoV-2感染的磷酸化蛋白质组学分析
参考文献:
1. Mehdi Bouhaddou,et al.,2020. The Global Phosphorylation Landscape of SARS-CoV-2 Infection. Cell.
2. Florian Meier, et al., 2019. Parallel accumulation – serial fragmentation combined with data-independent acquisition (diaPASEF): Bottom-up proteomics with near optimal ion usage. Nature Methods.