激光显微切割——空间肿瘤组学研究的利器


激光捕获显微切割(laser capture microdissection, LCM)技术是于20世纪90年代末由美国国立研究院开发的一项新技术。LCM技术可以在显微镜直视下从器官或组织切片中准确获取某个特定的细胞群或单个细胞,它的出现使解决肿瘤异质性这一难题成为可能。随着二代测序和多组学技术的发展,LCM技术作为同质化样本的重要获取手段,已成为肿瘤基础研究中的支撑技术。
LCM系统的原理及优势
LCM技术是在显著镜直视下利用激光将组织切片中特定区域的细胞切割并收集起来,目前市场上主要有四种类型的LCM系统,它们的基本工作原理相似,只是样本的收集方式略有不同,表1总结了四种LCM系统的特点及优势。以蔡司的Palm microBeam为例,先利用355nm的紫外激光在倒置的显微镜下对样本进行切割,切割时样品移动,而激光束不动,从而确保激光束始终聚焦在切割平面;待切割完成后,发射一个激光脉冲,使切下的小块组织向上弹射、进入收集装置。整个过程简单,没有任何机械接触,无污染、无热损伤,不需要特殊耗材,并且支持在普通拨片上进行切割。
相比于传统的细胞获取方法,LCM技术具有明显的优势:样品来源广泛,同时适用于福尔马林固定石蜡包埋的(FFPE)组织切片和冷冻切片;此外,部分系统还支持活细胞和染色体的切割,捕获效率高,操作简单,用户只需在显微镜观察下使用鼠标在显示屏上选择要切割的范围;而且LCM是以高能量激光进行切割,避免直接接触样品带来的外界污染,同时激光产生的热量会被瞬时冷却,不会破坏靶细胞内的DNA与蛋白质等大分子,这对于下游基因组学和蛋白质组学的分析极为重要。
表1:四种LCM系统特点及对比

LCM的样本类型
为了使待切割样本能保持组织的原始形态,在切割前一般需要对组织进行固定,常用的固定方法有两种:一种是使用的石蜡包埋、福尔马林固定,另一种是低温冷冻。石蜡包埋需历经脱水、透明、浸蜡、包埋等多个步骤,该方法较繁琐、耗时长,且可能造成萃取物的损失,并会破坏组织中DNA、RNA、蛋白质等大分子的结构。它的优点在于石蜡的固定作用能较好地保持细胞形态,形成的图像清晰、有利于观察,而且FFPE具有大量的样本来源,故此,仍有不少研究人员将它作为动植物组织切片的制备技术。而冷冻切片法在LCM中的使用频率越来越高,它具有操作便捷、实验周期短、污染小、温度可调等特点,有利于保证组织中大分子结构的完整性;操作时仅需将新鲜或固定好的材料嵌入组织冷冻包埋剂中,快速冷冻后即可切片。对于一些含水量较大的植物组织,样品在冷冻过程中往往会形成大量的冰晶,从而破坏细胞结构。近年来随着冷冻保护剂和超低温速冻法的使用,该情况得到了明显的改善。
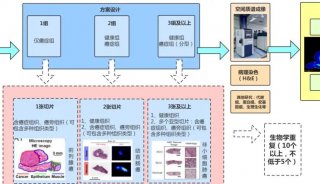
基于LCM的空间多组学实验方案
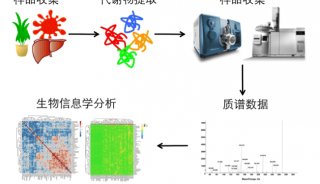
近年来,随着微量RNA提取、单细胞全基因组扩增等分子生物学技术的发展,LCM结合二代测序(NGS)、双向凝胶电泳(2-DE)、质谱等技术在肿瘤基因组学、蛋白质组学、代谢组学中展现出了巨大的潜力。
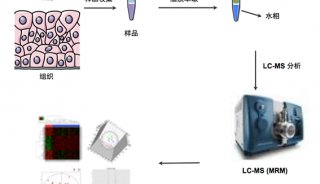
质谱法是多组学研究中发展最快、最具活力和潜力的技术,目前,常用的质谱技术主要有两种:电喷雾质谱(ESI-MS/MS)和基质辅助激光解析/电离飞行时间质谱(MALDI-TOF-MS)。布鲁克在2019年推出了基于timsTOF fleX的空间定位组学方案,将LCM与MALDI成像和ESI-MS/MS结合在一起。MALDI质谱作为一种新的分子成像技术,近年来在多组学研究中发挥了巨大的潜力,它无需标记、灵敏度高、分子特异性强,能一次从组织标本中同时检测上千种生物分子,提供其他技术无法获得空间分布信息。通过timsTOF fleX MALDI成像可以得到分子在整个组织的空间分布情况,然后可以将高表达的区域或者具有相似分子组成的区域作为目标微区(ROI)进行激光微切割,再将微切割的样本进行LC-MS/MS深度的多组学分析。与传统的“整体匀浆方法”相比,基于LCM的MALDI成像充分地考虑到癌组织中不同的肿瘤亚细胞群之间的差异性,并分别对肿瘤不同细胞群体进行了有针对性的深度多组学分析。

图2:基于timsTOF fleX的空间定位组学工作流程[2]
大数据、图像分析和机器学习
参考文献
[1] Ferdinand von Eggeling, Franziska Hoffmann. Microdissection—An Essential Prerequisite for Spatial Cancer Omics. Proteomics. 2020, 20:17-18.
[2] Dewez F, Oejten J, Henkel C, Hebeler R, Neuweger H, De Pauw E, Heeren RMA, Balluff B. MS Imaging - Guided Microproteomics for Spatial Omics on a Single Instrument. Proteomics. 2020, 20(23).