文献分享 | 时间梯度的蛋白质组学和泛素化蛋白质组学用于TPD药物开发

蛋白激酶、离子通道、受体等人体蛋白是当前药物开发最常用的药物靶标。截至 2015 年,美国食品药品监督管理局(FDA)批准的1578种药物分子靶点中 667 种为人源蛋白,占总药物靶点的 75%以上。随着人类基因组成功测序及不断深度解析,构成人类基因组的蛋白质编码基因的实际数目确定为2万多,存在大量潜在药物靶点。
传统靶点确认及干预策略包括使用小分子拮抗剂与靶蛋白特定位点结合来阻断或调节蛋白质功能,然而,细胞内超80%蛋白质如骨架蛋白、转录因子和非酶蛋白等尚未发现有效小分子拮抗剂。同时,该种“占位驱动(occupancy driven)”作用模式需持续占据靶蛋白活性位点,要求小分子拮抗剂具有高亲和力、长半衰期且一般使用量较大以满足靶点饱和,导致毒副作用大且易产生耐药。为突破现有药物研发技术的诸多瓶颈,靶向蛋白降解(TPD)技术应运而生,并在近些年获得突飞猛迚的发展,为药物开发提供了新路径,成为极具潜力的新药开发技术之一。
泛素-蛋白酶体系统(Ubiquitin-proteasome System,UPS)是细胞内80%以上蛋白质降解的主要途径,在DNA修复、信号传导、转录翻译、免疫应答等多种细胞活动中起重要作用。UPS由泛素(ubiquitin,Ub)、泛素活化酶(ubiquitin activating enzyme,E1)、泛素缀合酶(ubiquitin-conjugating enzyme,E2)、泛素-蛋白质连接酶(ubiquitin-protein ligase,E3)、蛋白酶体及其底物蛋白等构成。越来越多的文献采用蛋白质组学和泛素化蛋白质组学的方法进行TPD药物靶点和作用机制的评估。在实验设计时,一般考虑药物处理的浓度梯度和时间梯度,本期将介绍TPD药物处理的时间梯度进行蛋白质组学和泛素化蛋白质组学的实际应用案例。
时间梯度蛋白质组学评估
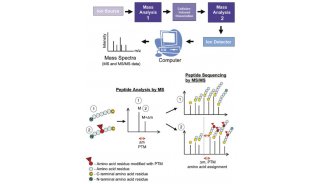
近几年来,蛋白质组学技术和研究思路都有了令人鼓舞的进展蛋白质组学是研究疾病发生过程中蛋白质变化、生化代谢途径改变和鉴定的有力工具。在药物开发中的作用主要表现在疾病检测、药物靶点发现、药物代谢转化、药物不良反应研究等方面。通过比较正常体与病变体、给药前后蛋白质谱的变化,蛋白质组学技术可提供疾病发生、药物作用和药物不良反应的分子机制信息(图1)。基于化学标记的原理实现对多个样本中蛋白质的同时定量分析,通过比较不同生理状态、疾病状态或药物处理后的样本,可以揭示蛋白质在不同生物过程中的调控机制,寻找潜在的生物标志物或靶点。

图1. 蛋白质组学实验流程
基于质谱的蛋白质组学方法,Huang等人开发了一种基于二氨基嘧啶支架(TL12-186)的多激酶降解剂。为了确定TL12-186的可降解靶标,以DMSO为对照组,给予不同的给药时间梯度0min,1hr,2hr和6hr,共4个时间点(图2A),采用了TMT定量蛋白质组学方法,以无偏的方式测量蛋白质丰度的变化,结果显示随着时间的增加,多种激酶(PTK2、FER、 AURKA等)被下调(图2B)。并且大多数蛋白在6小时后呈现显著下调的趋势,降解的比例在75%-87.5%(图2C)。
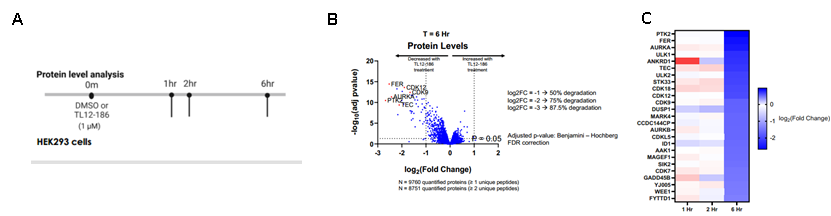
图2. TL12-186处理的定量蛋白质组学分析。(A) 实验设计,(B) 处理6h定量蛋白质组火山图,(C) 靶点蛋白在1hr,2hr,6hr比值的热图
时间梯度泛素化组评估
为了确定蛋白质是否被靶向降解,通常需要确定蛋白质是否已被泛素化。泛素化分析有助于深入了解蛋白质降解物的作用机制,所谓泛素化,指的是这样一个蛋白质修饰过程:在一系列酶的参与下,泛素分子选出特定的靶蛋白,给它们“贴上标签”。随后,这些被修饰的蛋白质会被送入蛋白酶体,在这台“蛋白质粉碎机”中被切割成碎片,实现蛋白质的降解。目前,基于非标记定量DIA和标记定量TMT的技术,均可以实现深度覆盖的泛素化蛋白质组分析,在细胞系中定量上万个泛素化位点(图3)。

图3. 泛素化组学实验流程
随后该课题组将TL12-186的多激酶降解剂处理的样品进行泛素化组学的评估,在经过MG-132(一种蛋白酶体抑制剂)预处理后(-30min),再收集不同时间梯度的的样本进行全细胞的泛素化组分析(0min、15min、30min、1hr、2hr、3hr、4hr、5hr、6hr),共10个时间点(图3A),使用DIA-MS进行泛素组分析,可以在单次MS分析中确定超过100,000个泛素化位点和超过85,000个K-GG肽段,实现了超深度的泛素化蛋白质组分析。结果显示,与全蛋白质组的结果相对应,多种激酶蛋白(PTK2、FER、 AURKA等)被下调,而其泛素化的水平在上升(图4B),并且基于时间梯度的泛素化组评估显示,多个位点在15分钟内发生了超过10倍的差异变化(图4C)。除了鉴定到多种已知靶激酶蛋白的泛素化之外,在AURKA蛋白上发现新泛素化位点,在加药6h后,AURKA蛋白被显著下调(图4D),而其泛素化的水平也随着时间梯度在不断的上升(图4E),同时一些新的泛素化位点被鉴定到,提示可能存在新的降解机制(图4F)。
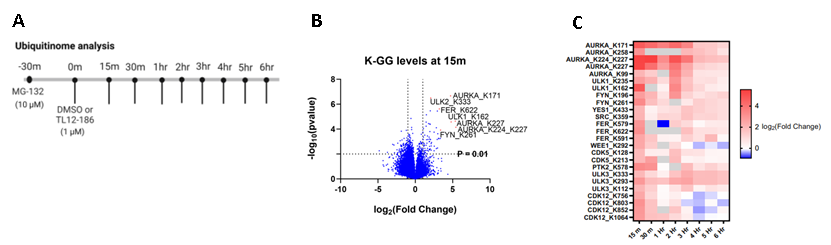

图4. TL12-186处理的定量泛素化蛋白质组分析。(A) 实验设计,(B) 处理15min定量泛素化位点的火山图,(C) 药物靶点的泛素化位点不同时间点比值热图,(D) AURKA不同时间点蛋白比值,(E) AURKA的泛素化位点动力学,(F) AURKA新发现的泛素化位点
结论:
· 通过深度覆盖的蛋白质组学与泛素化组学分析,在蛋白质组学层面上可通过蛋白丰度的差异变化寻找潜在的生物标志物或靶点,而泛素化组学的协同验证,有助于阐明降解的特异性的差异。
· 基于时间梯度的数据分析,同一蛋白上不同位点的泛素化谱不同,提示在靶蛋白降解过程中,少数位点的重要性。
· 泛素化动力学和降解动力学,可扩展新的蛋白质降解方法。
我们的解决方案
全蛋白质组分析
· 快速检索待测靶点的细胞系数据,300+不同类型人源细胞系蛋白质鉴定数据库,涵盖12,000种以上蛋白质,帮助您快速锁定候选靶点,缩短实验时间,节约成本;
· 深度覆盖的全蛋白质组学数据,实现9000+蛋白质覆盖;
· 标准化数据分析流程,整合常用数据质控和差异表达分析模块,内置TPD靶点数据库,靶点降解情况一目了然;
点击查看详细介绍
Untangled,公众号:氨探生物TPD业务介绍 | 基于全蛋白质组的靶点识别与先导化合物优化服务
泛素化蛋白质组分析
· 利用自主研制的高特异性K-ɛ-GG抗体,增加了泛素化肽的富集效率及特异性;
· 高灵敏度的DIA深度检测方法;
· 深度覆盖的泛素化蛋白质组学方法;
· 在未经MG132处理的单个人细胞系样品中检测到20,000个不同的泛素化位点;
· 样品量起始量低至500ug;
点击查看详细介绍 Untangled,公众号:氨探生物TPD业务介绍 | 蛋白泛素化与泛素化组确定蛋白降解类药物作用机制(MOA)
若您对我们的产品感兴趣,或有宝贵的意见和建议,请联系我们:info@untangledbio.com。
1. Time-resolved deep ubiquitinome profiling for protein degraders. ASMS2023, TOB pm 03:30.
2. A Chemoproteomic Approach to Query the Degradable Kinome Using a Multi-kinase Degrader. Cell Chem Biol. 2018 Jan 18;25(1):88-99.e6.
3. Modeling the CRL4A ligase complex to predict target protein ubiquitination induced by cereblon-recruiting PROTACs. J Biol Chem. 2022 Apr;298(4):101653.
解构健康奥秘、探寻生命答案,氨探生物以一流的分子表型组平台和成熟的临床转化应用体系,为优秀的研究团队进行技术和数据赋能,致力于实现分子表型水平的精准诊疗。