MIT发现的这款Biomarker,作用“一箭双雕”
大约在10年前,生物标志物的发展还未起步。但现在,生物标志物已经开始了临床前期的研究,从动物模型开始,再到临床研发阶段。随着医学发展更加个性化、更依赖于分子水平的研究,基因组和蛋白质组学研究已经证明,药物研发和生物标志物(Biomarker)发展之间的重合也呈必然的增长趋势 。
癌细胞如何迈出扩散的第一步?
生物标志物Mena蛋白来帮忙
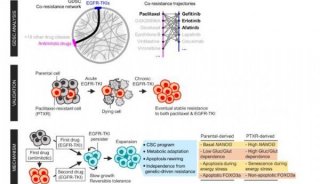
近日,麻省理工学院(MIT)的生物学家发现:先前已被证明可以帮助癌细胞通过身体扩散的一种做“Mena”蛋白的生物标志物,可以揭示侵袭型乳腺癌患者是否受益于紫杉醇(该种癌症最常用的一种药物)。
据悉,该研究结果可以为医生提供三阴性乳腺癌选择药物的新方法。一般情况下,三阴性乳腺癌缺少3种常见的乳腺标志物——雌激素受体,孕激素受体和 Her2 蛋白。
而此次,研究人员发现:将紫杉醇与另一种药物结合,可以干扰“Mena”蛋白水平的影响,比单独使用紫杉醇能够杀死更多的细胞。
文章的作者之一,身兼MIT生物教授和科赫综合癌症研究所(Koch Institute for Integrative Cancer Research)成员Frank Gertler表示,靶向紫杉醇通路对细胞表达“Mena”蛋白具有易感性。该研究表明在治疗过程中监测“Mena”蛋白的水平是很有必要的,如果“Mena”蛋白升高,意味着切换到另一种治疗类型或是有用的。
细胞如何生存?
众所周知,“Mena”蛋白与细胞骨架相互作用的方式可以帮助细胞迁移。许多癌症患者一种叫做Mena入侵或者MenaINV的蛋白质,该蛋白帮助癌细胞从原来的位置流动到另一个位置,即“转移”。一般拥有较高水平的入侵蛋白的乳腺癌患者,往往拥有更多的转移和更低的生存率。
30%到70%的三阴性乳腺癌患者对化疗反应良好,但疾病复发一般出现在6到10个月。研究人员好奇,“Mena”蛋白是否也可能在癌症细胞抵抗化疗中发挥作用?
另一位参与研究的人员Madeleine Oudin表示,目前已经知道有众多好药可以杀死大量的癌症,但有些患者并不对药物产生响应,有些即使能做出响应但也只能维持较短的时间。
于是,他们测试了几种不同化疗药物对三阴性乳腺癌细胞“Mena”蛋白水平的影响,并发现拥有“Mena”蛋白水平最高的是紫杉醇治疗。然而,其他两个常用的化疗药(阿霉素和顺铂)对“Mena”蛋白水平的影响未被检测到。
紫杉醇,常被用于进展期卵巢癌的一线和后继治疗,它通过干扰组成细胞骨架的微管(Microtubule)里的管状蛋白,从而帮助细胞进行分裂。微管既可以是动态的,也可以是稳定的,而动态的版本是细胞分裂所必需的。紫杉醇能够稳定微管,干扰细胞分裂和杀伤细胞。
在对转移性三阴性肿瘤小鼠注射紫杉醇后,研究人员发现,最高水平“Mena”蛋白的肿瘤表现出最坏的反应:该药物没有降低原发肿瘤或转移。无论是侵入性肿瘤还是原发性肿瘤,“Mena”蛋白都具有相似的影响。
研究人员还表明,高“Mena”蛋白水平的癌细胞比低“Mena”蛋白水平的癌细胞拥有更多的动态微管,动态微管越多,细胞分裂更容易并能对紫杉醇产生抗性。
面对抗性
以往的研究表明,紫杉醇治疗也影响细胞通路——ERK信号通路,后者是过度活跃的癌细胞促使细胞增殖。紫杉醇治疗过程中打开了ERK信号通路,使癌细胞在这种治疗下生存,但如果同时抑制ERK信号,治疗会更成功。
在肿瘤分子治疗研究中,MIT的研究小组试图对乳腺癌细胞中高“Mena”蛋白水平的患者联合使用紫杉醇与ERK通路抑制剂高水平的曼娜,发现它单独使用比紫杉醇能更有效地杀死细胞。目前,在乳腺癌患者身上测试这种药物组合疗法的临床试验已经开展。
研究结果还可以帮助医生根据患者体内的“Mena”蛋白水平选择治疗,即提供更多的治疗选择信息,并找出不太有效的治疗与化疗患者。
哈佛医学院癌症生物学和外科教授Bruce Zetter表示,三阴性乳腺癌患者没有很多的治疗选择,如果这项工作可以帮助确定最有可能响应紫杉醇的患者,并鼓励更多地患者使用MEK抑制剂和紫杉醇的组合,或能极大地提高生存期。
研究人员还希望发现更多的“Mena”蛋白如何影响微管的机制,并希望能够揭示其他类型癌症中“Mena”蛋白的作用机制。