访美国病理学家协会国际高级医学顾问

为期近一个月的中国之行,Jay还特意给自己起了个中文名字“沈博杰”,他觉得这样会让人觉得更加亲切。
担任美国病理学家协会(CAP)国际高级医学顾问一职的Jay虽然只会说简单的中文,但丝毫不影响他与国内检验科人员进行交流。
CAP认证作为美国一个非营利的临床实验室认可机构成立于1947年,自1962年起在美国普遍采用执行,1994年起被世界各国公认为最适合医疗检验室使用的国际级实验室标准。通常认为经过CAP认可后的实验室检测能力已达到世界水准,如无其他官方解释,FDA承认经CAP认可的实验室所提供的质量报告。
“中国的CRO市场是世界上增长最为迅速的国家之一,推动CAP认证在中国的发展,让中国的每个实验室的检测质量与水平都能达到国际顶尖水准。最重要的是,CAP认证的体系可减少患者在不同医疗实验室的重复性检测。”Jay对《科学时报》记者说。
“每份检查清单的相关问题都非常具体。每年我们都要对CAP认证的审核目录进行更新,以反映最新的科技和操作实践水平。”Jay觉得CAP认证具备与时俱进的特征。
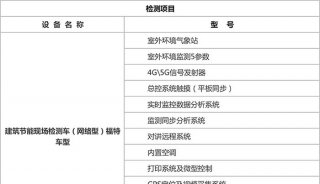
据了解,美国约有600多位科学家专门负责对CAP认证的制定、调整、申请等方面的工作。Jay打开随身携带的笔记本电脑,向记者展示最新版的CAP认证文件,里面包含了对实验室人员、安全、计算机服务、测试方法、设施等17个方面的审核目录。
“2011版的CAP认证文件马上就要公布了。” Jay说,虽然并不是每年都要对CAP认证文件进行调整修订,但是每次调整修订都会清楚地标明与上一版相比调整或删除的地方,还会告诉评审员如何去评审新增的项目。
谈到CAP与ISO的关系时,Jay用“互动、互补”来形容。他觉得,ISO更注重实验室文件的归档,“是不是都记录下来了”。而CAP则更加关注文件是否被执行,“文件是不是已经实施了”。“其实,CAP也关注文件的归档,但是它要求必须有相应的证据证明文件所记录的事情必须保质保量地完成。”
此外,Jay认为CAP比ISO在审核目录上更加的细化, 为实验室提供方法明确的指导准则,“它们两个都有各自的细节与条款,而CAP会比ISO有更多的目录,比如,今年CAP会增加关于分子病理学的审核项目。”
“当然,CAP与ISO都是实验室的认证标准,不能笼统地说哪个更好,每个实验室要根据自己的实际情况来选择适合的认证标准。但是两者并不冲突、排斥,实验室可以同时选择两种认证标准。” Jay说,世界上约有45个国家和地区的超过7000家实验室通过了CAP认证,其中,15家实验室来自中国。
Jay认为,实验室进行CAP认证,标准是认可决策的基础。他向记者介绍了通过CAP认证的相应标准的4个方面:标准Ⅰ与实验室人员资质等有关;标准Ⅱ是有关实验室的物理设施和生物安全;标准Ⅲ主要围绕着质量展开,涉及到质量控制、能力验证(PT)等方面;标准Ⅳ则是从检查入手,包括外部组织的现场检查和内部的自我检查。
如果仔细浏览CAP认证文件,你会发现它所要求的实验室认可检查清单,主要以3000多个问题的形式表示。“除了有对整个实验室和各个专业的基本要求,还有对不同专业的特殊要求。当然,也存在着不同专业,有时候认可检查清单的内容可能相同。”
那么,实验室通过CAP认证之后,到底能够带来什么益处呢?
“首先能够确保病人的安全性,因为所有经过CAP认证的实验室都参与到全球的室间比对,所获得的数据都是国际的标准。”Jay说。
此外,CAP的服务客户,可以拥有先进的质量管理工具,享受质量追踪的服务;还可以下载CAP官方网站上很多产品,以及参加一些培训项目。
“经过CAP认证的实验室数据是被美国FDA所认可的。” Jay坦言,这也吸引了很多渴望产品进入欧美市场的医药企业的目光。
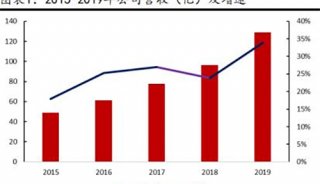
资料显示,目前CRO公司承担了全球将近1/3的新药开发组织工作,CRO服务的全球市场以每年20%~25%的速度增加。2010年,全球CRO市场达到约360亿美元的规模,年增长率达16.3%。
而当前的中国正成为越来越多的跨国制药公司“安营扎寨”的目标,自然而然也推动了CRO服务的升温,伴随而来的就是对CAP认证的需求。这也正是促使Jay此次中国之行的原因。
在走访中国几家医院之后,Jay觉得一些实验室的设施管理很不错,而对于试验流程,他因没有深入了解,不能给予评判。
让Jay体会最深的还是语言上的障碍。“尽快地把CAP认证文件翻译成中文,培育本土的CAP评审员势在必行。”此外,由于CAP认证需要全球的室间质评,涉及到海关报关的相关问题,寻找到一家优秀的物流合作伙伴也是Jay一直思索的事情。