阿尔茨海默症研究进展(药物篇,中)
在研项目:中枢神经系统疾病(阿尔茨海默症和帕金森病)药物研发包括靶点化药以及上市化学药和中药的二次开发。
续上文。
2.治疗
治疗药物方面,早发现早治疗AD目前被大多数人接受为最有可能有效帮助的AD病人的策略。随着Aβ PET显像示踪剂美国药监局批准上市和Tau PET显像示踪剂的批准临床研究,大药企开始使用这两个生物标志物筛选病人入组或者作为疗效测试指标。
2.1 胆碱能系统
胆碱酯酶是AD药物研发最为成功的靶点,美国药监局目前为止只批准了5个AD新药(NCE),其中4个是胆碱酯酶抑制剂(表一)。这个领域目前在研新产品不多,可以查到进行中临床试验只有2个;一个1期临床药物以及一个石衫碱甲的4期临床试验。
2.1.1 VU0467319
范德堡大学研发的毒蕈碱型乙酰胆碱受体(mAchR1)正向别构调节剂(positive allosteric modulator),即PAM激动剂,预计今年上半年开始一期临床(2)。这个靶点一度很受重视,但因传统激动剂对外周系统的毒副作用和Aβ假说的重视影响了这个靶点的进程。
2.1.2 石衫碱甲
上海市精神卫生中心2016年11月开始做的石衫碱甲的4期临床试验,在300个MCI期AD病人中做为期52周的MCI到AD转化率的实验,预计2018年12月完成(2017年12月完成数据采集)。
2.2 淀粉样蛋白病变
这个机制目前在研的药物最多,也出现了许多失败的情况。在研药物包括小分子,抗体和疫苗。目前,2/3和3期临床试验的药物预计2019年开始会有结果,这个假说是否可以影响AD病情在2020-2023年之间估计可以得出定论。如果安全并可以降低Aβ斑块(而且伴有一定认知效果),这方面的药物将可能被FDA批准,跟降胆固醇的药预防心脏病一样,在Aβ异常增高的人群中使用。
2.2.1 小分子药物
针对淀粉样蛋白病变假说的小分子靶点主要是Aβ预蛋白APP代谢通道的三个内泌酶(secretase):α, β和γ内泌酶。其中研究最多的是β内泌酶,BACE。另外有许多靶点可以间接的影响淀粉样蛋白病变。
α-内泌酶是个很好的靶点,需要激活剂,虽然目前酶激活剂本身的研发还没有太好办法,但可以通过信号通路激活。比如上面提到的毒蕈碱型乙酰胆碱受体激动剂的可以 通过调节蛋白K激酶(PKC)活性来增加α-内泌酶活性。另外从苔鲜动物草苔虫(Bugula neritina)中提取出的一种大环内酯类物质Bryostatin 1(苔藓虫素)也被发现有PKC调节作用,并对1例严重家族性AD病人有效果,目前Neurotrope正在进行2期临床试验。同时Aphios公司也在进行Bryostatin衍生物的研究,APH-0703在巴哈马做了一例AD病人,,公司网站称结果“显著、鼓舞人心”,目前该公司正在研发比APH-0703活性更好的在预临床阶段的衍生物APH-104。
γ-内泌酶一度有很多公司在研发,但底物非特异抑制剂临床证明抑制γ-内泌酶不但不能帮助AD病人反而可以加重病情(5),公认的原因是γ-内泌酶有好多APP以外的底物如Wnt, 抑制这些底物的活性导致毒副作用。目前选择性γ-内泌酶调节剂的研究在进行中,辉瑞的PF-06648671已经进入临床期。
2.2.1.1 BACE抑制剂
目前在研的2-3期临床的BACE抑制剂共有6个药物,上面提到的杨森的JNJ-54861911和诺华/安进的CNP520在做预防性试验(1.5,1.6)。其他4个见表二,其中两个获得美国药监局的绿色通道身份(Fast Track designation)。这个靶点是否有效2019年底2020年初可以知道初步结果。不过默沙东刚宣布的Verubecestat的3期临床失败(表二,红颜色),为这个靶点带来严重危机,但礼来/阿斯利康今年3月开始1400病人的现在进行实验的延续(表二,绿颜色),也表明了这两家大药企对BACE靶点的信心!
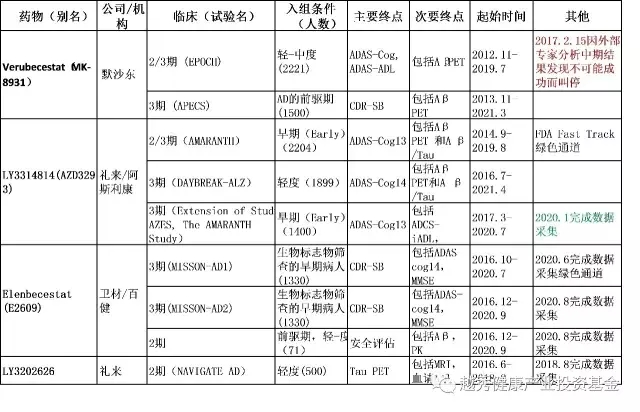
表二:2-3期在研BACE抑制剂(数据来源:clinicaltrials.gov; yahoo.com搜索和Eisai.com)
2.2.1.2 其他影响Aβ的在研小分子药物
文献中的可以通过不同途径影响或清除Aβ的小分子有很多。除了上面提到的辉瑞的γ-内泌酶调节剂,下面是4个不同机制的在研的其他影响Aβ的小分子药物,最早的2018年可以知道结果。
2.2.1.2.1 Azeliragon (TTP488, PF-04494700)
RAGE受体抑制剂,抗氧化并有清除Aβ作用。vTv 药物公司2013年获得FDA绿色通道,2015年4月开始在800个轻度AD病人中做一个叫STEADFAST的3期临床,预计2019年1月完成。
2.2.1.2.2 ALZT-OP1(色甘酸鼻喷剂Cromolyn和布洛芬Ibuprofen)
老药新用联合新用,布洛芬抗炎症,色甘酸有抗Aβ聚集和降低Aβ作用。 AZTherapies公司2015年9月开始在600个早期病人中做一个叫COGNITE的3期临床,预计2018年3月完成。
2.2.1.2.3 CT1812
Sigma-2/PGRMC1受体结合剂,可以抑制Aβ与Sigma-2/PGRMC1受体结合。CogRx公司2015年9月开始在114个健康志愿者进行1期临床,2016年5月完成。2016年9月1/2期临床开始在16个早中期AD病人在澳大利亚的几个中心进行。
2.2.1.2.4 PF-05251749
没有透露具体机制的第二个1期检测脑脊液Aβ。辉瑞2016年11月公司产品链列举此化合物为AD在研产品,已完成1个一期临床。并在2016年6月在比利时54个健康和健康老人中开始第二个一期临床。
2.2.2 抗体药物
针对Aβ的抗体是这个领域做的最多的,也是失败最多的。在五个临床数据最多的Aβ抗体中,辉瑞的Ponezumab和辉瑞/杨森的Bapineuzumab已经被放弃,但罗氏/基因泰克的Crenezumab (MABT510A)(1.3,表三),罗氏/基因泰克/中外制药的Gantenerumab (RG1450)(1.1,表三)和礼来的Solanezumab(1.1,1.4)都获得了新生。虽然礼来的新总裁刚刚宣布终止了刚开始的SolanezumabExpediton PRO3期临床试验(6, 表三红颜色)但罗氏刚宣布开展一个新的Crenezumab3期临床试验(表三,绿颜色)。目前业内最看好的是百健的Aducanumab (BIIB 037,表三)。尽管2016年公布的Aducanumab的1期临床数据揭示能够有效减缓早期AD病人的认知功能减退,但如何控制副作用和进行中的2个3期临床是否能重复这个样本很小但到目前为止Aβ领域最好的结果只有时间可以回答。希望2020年可以有好消息。
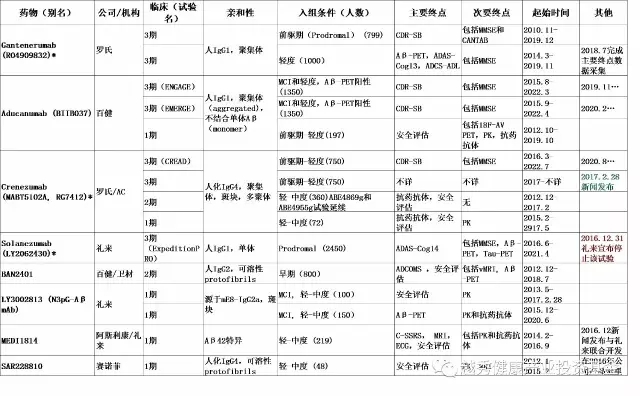
表三:在研Aβ抗体药物
2.2.3 疫苗
疫苗是个非常有前景的方向,但包括脑膜脑炎在内的毒副作用是个亟待解决的难点。目前Aβ领域至少有6个临床期疫苗。
2.2.3.1
诺华的CAD106疫苗在做2/3期预防临床试验(1.6)走在最前沿。
2.2.3.2
AC Immune公司的ACI-24疫苗在做两个临床试验:2009年开始在欧洲不超过198个AD病人中进行 1/2期临床试验,何时完成不详和2016年3月开始在美国24个唐氏综合症病人中进行1期临床,预计2019年8月完成。
2.2.3.3
Araclon的ABvac 40和ABvac42疫苗没有在世界卫生组织或Clinicaltrials.gov上登录,但公司网站显示已在2015年分别进入1期和2期临床。
2.2.3.4
AFFiRiS公司2010年9月到2013年2月在欧洲做了332个AD病人的AFFITOPE AD02疫苗2期临床试验,结果发现疫苗没有效果。但有意思的是辅助免疫配方(后来被该公司命名为AD04)对照组(~50病人)有约一半病人的病情得到缓解。AFFiRiS公司还在思考下一步如何进行。
2.4.5
United神经科学公司的UB-311疫苗2015年10月开始在台湾的45个轻度病人中进行2期临床试验,预计2017年12月完成。
2.4.6
灵北2015年3月开始在35个轻度病人中开始Lu AF20513疫苗的1期临床试验,预计2017年5月完成。
2.3 Tau蛋白病变
针对Tau蛋白病变的在研药物不多,可以查到的临床研发药物有6个:2个小分子,2个抗体和2个疫苗。
2.3.1小分子药物
2.3.1.1 LMTM,亚甲蓝(Methylene blue)衍生物
前面提到TauRx公司2016年宣布LMTM 的第二个3期临床失败,但TauRX声称LMTM在完成的两个3期临床试验中LMTM单独使用组跟LMTM与Aricept联合用药组对照有明显疗效,虽然在测试过的剂量中没有量效关系。TauRx公司的这个分析方式遭到很多非议因为单独用药组没有相应安慰剂对照组,但公司准备继续LMTM的研发,正在筹备LMTM单独用药临床试验。
2.3.1.2 TPI 287
Cortice公司的可以影响Tau病变的的抗癌药。加州大学旧金山分校2013年11月开始在33个轻到中度病人中进行1期临床,预计2017年11月完成。
2.3.2 抗体药物
2.3.2.1 ABBV-8E12(C2N 8E12)
AbbVie公司2015年3月从C2N公司转让而来的Tau抗体,2016年10月开始在400个早期AD病人中进行2期临床,预计2020年4月完成。公司声称可以尽快在不同的适当时机知道试验结果,最大程度推进研发速度。
2.3.2.2 RO 7105705(RG 6100)
基因泰克和AC Immune公司联合开发的Tau抗体。基因泰克2016年6月开始在71个健康人和轻度到中度AD病人中进行1期临床试验,预计2017年5月完成。
2.3.3疫苗
2.3.3.1
AADvac-1是Axon 神经科学公司针对Tau氨基酸294到305的疫苗,2016年3月开始在185个轻度AD病人中进行2期临床试验,预计2019年2月完成。
2.3.3.2
ACI-35是AC Immune公司研发的针对磷酸化Tau蛋白的疫苗,2013年12月开始在24个轻度到中度的AD病人中开始1期临床试验, 2015年转让给强森公司,目前进展不详。