治疗阿尔茨海默症的天然疫苗
Laval大学、CHU de Québec和葛兰素史克GSK的研究人员开发了一个非常实用的方法,能够有效刺激阿尔茨海默症患者大脑中的天然防御机制。这项重要突破于一月十五日提前发表在美国国家科学院院刊PNAS杂志的网络版上,该研究不仅有助于治疗阿尔茨海默症,还为人们提供了预防阿尔茨海默症的潜在疫苗。
阿尔茨海默症是世界上最常见的痴呆病因,人们目前还无法根治这一疾病。阿尔茨海默症的主要特征之一,是患者大脑产生毒性分子β淀粉样蛋白。神经系统的防御者小胶质细胞(Microglial cell)无法清除这一物质,导致β淀粉样蛋白沉积形成老年斑senile plaque,继而引发其他相关病理学症状。因此,能够刺激免疫系统有效清除β淀粉样蛋白的化合物就具有极大的治疗潜力。
Laval大学Serge Rivest教授领导的研究团队就发现了这样一个刺激大脑免疫细胞活性的分子,MPL(单磷酰脂A)。单磷酰脂A是一个LPS衍生的Toll样受体4激活剂,有独特的免疫调节作用,已经被GSK作为疫苗佐剂广泛使用了多年,其安全性久经考验。
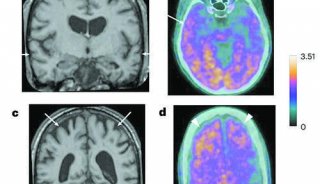
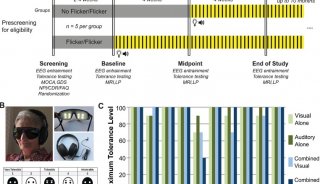
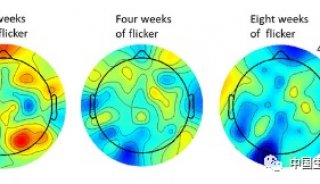
研究人员在十二周内给具有阿尔茨海默症症状的小鼠进行每周MPL注射,成功清除了80%的老年斑。他们通过实验来衡量小鼠学习新任务的能力,发现在治疗过程中小鼠的认知功能得到了显著提升。
研究人员认为MPL具有两种应用潜力。可以用这种药物对阿尔茨海默症患者进行肌肉注射,以延缓疾病进程。也可以将其整合到疫苗中去,刺激机体产生针对β淀粉样蛋白的抗体。“已经患有阿尔茨海默症的患者可以用这种疫苗来刺激自身的天然免疫,” Serge Rivest说。“而那些具有阿尔茨海默症风险因子的人也可以将这种疫苗作为预防措施。”
这项研究显示,系统性的重复注射MPL能够显著减少小鼠大脑中的β淀粉样蛋白,大大增强小鼠的认知功能。MPL在触发温和炎症反应的同时,能诱导小神经胶质细胞的吞噬作用。
“当我们十年前开始研究阿尔茨海默症时,我们的目标是为患者开发更好的治疗手段,” Rivest教授说。“这项发现让我相信,我们已经离这一目标很近了。”
Toll-like receptor 4 stimulation with the detoxified ligand monophosphoryl lipid A improves Alzheimer’s disease-related pathology
Jean-Philippe Michauda, Maxime Halléb, Antoine Lamprona, Peter Thériaulta, Paul Préfontainea, Mohammed Filalia, Pascale Tribout-Joverb, Anne-Marie Lanteigneb, Rachel Jodoinb, Christopher Cluffc, Vincent Brichardd, Rémi Palmantierd, Anthony Pilorgetb, Daniel Larocqueb,1, and Serge Rivesta,1
Alzheimer’s disease (AD) is the most common cause of dementia worldwide. The pathogenesis of this neurodegenerative disease, currently without curative treatment, is associated with the accumulation of amyloid β (Aβ) in brain parenchyma and cerebral vasculature. AD patients are unable to clear this toxic peptide, leading to Aβ accumulation in their brains and, presumably, the pathology associated with this devastating disease. Compounds that stimulate the immune system to clear Aβ may therefore have great therapeutic potential in AD patients. Monophosphoryl lipid A (MPL) is an LPS-derived Toll-like receptor 4 agonist that exhibits unique immunomodulatory properties at doses that are nonpyrogenic. We show here that repeated systemic injections of MPL, but not LPS, significantly improved AD-related pathology in APPswe/PS1 mice. MPL treatment led to a significant reduction in Aβ load in the brain of these mice, as well as enhanced cognitive function. MPL induced a potent phagocytic response by microglia while triggering a moderate inflammatory reaction. Our data suggest that the Toll-like receptor 4 agonist MPL may be a treatment for AD.