肿瘤免疫药物相继上市,是否已经走向标准化?
肿瘤免疫治疗的发展近几年来如火如荼,针对包括 T 细胞及其相关受体的机制研究与药物研发层出不穷,各种相关药物与疗法接连上市。其中,程序性细胞死亡蛋白-1(programmed death-1,PD-1)及其配体(PD-L1)抑制剂是免疫检查点单抗药物,其应答之广度、深度、和持久性均十分罕见,是近年来肿瘤免疫疗法研究的热点。
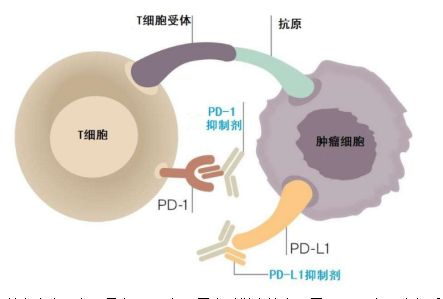
说起 PD1和PD-L1,其实由来已久。早在1992年,日本科学家就发现了PD-1蛋白,十年后,PD-L1被发现在肿瘤微环境中,特别是肿瘤细胞上过度产生,且此分子的过度表达选择性地抑制了肿瘤微环境中淋巴细胞的免疫反应。PD-1和PD-L1的关系类似于结合子和受体,所调控的免疫调节分子信号通路可压制免疫细胞对肿瘤细胞的进攻。肿瘤细胞利用 PD-L1 结合到细胞表面受体PD-1上,这一结合负调节免疫细胞活性,从而阻断免疫细胞对肿瘤细胞的攻击,因此肿瘤得以通过这个通路将自己隐藏。[1]
此机制发现后,关于利用抗体阻断PD1和PD-L1,从而让T细胞实现正常的肿瘤消灭功能的研究便开始兴起。PD-1/PD-L1信号通路被发现与免疫逃逸机制密切相关,阻断该通路可增强机体内源性抗肿瘤免疫效应。近年来,越来越多的研究证明,阻断此信号通路对癌症的治疗有效。继血液肿瘤之后,更多的实体瘤领域也开启了肿瘤免疫治疗的研究,例如有研究证实,针对阻断PD-1/PD-L1 通路免疫检查点的治疗在肺癌中取得了明显效果[2],且PD-1/PD-L1抑制剂在结直肠癌等消化道肿瘤领域也颇有潜力[3]。
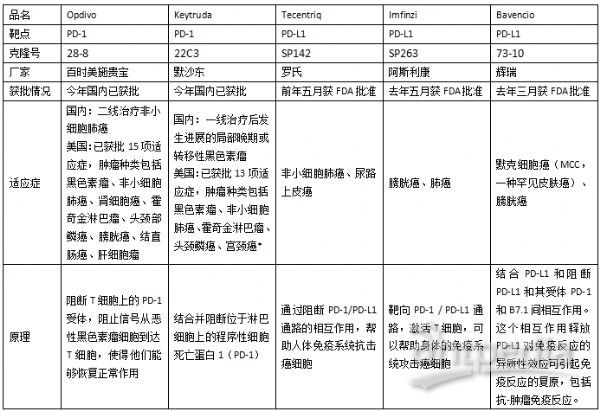
目前,FDA批准了2款PD-1抑制剂(Opdivo和Keytruda,两药目前在国内刚刚获批)和3款PD-L1抑制剂(Tecentriq、Imfinzi、Bavencio)上市。同时,也分别批准了相应的伴随/补充诊断抗体:28-8、22C3、SP142、SP263、73-10(克隆号)这4个PD-L1单抗,用于PD-L1表达水平的IHC检测。就在6月15日,BMS的PD-1单抗药物 (Opdivo, Nivolumab) 的中国上市申请正式获得CFDA批准,用于二线治疗非小细胞肺癌。
首先在这个领域展开厮杀的无疑是医药行业的各大巨头。已批准的五款抑制剂分别属于百时美施贵宝、默沙东、罗氏、阿斯利康和辉瑞。而Abcam在补充诊断抗体领域占据半壁江山,获批的伴随/补充诊断抗体中有一半 (28-8、SP142、73-10) 为其上市产品。据悉,Abcam将推出更多的合作开发的PD-L1抗体。
从以上现状不难发现,目前获批的药物大多有着专用的补充诊断抗体与其配合。而对于患者而言,只有在应用这些抗体进行IHC检测且检出表达量高于一定值时,才适用相应的药物。这样的“一药一检(One drug, one assay)”情况意味着患者面临重复的尝试。为了寻找应对之策,不久前,FDA牵头四家企业和两家学术机构发起了“蓝印计划” (Blueprint Initiative),以期在未来能让针对PD-L1 的IHC 检测更加规范化。
就在今年,科学家们宣告了蓝印计划PD-L1免疫组织化学(IHC)相似可比性的II期临床测试结果,他们通过5种已经过验证的PD-L1检测方法(涵盖22C3、28-8、SP142、SP263和73-10),并对 81 位临床肺癌患者的不同组织学样本进行检测,由一组国际病理学家来评判。这项测试旨在验证 I 期测试的结果,评估PD-L1评分的可靠性,进一步得出了22C3、28-8和SP263检测可互换性的分析证据,并发现SP142检测肿瘤细胞中肿瘤占比分数的敏感性较低,而73-10与其他检测相比显示出了较高的敏感性,玻片和数字图像评分也高度一致(皮尔逊相关>0.96)[4]。 随着相似性研究的进一步深入,这些结果无疑能够让帮助医生为患者选择治疗方案,从而改善治疗效果。
历年发布的癌症数据报告显示,中国的癌症发病率逐年攀升,2017年发布的2013年统计数据(癌症数据一般滞后三年)就指出,中国每天约有一万人确诊为癌症,预期寿命85岁时,累计患癌风险高达36%。这意味着在中国,癌症治疗有着巨大的需求,和巨大的市场。有人预计,我国未来抗肿瘤药的市场将达 3000 亿。未来,肿瘤免疫疗法将成为肿瘤治疗领域继手术、放化疗和靶向治疗的另一项基石性治疗方法,而 PD-1/L1 抗体药物作为肿瘤免疫疗法中最具有代表性意义并且使用最为广泛的基石性治疗品种,必将在整个抗肿瘤用药市场规模中占据一席之地。希望在不久的将来,患者能够省去重复检测的麻烦,只需通过一种检测方法即可了解自己适合何种免疫治疗。而随着肿瘤免疫治疗应用的不断普遍化,PD-1/PD-L1抑制剂的通用诊断试剂一旦面世获得证实,也必将拥有极其广阔的市场。蓝印计划的诞生只是推动肿瘤免疫治疗的其中一步。且目前虽然部分诊断方法表达出了相似性,却还远远达不到“通用”的程度,即经过一种检测即可了解是否适用多种免疫治疗药物。看来,尽管PD-1和PD-L1在肿瘤免疫治疗的标志物中“跑得”已经相对较快,但仍有许多像诊断试剂不够“通用”、部分诊断试剂相对而言灵敏度较低(如SP142)等不足之处。虽然今年PD-1抑制剂在国内的获批是一个很好的开端,不过要达到真正的广泛应用,从诊断方法到新药开发,国内还有很长的路要走。
参考文献:
[1] 程远,黎军和,PD-1/PD-L1抑制剂在肿瘤免疫治疗中的研究进展,《中国肿瘤临床》 , 2016 , 37 (21) :3301-3304
[2]林城,陈雄等,PD-1/PD-L1信号通路在非小细胞肺癌免疫逃逸及其治疗中的研究进展,《中国肺癌杂志》 , 2014 (10) :734-740
[3]马宝镇,高全立,抗PD-1及PD-L1在肿瘤治疗中的进展,《中国免疫学杂志》 , 2017 , 33 (5) :796-800
[4] ST Ming, KM Kerr et al, PD-L1 immunohistochemistry comparability study in real-life clinical samples: results of Blueprint phase 2 project, Journal of Thoracic Oncology , 2018
-
标准

-
标准

-
科技前沿

-
科技前沿

-
科技前沿
-
焦点事件
-
产品技术