蛋白质组学之逆袭,深度注释基因组
申请课题缺创新点?撰写论文没思路?急着毕业时间紧?别怕,对于吉凯,一切都是套路!更有甚者,对于宇宙终极难题:“屌丝如何逆袭白富美?”老司机黄博也有一套经典案例分享给大家。
从前,在生物学研究领域,有一个白富美叫基因组学(Genomics),她有一项强大的技能:DNA测序,凭借这项技能,她完成了对多种物种的基因组测序、定位了编码基因和确定编码基因的结构等基本的基因组注释任务。但她对基因组注释方法主要依赖于DNA及RNA序列信息。而为了更加精确地解读完成测序的基因组,单凭她一己之力是不够的,还需整合多种类型组学方法来进行基因组注释。
白富美人人想追,但这年头没啥创新点,怎能获得美人垂青?来吧,干了黄博这碗热气腾腾的鸡汤!
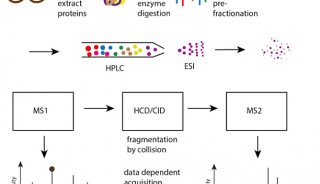
著名屌丝闪亮登场!名曰蛋白质组学(Proteomics),暗恋女神已多年,苦于自身并无一技之长,虽长期以来一直在女神面前狂刷存在感,但并未引起女神注意。故针对基因组学技能缺陷,潜心修炼,终获独门神技——串联质谱技术,弥补女神缺憾,终于逆袭成功。该技能实现了对蛋白质组的高覆盖,使得利用串联质谱数据进行基因组注释成为可能。串联质谱数据一方面可以对已注释的基因进行表达验证,另一方面还可以校正原注释基因,进而发现新基因,实现对基因组序列的重新注释。这样一来就很好的弥补了基因组学的不足,从而一举获得女神青睐,抱得美人归。成为生物学研究领域的史密斯夫妇,他们给自己的组合取了个很没创新性的名字——蛋白质基因组学(Proteogenomics),义指蛋白质组学与基因组学的交叉,这个交叉范围很广且可以多种方式定义,但通常是指基于串联质谱技术的蛋白质组学信息研究来提高对基因组的注释。
今年6月份,国际知名期刊Nature和Cell分别报导了这对夫妇利用自身强大技能对生物学研究领域邪恶组织成员乳腺癌和卵巢癌进行无情打击的英勇事迹。
其中在Nature题为”Proteogenomics connects somatic mutations to signalling in breast cancer”的报导中描述了对来自 “癌症基因组图集”(TCGA)、代表由mRNA定义的四个主要乳腺癌内在子类型的105个乳腺癌样本所做的基于iTRAQ联合串联质谱量化了超过12,000个蛋白质和33,000个磷酸化位点的蛋白质组学和磷酸化蛋白质组学分析。
针对一些乳腺癌亚型和携带常见突变如PIK3CA和TP53突变的肿瘤,分析结果揭示出了一些新的蛋白质标记物和信号通路。另外将一些基因中的拷贝数改变与蛋白质水平联系一起,从而鉴别出了10个新的候选调控因子。其中两个候选基因SKP1和 CETN3可能与癌基因EGFR有关联。EGFR是一种特别具有侵袭性的乳腺癌亚型——“基底细胞样”肿瘤的标志物。除此之外,通过孤立点分析了一些激酶的磷酸化状态,凸显出了乳腺癌样本中一些异常活化的激酶,如HER2, CDK12, PAK1, PTK2, RIPK2和TLK2。分析的结果是用于人类乳腺癌研究的一个高质量的蛋白质组学资源,是利用能够说明基因组与蛋白质组之间联系的技术和分析方法获得的。这些数据缩小了大的删除区域和扩增区域内候选驱动基因的范围,识别出了潜在的治疗目标。
而在Cell题为“Integrated Proteogenomic Characterization of Human High-Grade Serous Ovarian Cancer”的报导中,同样利用基于iTRAQ联合串联质谱的蛋白测量和鉴定技术,鉴定出这169种肿瘤样品中的9600种蛋白,并且选择研究了这些样品中常见的3586种蛋白。分析了169名卵巢癌患者的肿瘤蛋白质组以便鉴定她们所患肿瘤中存在的关键性蛋白。通过将这些卵巢癌蛋白质组方面的发现与已知的这些肿瘤的基因组数据整合在一起,使我们重新认识了最为恶性的卵巢癌---浆液性卵巢癌(serous ovarian cancer)。
尽管很多人知道我们的基因在癌症产生中发挥着作用,但是基因经常只是一个起始点。基因转录为RNA,然后RNA再翻译为蛋白。这些蛋白的活性存在显著差异,其中很多蛋白发生的变化影响它们的功能及其与其他蛋白之间的相互作用。癌症(特别是高分级浆液性卵巢癌)的特征是遗传指令发生差错。一种情形是基因组的某些区域存在更多拷贝。这些所谓的拷贝数变化能够导致蛋白丰度变化。在这项新的研究中,当对已知的发生拷贝数变化的基因组区域进行比较时,研究人员发现2号、7号、20号和22号染色体的部分区域导致200多种蛋白的丰度发生变化。
人类尚未充分认识复杂的癌症基因组是如何转化为导致复发和死亡的驱动生物学的,将蛋白质组学与基因组学结合在一起能够让我们获得对癌症的新认识,同时提供一种有价值的资源以便科学界能够用来提出关于这些疾病的新假设,以及治疗它的手段。蛋白质基因组学终有一天会被证明是一种强大的临床工具,使得人类能够横跨癌症基因组学与临床效应之间巨大的知识鸿沟。
以上两个案例中,蛋白质组学都使用了他独门绝技串联质谱技术中关键的一招——iTRAQ(这一招杀伤力极大,前面已作介绍,在此无需赘言),在此利用iTRAQ获得强大的蛋白质组数据完成了对基因组更深层次的注释。关于蛋白质基因组学夫妇的事迹就先介绍到这,但是他们的故事远未结束,相信在他们的紧密合作之下,还会不断碰撞出新的火花,比如说我们可以将基因组学中的测序或芯片数据与iTRAQ得到的蛋白质组学数据结合起来进行跨组学关联分析(具体的分析方法并不难,可以私信黄博深入讨论),从而获得表达谱的全景图,实现其间的互补和整合,对生物体特定状态下的基因和蛋白质表达水平进行全方位分析;并且在全局上获得对差异表达谱的广泛理解,挖掘受转录后调控的关键蛋白/基因,寻找验证某些重要的生物学调控;另外,对于一些蛋白数据库尚不完善的物种,通过转录组数据构建蛋白质序列数据库,提高蛋白质组学实验中蛋白质的鉴定数目。
今天咱就说到这儿吧,下次我们接着聊啥呢?
-
精英视角

-
会议会展

-
综述
-
财报

-
焦点事件

-
技术原理