酸碱滴定法的基本原理-强酸强碱的滴定
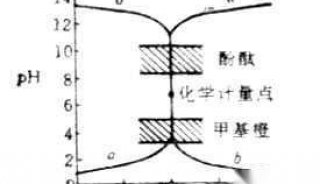
强酸和强碱相互滴定的滴定反应为:以NaOH液(0.1000mol/L)滴定20.00ml HCl液(0.1000mol/L)为例,滴定曲线如图1:
滴定开始前 pH=1.00
滴入NaOH液19.98ml时 pH=4.30
化学计量点时 pH=7.00
滴入NaOH液20.02ml时 pH=9.70
从滴定曲线可以看出:
(1)根据滴定突跃选择指示剂。滴定曲线显示,滴定突跃(在计量点附近突变的pH值范围)范围很大,为4.30~9.70,凡是变色范围全部或部分落在滴定突跃范围内的指示剂都可以用来指示终点,所以酸性指示剂(甲基橙、甲基红)和碱性指示剂(酚酞)都可以用来指示强碱滴定强酸的滴定终点。
(2)选择滴定液的浓度。浓度大,突跃范围宽,指示剂选择范围广;但是,浓度太大,称样量也要加大,所以一般使用0.1mol/L浓度的滴度液。
推荐
-
技术原理