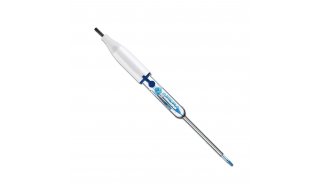
浅析氯化银电极的稳定性测试
氯化银电极是由表面覆盖有氯化银的多孔金属银浸在含Cl的溶液中构成的电极。氯化银电极可表示为Ag/AgCl/Cl,电极反应为AgCl+e=Ag+Cl。
氯化银电极电势稳定,重现性很好,是常用的参比电极。它的标准电极电势为+0.2224V(25℃)。优点是在升温的情况下比甘汞电极稳定。通常有0.1mol/LKCl,1mol/L KCl和饱和KCl三种类型。该电极用于含氯离子的溶液时,在酸性溶液中会受痕量氧的干扰,在工作中可通氮气保护。当溶液中有HNO3或Br,I,NH4,CN等离子存在时,则不能应用。此外,还可用作某些电极(如玻璃电极、离子选择性电极)的内参比电极。
由于Ag/AgCl电极在高温高压水溶液体系中具有很小的溶解度、极高的稳定性和可逆性,且即使在有氢存在的情况下电极表面也会得到很好的保护,这些特性都是其它电极无法比拟的。因此,人们对 Ag/AgCl 电极的研究更为深入和细致。
综合考虑电极微观形貌后可知,极差电位主要是由两个电极的反应活性面积不同引起的,氯化银电极反应活性面积的较大差距导致了极差电位不能控制在的范围内。由电极的工作原理可知,Ag /AgCl电极在海水中存在两个相界面,即 Ag-AgCl-Cl,电极表面的Ag和AgCl分别作为阳极和阴极参与反应过程并趋于平衡,即AgCl+e=Ag+Cl。
由于AgCl是一种难溶的盐,所以反应过程还存在着另一个平衡关系:AgCl→Ag+Cl。
当有电场信号传来时,微量电流通过电极界面,上述平衡出现偏离,由氯离子浓度控制的双电层遭受破坏,双电层重新建立平衡,导差电位的不稳定。所以极差电位及其稳定性是由电极表面的双电层决定的,而两电极表面的成分组成及形貌组织决定了双电层的分。银粉的粒度分布在 2~5 μm之间,则AgCl的颗粒数远多于银粉,AgCl的颗粒均匀地分布在银粉周围,且小颗粒的AgCl填充在大颗粒的银粉之间,从而有效地避免了大气孔的产生,大大提高电极的致密度及均匀性。电极表面缺陷少,可以看到AgCl稍微熔化时颗粒之间产生的界面,对于金属而言,由于晶界存在势垒,电阻率会随着晶界数量的增加而增加,氯化银电极这归结于晶界对传导电子的散射作用;由于样品电极内含有较多的银,电子将通过AgCl界面的散射和银交互传递,使信号有效的传导。