电导率测定方法介绍-电极法
一、电导率
电导率是用数字来表示降水样品传导电流的能力这种能力主要与降水总离子浓度、离子的电荷和水含半径、浓度及测量时的温度有关。降水中含有的无机酸、碱、盐具有良好的导电作用。而有机化合物在降水中离解度低,且浓度也低,对降水电导率影响较小。
二、电极法
1、原理
测定降水电导率的方法是测定降水的电阻率,电阻率的倒数即为电导率。距离1cm,载面积为1cm2的电极间所测得的电阻称为电阻率(Ω/cm)。距离1cm,截面积为1cm2的电极间所测得的电导称为电导率。用K表示。电导率的国际单位是S/m(西门子/米),也常用mS/m(毫西门子/米)或μS/cm(微西门子/厘米)表示。
 (1)
(1)
式中:C——电极常数;
R——电阻。
测量电导率的电极是由两块平行的铂黑片或铂片组成。根据本地区降水电导率的高低,可分别选用铂黑或铂电极。对于给定电极,C为常数,由(1)式可知,只要测出样品的R值,即可算出K。
电极常数C的测定,可选用一种电导率已知的标准溶液,利用该电极测其电阻,用下式计算出C值,常用的标准溶液为氯化钾溶液。
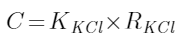 (2)
(2)
对于0.01000mol/L标准氯化钾溶液,25℃时KKCl为1413μS/cm,则(2)式变为:
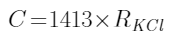 (3)
(3)
电导率多在25℃时进行测定。如果温度不是5℃,必须进行温度校正,校正的方法包括图解法和经验公式计算法。经验的温度校正计算公式为:
 (4)
(4)
式中:Kt——温度为t时的电导率;
Ks——25℃时的电导率;
a——各种离子电导率的平均温度系数0.022;
t——测定电导时溶液的温度。
2、仪器
①容量瓶:1000ml。
②烧杯:50ml。
③电导仪。
④恒温水浴器。
3、试剂
标准氯化钾溶液C(KCl)=0.01000mol/L:称取0.7455g氯化钾,溶解于重蒸蒸馏水中(重蒸蒸馏水必须煮沸以除去水中溶解的CO2,放冷后使用),移入1000ml容量瓶,用水稀释至标线。
4、步骤
1)温度调节
调节恒温水浴的温度为25℃,将盛有标准氯化钾溶液30ml的4支试管放入水浴中,恒温0.5h,使溶液温度达到25℃。
2)电极常数的测定
用3支试管中的标准溶液依次冲洗电极和50ml烧杯,将第4支试管中的标准氯化钾溶液倒入烧杯中,插入电极,测量电阻RKCl值按
(3)式计算电极常数C。
3)样品测定
使待测样品保持在25℃或接近于室温,用样品冲洗50ml烧杯和电极,然后装入30ml样品,测量杯中样品温度和电阻Rt值(R为温度t℃时的电阻)。
利用(1)式计算出样品的电导率Kt,再用
(4)式求出Ks。
5、说明
①测量完电导率的降水可用于pH值的测定。但不能用测量过pH值的降水样品来测量电导率,因为pH计的参比电极(甘汞电极)中的饱和KCl溶液会渗漏到降水中而改变它的电导率。同样道理,测过pH值的样品也不能用于降水离子成分的分析。
②新鲜蒸馏水的电导率为0.5~2μS/cm,存放数月后会增加到2~4μS/cm。原因是吸收了空气中CO2造成的,若实验室有酸、碱性气体污染则影响更大。因此降水样品应密封保存,尽快在采样后24h内测定完毕。




















