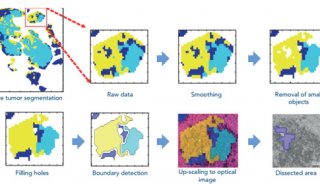
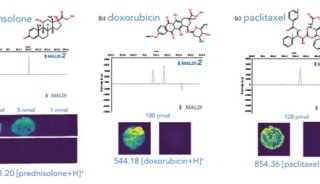
IR-58—潜在的结肠直肠癌靶向药物的鉴定(二)
3. IR-58的作用机制研究
IR-58优先富集在结肠直肠癌(CRC)细胞和异种移植物的线粒体中,这是一种糖酵解依赖性和有机阴离子转运蛋白多肽依赖性的过程。 IR-58通过诱导过度自噬(其通过活性氧(ROS)-Akt-哺乳动物类雷帕霉素靶蛋白(mTOR)途径介导)杀死肿瘤细胞并诱导凋亡。 RNA测序,质谱和siRNA干扰研究表明线粒体内膜44(TIM44) - 超氧化物歧化酶2(SOD2)途径转位酶受抑制导致IR-58诱导过度的ROS,自噬和细胞凋亡。 TIM44表达与CRC发展和患者预后不良呈正相关。

图3 用10μM IR-58 对HT-29, HCT116 , A549 细胞处理24小时并设置空白对照,然后进行RNA测序与质谱分析,重叠基因的mRNA表达增加。
图4
拟建IR-58自噬诱导机制模型。 IR-58优先以有机阴离子转运多肽(OATP)依赖性和糖酵解依赖性方式富集在肿瘤细胞的线粒体中。 IR-58显着抑制线粒体膜内44(TIM44)转位酶表达,使得超氧化物歧化酶2(SOD2)进入线粒体的摄取量减少,导致过度的活性氧(ROS)产生与哺乳动物雷帕霉素靶蛋白(mTOR)的去磷酸化,引发自噬。
随后,触发内源性凋亡。 PARP,聚ADP-核糖聚合酶。
结论:开发了一种新型NIR小分子自噬增强子,IR-58,具有线粒体靶向成像和治疗能力,用于CRC治疗。此外,TIM44第一次被确定为潜在的致癌基因,其通过TIM44-SOD2-ROS-mTOR途径在自噬中起重要作用。
新发现:IR-58被确定为优先富集在肿瘤细胞和体内特定目标肿瘤部位线粒体中的一种新的肿瘤自噬诱导小分子染料。
它在可预见的未来如何影响临床实践?
IR-58可能代表一种新型自噬诱导杀肿瘤小分子增强剂,而TIM44-SOD2-ROS-mTOR通路可能是临床CRC治疗的潜在靶标。 这项工作还可能提供一个潜在的策略来开发多功能小分子试剂用于成像指导的CRC治疗,这可以增强肿瘤靶向的特异性和减少离体靶组织中的潜在副作用,以及使实时监测肿瘤对治疗的反应。
原文:Huang Y, Zhou J, Luo S, et al.
Identification of a fluorescent small-molecule enhancer for therapeutic
autophagy in colorectal cancer by targeting mitochondrial protein
translocase TIM44[J]. Gut, 2016: gutjnl-2016-311909.
本研究中所用到的RNA Sequencing由锐博生物提供,所涉及到的动物实验以及siRNA锐博生物均有提供。
-
科技前沿
-
科技前沿
-
科技前沿