实验室分析方法--单组分的定量分析方法
根据Beer定律,物质在一定波长处的吸光度与浓度成正比,这是定量计算的依据。但是很多溶剂本身在紫外区有吸收峰或末端吸收,选用溶剂时应考虑溶剂本身吸收的干扰。选择溶剂时,被测组分的测量波长必须大于溶剂的截止波长。
常用的定量分析方法有标准曲线法、标准对照法、吸光系数法及差示分光法等,以下介绍前三种方法。
1)标准曲线法
标准曲线法又称工作曲线法或校正曲线法。标准曲线法较简单,在仪器分析中应用广泛,对仪器的精度要求不高,适合分析大批量的同类试样,但不适合分析组成复杂的样品。对于同一台仪器,在确定的工作状态和测定条件下,吸光度A与溶液浓度c之间呈线性关系。
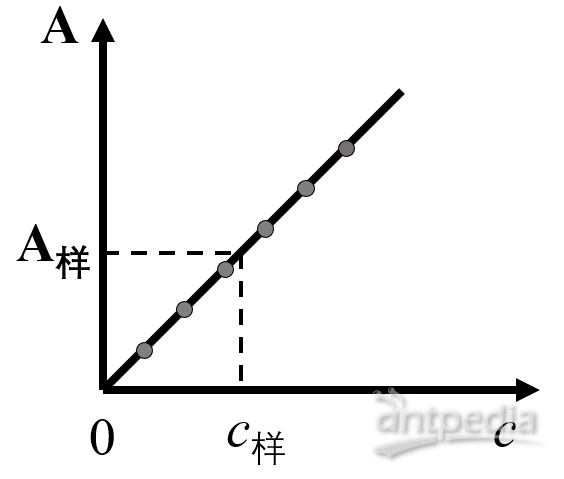
标准曲线
①测定方法
首先配制一系列不同浓度的对照品溶液(或称标准溶液),在相同条件下分别测定吸光度。以浓度为横坐标,相应的吸光度为纵坐标,绘制标准曲线(如上图),或根据二者的数值建立回归方程得A=bc+a。在相同的条件下测定试液的吸光度,从标准曲线或回归方程中求出被测组分的浓度。
②采用标准曲线法应注意的问题
(1)制备一条标准曲线至少需要5~7个点,并不得随意延长
(2)待测溶液浓度应在标准曲线线性范围内。
(3)待测溶液和对照品溶液必须在相同条件下进行测定。
根据Beer定律,理想的标准曲线应该是一条通过原点的直线。实际上,常有标准曲线不
通过原点的现象。其原因主要有几方面,如空白溶液的选择不当,显色反应的灵敏度不够,吸收池的光学性能不一致等,应采取适当措施加以改善。
2)标准对照法
如果绘制的标准曲线是通过原点的,测定试样时也可采用一种简化的方法,即标准对照法。
在相同条件下配制标准溶液(s)和样品溶液(x),在选定波长处,分别测其吸光度,根据Beer定律A=Ecl,因标准溶液和样品溶液是同种物质、同台仪器及同一波长于厚度相同的吸收池中测定,故l和E均相等,因此Cx=Ax Cs/As。
应用标准对照法的前提是绘制标准曲线需过原点,且一般要求标准溶液与样品溶液的浓度尽量接近,否则会引起较大的误差。
3)吸收系数法
根据Beer定律,若已知厚度l和吸光系数或百分吸收系数,即可根据供试品溶液测得的A值求出被测组分的浓度。C=A/El
许多化合物的吸收系数或百分吸收系数可以从有关手册或文献中查到。也可以将供试品溶液的吸光度换算成样品的百分吸收系数或摩尔吸收系数,然后与纯品的吸收系数相比计算出样品中被测组分含量。
如果查不到被测物质的吸收系数,或测定条件与手册、文献中不尽相同,则不能采用吸收系数法进行测定。