高分辨质谱仪实现非变性状态ADCs 药物的分析(一)
1 前言
单克隆抗体被认为是具有高度特异性的靶向药物,其对肿瘤细胞的靶向性非常高。而抗体- 药物偶联物(Antibody-drug conjugates,以下简称ADCs)技术,就是在抗体蛋白的特定氨基酸上偶联具有抗肿瘤作用的高效应化疗药物(或称小分子药物),以增加单克隆抗体的疗效、并降低小分子药物的毒性。相比单克隆抗体,ADCs 药物的生产工艺更为复杂,因此为了保证ADCs 药物的安全性和有效性,需对ADCs 药物的质量进行监控。药物抗体比(drug to antibody ratio,以下简称DAR)是评价ADCs 药物的生产工艺和产品质量的一个重要参数。目前大部分上市和在研ADCs 药物主要包括基于抗体自身的赖氨酸进行偶联的ADCs 药物(lysine-linked ADCs)和基于抗体自身链间二硫键经还原后的半胱氨酸进行偶联的ADCs 药物(cysteine -linked ADCs)(图1)。两类ADCs 的DAR 测定通常有UV、HIC和MS三种方法,其中MS检测方法因其快速、灵敏度高和强大的定性功能等优点,愈来愈广泛地被用于测定ADCs 的DAR。目前MS 用于测定ADCs 的DAR 通常是基于传统的RPLC/MS 平台,该平台下RPLC 采用的流动相呈酸性,且含有较高浓度的乙腈,蛋白在此条件下大多发生变性, 因此测定结果严格意义上讲反映的是ADCs 变性后的DAR。对于lysine-linked ADCs 而言,上述变性条件不影响其抗体结构的完整性,故RPLC/MS 平台不影响其DAR 测定。然而, 对于cysteine-linked ADCs 而言,上述变性条件破坏了维持抗体空间结构的非共价作用,ADCs 部分解离其轻链或重链,故RPLC/MS 平台无法用于其DAR 测定。随着非变性质谱(Native MS)技术的不断发展和推广,采用非变性质谱进行cysteine-linked ADCs 分析显示了强大的应用潜力。
Thermo ScientificTM ExactiveTM Plus EMR 质谱仪保持了Orbitrap 高分辨率、高质量精度的优势,同时扩展质量数范围至m/z 20000,并且在硬件设计上提升高质量端离子的传输效率,改进了HCD 压力,使其更加适用于完整蛋白质的分析。
适用于保留有三级和四级结构的非变性蛋白质和蛋白复合物的结构学、拓扑学研究以及生物制药中非变性状态下cysteine-linked ADCs 的分析。
本实验建立了基于ExactiveTM Plus EMR 和Protein Deconvolution 3.0 软件的非变性状态下蛋白质的分析流程(图2),并成功用于cysteine-linked ADCs 的分析,测定载有不同药物分子数的ADCs混合物的精确分子量,并测定其DAR值。

图1 Cysteine-linked ADCs 示意图
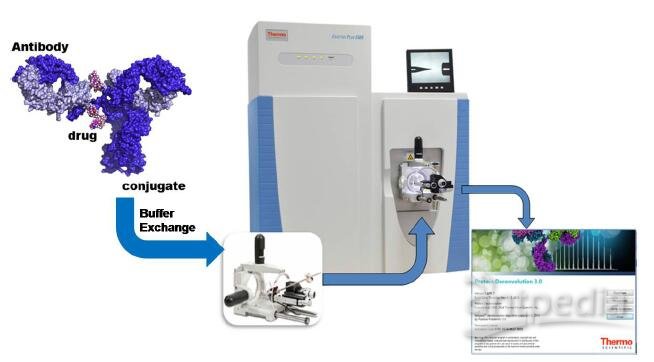
图2 非变性状态Cysteine-linked ADCs 的分析流程
2实验条件
2.1材料与方法
样品PCT为Cysteine-linked ADCs,PNGase F去糖基化后,采用Micro Bio-Spin® Chromatography Columns进行缓冲溶液交换,保存于100 mM 乙酸铵(pH 7.0)中,配制成浓度为5.5 μM的溶液备用。
2.2质谱分析
质谱仪 | Thermo Scientific Exactive Plus EMR |
离子源 | NanoFlex Source with emitter |
质谱数据采集模式 | Direct Infusion |
离子模式 | 正离子 |
喷雾电压 | 1.8 KV |
毛细管温度 | 275 ℃ |
毛细管温度 | ON |
质量范围 | m/z 3000–10000 |
分辨率 | 17500、35000、70000 |
S-lens (%) | 200 |
In-souce CID | 175 |
HCD | 25 |
MicroScan | 10 |
Spectra average | 50 |
-
企业风采

-
会议会展

-
企业风采

-
综述

-
产品技术

-
招标采购