单个神经细胞基因表达的qPCR综合分析
实验概要
本实验对单细胞的敏感性进行了分析,单细胞的基因分析可以为一种细胞类型高水平转换成另一种提供确切的证据。我们所描述的是Biomark Fluidig动态阵列分析单一神经细胞的高通量表达。在一次实验中,用96个qPCR探针(相当于9216次反应)分析高达96孔独立样本。它可以在2-3天之内完成。该实验对于几百个单细胞样品可以进行简单和有效的分析,实用性高。其过程如下图一: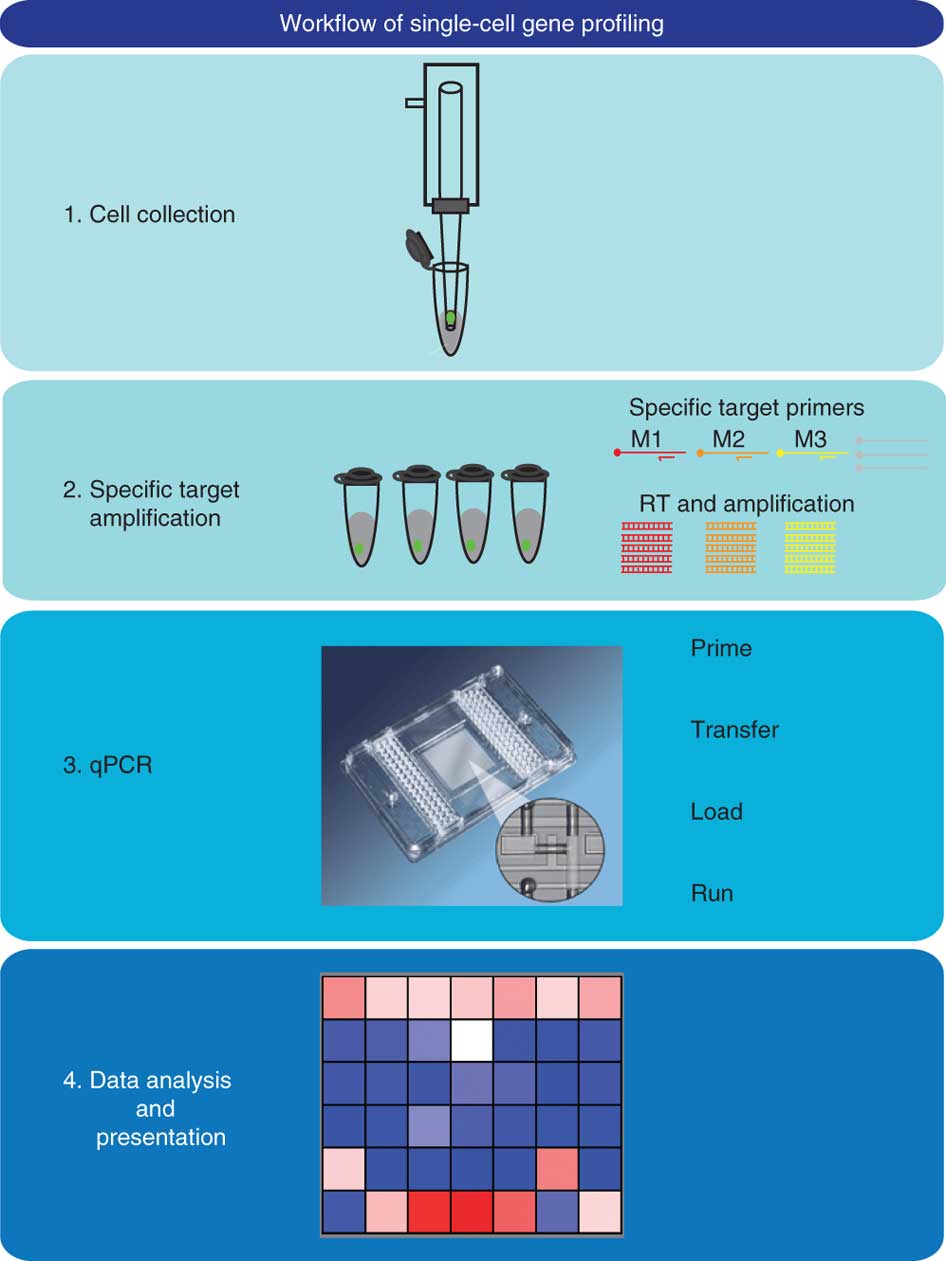
主要试剂
BioMark 48.48或96.96动态阵列(Fluidigm, cat. nos. BMK-M-48.48;BMK-M-96.96)
CellsDirect反应混合物(Applied Biosystems, cat. no. 11753-100)
TaqMan基因表达的预混液(Applied Biosystems, cat. no. 4369016)
DNAloading bufer(Fluidigm, cat. no. 100-0388)
EvaGreen DNA结合染料(Biotium, cat. no. 31000)
Assay loading reagent (Fluidigm, cat. no. 85000736)
低EDTA(0.1mMEDTA)的TE缓冲液(Teknova, cat. no. T0227)
ExoSAP(Affymetrix USB, cat. no. 78201))
氯化钠(Sigma-Aldrich, cat. no. S3014)
氯化钾(氯化钾; Merck, cat. no. 104938))
氯化钙.2 H2O((CaCl2, 2H2O; Merck, cat. no. 208291)
氯化镁.6 H2O(MgCl2, 6H2O; AppliChem, cat. no. A3618)
肝素钠(Sigma-Aldrich ,cat. no. H3375))
透明胶带(例如,透明胶带,3M)
实验步骤
1.收集单细胞
1) 准备PCR管,加入5μL 2×CellsDirect缓冲液(图2),置于冰上。
注意:使用无RNA酶的耗材和整个过程避免RNA的污染(清洁工作区,戴上手套,口罩,并使用无RNA酶的EP管)。
2) 在显微镜下,选择分离的单个细胞。显微下操作利用压力(3毫升注射器)清除单个细胞周围的物质,将细胞吸入移液管,将周围细胞或碎片对其污染降低到最小限度的(图2)。
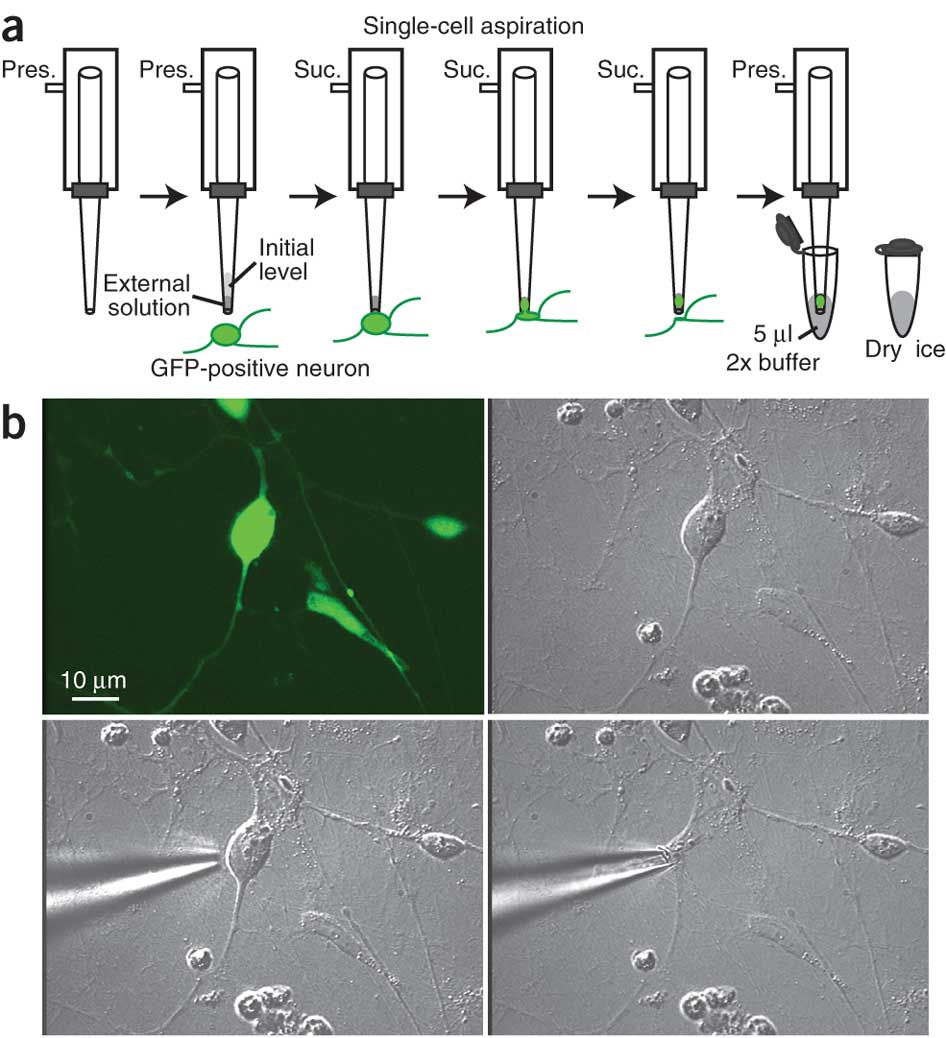
注意:使用最小的压力,以确保移液器吸取最少量的液体。
3) 收回移液管,移除注射器。将移液管枪头伸入PCR管底部。利用压力将细胞吹入溶液中,拿回移液器,立即冻结细胞于干冰上。
注意:使用最小压力吹出的细胞;每个EP管一次只能吸入一个细胞,只能应用一次;阴性对照样对qPCR分析必不可少;细胞可以储存-80°C几个月。
2. 特异片段扩增
1) 每个引物准备浓度为20 μM的引物对。对于特殊片段的扩增可以加大引物浓度(可达100个引物对),使每个引物终浓度为200 nM(如果您使用的是<100对引物,用稀释无RNase水,适当稀释)。请注意,如果被检测的基因多于100个,引物浓度相应增高(高于20μM)。
2) 准备如下反应混合物:
Component | Volume (μl; per sample) |
SuperScript III/RT Platinum Taq mix | 0.2 |
Primer mix (200 nM) | 2.5 |
RNase-free H2O | 1.3 |
Component | Volume (μl; per sample) |
SuperScript III/RT Platinum Taq mix | 0.2 |
Primer mix (200 nM) | 2.5 |
RNase-free H2O | 1.3 |
3) 从干冰取出细胞50℃水浴15秒解冻细胞,然后放在冰上。
4) 每管加入4μL反应混合物,放入PCR仪,预编程,运行如下:
Time | Temperature (°C) | Purpose |
15 min | 50 | Reverse transcription |
2 min | 95 | Denaturation |
Cycle 18–20 times: | ||
15 s | 95 | Denaturation |
4 min | 60 | Annealing and elongation |
Indefinitely | 4 | End |
5) 取出加入4μl的ExoSAP-IT,再放回PCR仪,运行如下:
Time (min) | Temperature (°C) | Purpose |
15 | 37 | Digest primers and dNTPs |
15 | 80 | Denature enzyme |
注意: cDNA可储存在-20°C,直到处理。
3. 样本的qPCR分析
1) 准备的qPCR反应液,如下所述:
Component | Volume (μl; per sample) |
TaqMan gene expression master mix | 2.5 |
DNA-binding dye sample loading reagent | 0.25 |
EvaGreen DNA-binding dye | 0.25 |
2) 在PCR管,准备如下的样本。然后快速涡旋几下。置于冰上。
Component | Volume (μl; per sample) |
Reaction mix | 3 |
ExoSAP-IT–treated samples | 2 |
3) 在PCR管加入分析样品如下,快速涡旋几下,置于冰上待用。
Component | Volume (μl; per sample) |
Assay loading reagent | 2.5 |
| qPCR primer pairs (20 μM) | 2.5 |
4) 准备Fluidigm Biomark qPRC芯片便于分析使用,将芯片放于IFC控制器激活 (15分钟)。
注意:该芯片必须加载1小时
5) 吸取5μL分析样本,5μL检测样本加入芯片上的进气口。
注意:吸取样品需谨慎,如有气泡,可以用干净无菌枪头除掉气泡。应小心以避免交叉污染或反应量的损失。
6) 样品上机。
7) 运行qPRC反应,包括熔解曲线分析,其运行的程序描述如下:
Time | Temperature (°C) | Purpose |
2 min | 50 | Thermal mixing |
30 min | 70 | Thermal mixing |
10 min | 25 | Thermal mixing |
2 min | 50 | Uracil-N-glycosylase activation |
10 min | 95 | Hot start for Taq polymerase |
Cycle 35 times: | ||
| 15 s | 95 | Denaturation |
| 1 min | 60 | Annealing and elongation |
| Ramp | 60–95 | Melting curve |
8) 初始化芯片扫瞄,允许ROX(参考染料)扫描进行。打开软件中ROX扫描文件,调试,如果未出现任何问题,让软件进行了充分的qPCR反应。
注意:在你选择的时间进行数据分析。
4. 数据分析
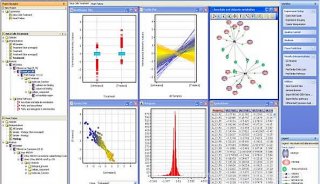
使用PCR分析软件分析数据。确定循环阈值后,数据以热图形式输出。选择数列快速检目从单细胞样品中获得的溶解曲线与参考反应比较获得的溶解曲线,用着稀释曲线分析。所有的数据,可以在输出在Microsoft Excel或其他类似的软件作进一步分析。
附 件 (共2个附件,占166KB)
![]()
图2.jpg
95KB 查看![]()
nprot.jpg
71KB 查看