单抗生产工艺的发展趋势(三)
3.3广泛应用的单抗下游平台
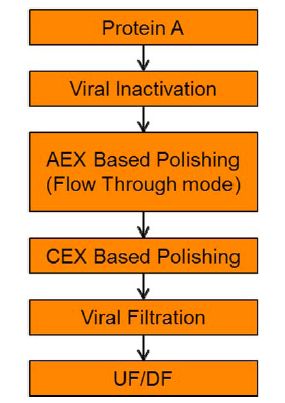
CEX和AEX的传统工艺不能完全满足这需求。实现该目标的一个关键修改是使用混合模式层析作为单抗下游平台的一部分。混合模式层析是将疏水基团加入AEX或CEX的骨架结构中。层析填料的疏水性增强,使其在CEX和AEX模式上都得到了改善了去除多聚体的能力,更适合于单抗工艺。此外,这两种层析方式还可同时去除HCP和DNA。不同单抗的亲水性不同。因此KBI公司的平下游台工艺被定义为阴离子交换层析(如Q葡聚糖FF或Capto Q或Fractogel SO3等疏水性填料到Captoadhere或Nuvia cPrime的混合模式填料)。这种对疏水性的调整可以为每一个单抗量身定做最佳的条件。同样的,取决于所选的填料种类,CEX的结合和洗脱工艺也会略微或者中等程度调整疏水性。尽管该方法需要一定程度的实验工作,如果适用于某个单抗,首选方法使用包含AEX和CEX的混合模式层析,这样可以使用较少的疏水性固定相的用量。如图6所示的该流程在KBI公司中包括单抗结构、细胞系和细胞培养工艺的等方面得到广泛应用。
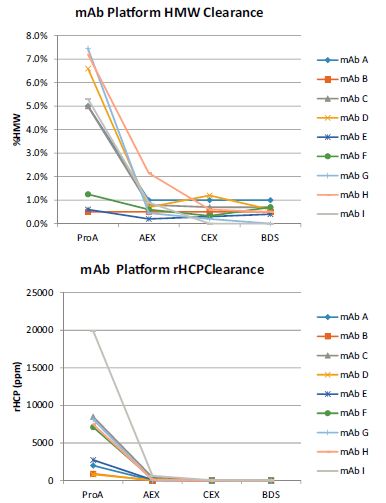
图7显示了,通过这个平台工艺进行了大量的单抗HMW聚合物和HCPs的清除图谱文件。从图中可以看出,采用该平台后,HMW的总水平小于1%, HCP低于50 ppm。特别是对于KBI公司这样的CMDO来说,能够广泛覆盖的不同结构单抗的能力是平台的关键。
图6 KBI生物制药公司为FIH manufacturing采用的单抗下游工艺
图7 KBI生物harma平台DSP方法的性能。(a)HMW结果,(b)HCP结果
各种下游平台工艺可以满足最先进的细胞批培养的单抗生产工艺处理需要。然而,在细胞培养工艺的生产力的提高要求研发替代方法,以提高下游的生产效率。由于希望更充分地利用现有的生产设施,并希望减少生物药的生产成本,这些技术在生物制药领域引起了极大的兴趣。最终目标是将生产的生物仿制药的成本降低到每克10美元。
4.1 连续生产
小分子药物通常采用连续生产方法,以最大限度地提高生产设备的生产效率。然而,而传统的生物制药生产只能采用离散的批生产方式,包括上游细胞培养工艺和下游的层析工艺。在这方面,人们对实现生物制药生产的持续加工的价值越来越感兴趣。流加细胞培养工艺是将新鲜培养基添加到原有培养基中,并不断提取含有产品的培养基,其主要用于不稳定或表达量低的产品。传统的流加培养工艺仅用于培养不能在批培养中达到高水平的被抑制表达或不稳定的产品。然而,出于生产效率的考虑而不是与产品本身有关,近期流加培养工艺正变得越来越普遍。因为不需要等待细胞低的接种量中扩增的时间,而是通过一个连续的连续介质来维持在高细胞密度的生产阶段,流加培养工艺可明显提高生物反应器的生产率。需要大量的细胞培养基的缺点可在后勤上适当解决,这套系统证明花费更高的费用获得更高的生产力合算的。此外,细胞分离技术的改进(如Repligen公司的切向流分离技术)也促进了的流加细胞培养的广泛应用。
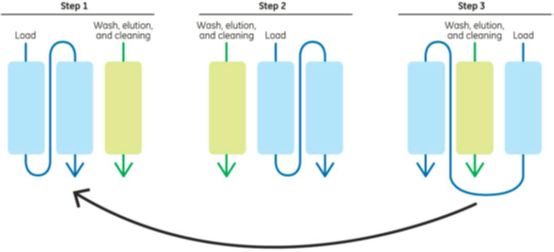
在连续流加培养中,产品的纯化可以通过分批层析系统的多个循环来处理,这也引起了对连续的上游和下游工序的重新兴趣。传统的层析是一个批处理过程。步骤从层析柱的卫生处理,平衡,和装载到洗涤,洗脱,脱柱和柱再生,和储存。批处理工艺的通量和生产率是有限的。首先,由于流动分布的限制,层析柱的最大直径只能达到2米。因压力降的限制,填料床高度最高只能装30厘米 (通常是20厘米)。这从根本上限制了单个循环处理产品的数量。当需要多个循环时,中间产品需要保存较长的时间。中间样品储存步骤也需要采用大体积的储罐,这是对生产率的另一个限制。连续的层析分离可以把这个批处理工艺变成连续的或半连续的工艺,如图8所示。结合一个持续的上游流加培养工艺,可以改变目前生物制药生产工艺的设计模式。最近对连续生产工艺的经济分析表明,连续生产工艺可以与传统的批量生产工艺相比,采用一个大幅减小的生物反应器的生产成本基本相同。这可以显著减少建造一个商业化生产的制造设施所需的资本支出。与2.1和2.2节中讨论的一致,该法是推动以低成本生产生物仿制药的驱动因素之一。有分析表明,即使在500L生物反应器的规模下,连续生产工艺也能达到17美元/g的低成本。
连续的层析分离可以采用多种形式进行。周期性的反流层析法是一种形式(来自GE医疗),即采用多个层析柱在操作循环的不同阶段实行连续操作。其他形式包含多柱逆流溶剂梯度净化,采用ChromaCon公司的ContiChrom®系统、Tarpon Biosystems公司(现为颇尔公司)的BioSMB 技术从和Semba Bio公司的Octave 层析系统回收的洗脱峰的前部和尾部以增加产量以及纯度。
最近在该领域的一场争论是,为了尽可能提高的生产率,采用端到端的连续工艺是否需要以及如何实行。为实现该目标需要将多个工艺步骤,包括病毒灭活、超滤/透析和病毒过滤工艺整合为一个连续的流程。随着时间的推移,不断地进步的将会出现,但是否需要一个完全连续的工艺仍有争议。将连续的细胞培养与连续的吸附层析相结合,然后通过在第3.2节中描述的高加载精制工艺完成剩余的单抗下游工序,可能已可以满足需要。
持续生产工艺的进一步发展是不可避免的,并将导至供应商生产数量和营销系统的数量发生改变。这一领域已经克服了一些关键的技术障碍,现在的重点是对这些系统进行大规模的验证,以及使用快速的过程控制技术来改进这些系统的控制。在本文列出的新兴技术领域中,因它仍选用传统的层析填料所,连续生产似乎是第一个将大规模实现的系统。
图8 连续层析原理
4.2 非层析分离
另一种提高生产率的方法是将层析工艺换为非层析工艺。对层析的依赖的一个关键原因是它能够处理大量的宿主细胞蛋白杂质,同时将与产品的性质高度相似的组分的分离。然而,层析步骤是明显的限速步骤,尤其是遇到大批量生产的产品时,比如采用大体积的生物反应器中进行高表达培养时。生物分离依赖的层析工艺,受限于层析柱的床直径和床高度。多数层析填料是可压缩的,这意味着装柱时不能使用低压泵和cGMP生物制药的系统中使用的系统将柱子超过一定高度。此外,目前最大直径的层析柱的直径为2米。因此,即使有了连续的层析,载量仍然是受限的。非层析分离的设想是寻找一个代替层析的方法,一次性处理整批细胞培养收获液的操作实现生物分离。这有可能极大地提高生物制药的生产能力。
使用聚合物的选择性沉淀方案可以在一次操作中捕获整个生物反应器中的产物,而不是依赖于多个层析循环。如果这些类型的单元操作具有高度选择性和一般性质的,它们将会在大规模的生物处理中得到广泛应用。有多种聚合物可以用于单抗的沉淀,如阴离子高聚物沉淀产品和辛酸水解宿主蛋白杂质。不同机制的聚合物的组合可以创造出更好的选择性。例如,盐(高离子强度导至的沉淀)可以与带电的聚合物结合,可以通过电荷的中和作用或者通过蛋白质分子排斥作用的聚乙二醇(聚乙二醇)实行分离。合适的组合有可能产生高度选择性的分离,这样就可以减少下游工序中多个连续的层析工艺的依赖,也有可能设计出具有多种机制的聚合物,实现对宿主细胞蛋白杂质或产品的选择性沉淀。
选择性沉淀的另一个扩展是絮凝生物反应器上清中的细胞。絮凝剂如低pH (< pH 5.0)和聚合剂,如PDDA(polydiallyldimethylammonium chloride)不仅可以用来沉淀细胞和细胞碎片,也沉淀了宿主细胞蛋白质和DNA等杂质。因此,絮凝剂在在收获中在已其其他作用的同时,还可用于大规模去除杂质。在某些情况下可以去除大量的宿主细胞蛋白质,这样就可以减少下游工艺步骤。
双水相萃取(ATPS)通告向溶液中加入混合聚合物和盐或两种聚合物而产生两个分离的水相。如加入PEG-盐和右旋-PEG APTS。已有数个采用ATPS实行高选择性分离的报道。然而,由于分区机制难以开发,而且通常不具备足够的专属性支持单抗之类的蛋白质的分离,所以其大规模应用受到了限制。已有一个PEG/磷酸的ATPS系统实现了从转基因植物提取物中单抗的目的。最近,多步ATPS已经开发出来,试图为多种不同类型的单抗创建一个统一的平台。考虑到分离领域的需求,预计未来ATPS会有更大的发展。
所有这些分离技术都有引入关注的潜力,并且可以大幅提高现有主流生产设备的处理能力。然而,所有这些技术都需要进一步的开发,以使自己成为可扩展的技术,可以在不需要优化的情况下普遍适用于各种单抗的纯化工。
4.3 筛选表达系统
除了哺乳动物细胞培养外,单抗还可以在其他表达系统中产生。进一步发展的一个关键领域是研究替代表达系统,该系统可以产生更高的生产力,同时保留与人类免疫系统兼容的糖基化模式。这些发展可能会使这个领域超越目前最先进的CHO细胞培养。
一个关键的替代表达系统是转基因植物。其中一些系统已经用于临床生产,例如转基因烟草。使用土壤杆菌(Agrobacterium)瞬转获得转基因烟草。这种方法被广泛用于生产中和HIV病毒的抗体。许多公司已经开始使用烟草作为首选的表达系统(Medicago, Kentucky Bioprocessing)。然而,转基因植物表达的挑战仍然包括高水平的内毒素和较低的表达水平。另一种担忧是蛋白酶的分泌,导至植物提取物的有效期缩短。此外,目前对转基因植物生长的担忧限制了这种技术的扩展性,大规模生产的实施有赖于公众的认可。将转基因植物与一般的生态系统分离的要求意味着它们的种植只能局限于大型的、自动化的温室。这限制了这项技术的快速扩展。在这一领域进行了大量的研究,植物表达可能是未来大规模商业生产的一种技术。
大肠杆菌的胞内和胞外均可产生非糖基化单抗和抗体片段。很有吸引力的是大肠杆菌可以快速培养并达到较高的表达水平。然而大肠杆菌没有糖基化机制,因此如果糖基化对活性很重要,这可能是限制其应用的一个重大的不足。目前,大肠杆菌主要作为单抗生产平台的补充,仅用于抗体片段的临床样品生产。
酵母表达系统已被用于临床生产。特别的是,啤酒酵母已用来表达商业多种生物疗法的。然而,一个关键的限制是在啤酒酵母中产生过多的非哺乳动物糖基化模式。此外,由于内质网中错误表达和折叠,啤酒酵母的全长度单抗的表达水平受到了限制。毕赤酵母是一种较好的重组蛋白质表达系统。这是一种可以在非常高的细胞密度下培养的甲基营养酵母。在毕赤酵母系统中使用的启动子非常强大,并且在细胞外分泌的情况下会产生显著的表达水平(高达20 g/L)。毕赤酵母的糖基化比在啤酒酵母中要少。毕赤酵母的工程菌株消除了蛋白酶表达的问题,同时也可抑制了高甘露糖的生成。这个系统面临的另一个挑战是,在这个表达系统中缺少适当的蛋白质折叠伴侣。其结果是,该产品可以以多种形式存在。不过,随着毕赤酵母的工程菌株被开发出来,这一障碍可以被克服。毕赤酵母的高产能使其成为单抗未来的候选对象表达体系。
生物制药生产的另一个新兴平台是微藻生产系统。微藻是一种光合微生物,可在很大数量的发酵器中培养。微藻已被用于工业生物技术产品的生产。当前微藻发酵系统的产量仍然相对较低。在这个表达系统接受生物制药生产之前,还需要克服其他障碍,包括糖基化和其他转录后的修饰。
本文讨论了单抗平台方法以及它在加速许多不同疗法向临床和市场的发展的必要性。使用平台方法使许多生物制药公司能够在一年或更短的时间内成功地从基因中取得成功。基于它们的内部抗体结构,细胞株和细胞培养过程,每个生物制药组织已经开发出了它最适宜的平台方法。最新的趋势包括使用多模态层析法作为工艺平台的一部分,以及在一种流动模式下使用两步精制工艺。这些工艺改进使单抗平台的更广泛的适用性,以及对下游处理的吞吐量瓶颈有意义。随着细胞培养能力的不断提高,其他可以提高下游工序生产率的替代形式也在不断发展。这些包括蛋白质在连续模式下的操作,而不是一种批处理模式。可以想象,连续处理可以在未来的整个下游工艺中得到发展。使用沉淀或ATPS的非层析分离工艺是单抗下游工艺的另一个可能的未来方向。下一个十年将会看到单抗下游工艺平台的进一步发展,这是基于生产力和新的分子模型的驱动。
参考文献:
Shukla AA, Wolfe LS, Mostafa SS, Norman C.Evolving trends in mAb production processes.Bioeng Transl Med. 2017 Apr 3;2(1):58-69.