君实启动PD-L1治疗晚期或复发性实体瘤I期临床研究
2月12日,君实登记启动了其自主研发的人源化抗PD-L1单克隆抗体JS003的一项国内I期临床研究,用来评估JS003在经治的晚期或复发性实体瘤受试者中的安全性、耐受性和剂量限制性毒性(DLT)。计划入组36人。

来源:药物临床试验登记与信息公示平台
该研究为开放、非随机、单臂试验,主要终点指标为首次及末次给药后21天的安全性、耐受性和剂量限制性毒性(DLT);次要终点为:免疫原性JS003抗药抗体产生的时间和比例;JS003的血清浓度及PK参数,JS003的抗肿瘤活性,JS003的受体占位和淋巴细胞亚群分析。试验分组如下:

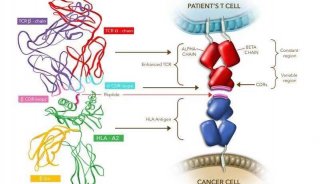
JS003是君实自主研发的人源化抗PD-L1单克隆抗体,于 2018年8月获NMPA核准签发药物临床试验批件。PD-L1是重要的癌症生物标志物和免疫疗法的靶标。PD-L1与PD-1的结合诱导T细胞耗竭,即一种无效的T细胞活性状态。许多临床研究证明,通过抗PD-L1单抗与PD-L1结合,从而阻断PD-L1与PD-1结合可逆转T细胞耗竭状态并增强其抗肿瘤活性。
根据君实于2019/9/26递交的科创板招股书介绍,JS003与国外同类药物相比,识别相同的靶点PD-L1,具有完全不同的抗原识别CDR 序列,且临床前药效学表明其作用强度和持续时间与国外同类药物相当,临床前药代动力学显示其具有较低免疫原性,并已进入I期临床。

推荐
-
焦点事件

-
企业风采