Nature子刊:吸烟导致PD-L1高表达,从而诱发肿瘤免疫逃逸
据WHO世界卫生组织2017年统计,吸烟每年造成约700万人死亡,烟草和烟草烟雾中已发现8000多种化合物,其中70种是致癌物质,包括多环芳烃(PAHs),以及烟草特有的亚硝胺、挥发性亚硝胺等等。烟草烟雾会诱导大量的体细胞基因组突变,进而诱发肺癌等癌症的发生发展。肺癌目前已经成为发病率第一的癌症,超过87%的肺癌由烟草烟雾引起,吸烟所产生的烟草烟雾已经成为目前全世界面临的最大公共卫生威胁。
吸烟会导致肺癌等多种癌症,然而奇怪的是,使用细胞免疫疗法治疗癌症时,吸烟的癌症患者对免疫疗法的治疗效果反而比不吸烟者更好。这是为何?
2019年3月,国家癌症中心周光飙团队在 Nature 子刊 Nature Communications 杂志上发表题为:The Aryl hydrocarbon receptor mediates tobaccoinduced PD-L1 expression and is associated with response to immunotherapy 的研究论文。
该研究发现,吸烟产生的烟雾会通过芳香烃受体(AhR)诱导PD-L1的过表达,从而导致肿瘤的免疫逃逸,促进肿瘤的进展。因此针对PD-L1/PD-1的细胞免疫疗法对吸烟的癌症患者效果更好。

PD-1(programmed death 1),程序性死亡受体1,是免疫细胞T细胞上表达的一种蛋白,用于识别并“杀死”肿瘤细胞。
PD-L1(programmed cell death-Ligand 1),程序性死亡受体-配体1,是肿瘤细胞上所表达的蛋白,PD-L1会特异性结合PD-1,结合后便抑制了T细胞的活化和增殖,从而造成肿瘤细胞的逃逸。
基于PD-1/PD-L1的免疫检查点抑制剂,成功开发并上市了多款细胞免疫治疗药物,拯救了无数癌症患者,基于免疫检查点的细胞免疫疗法也荣获了2018年的诺贝尔生理学或医学奖。
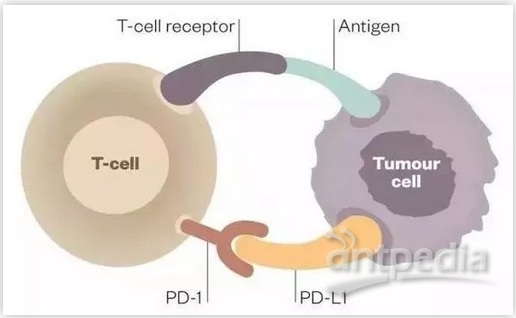
PD-1/PD-L1的免疫检查点抑制剂,对肺癌的治疗也显示出了有希望的临床疗效,然而,和不吸烟的肺癌患者相比,接受PD-1/PD-L1抑制剂治疗的吸烟肺癌患者的客观改善更明显、临床益处更持久、生存期更长。
之前的研究表明,吸烟者的肿瘤细胞中存在更高的非同义突变和更高的新生抗原负荷,说明吸烟可能诱发了肿瘤免疫逃逸,因此针对免疫逃逸的细胞治疗对其效果更明显。
该研究首先通过体外和体内实验,发现烟草烟雾和苯并(a)芘(简称BaP,烟草等燃烧不充分时产生的一种致癌物),均会诱导肺上皮细胞的PD-L1过表达。
表达PD-L1的肺癌细胞,会通过与T细胞上PD-1结合,从而抑制T细胞,产生肿瘤免疫逃逸。因此吸烟产生的烟雾,通过遇到肺上皮细胞表达PD-L1使肺癌细胞逃过T细胞的免疫检查。
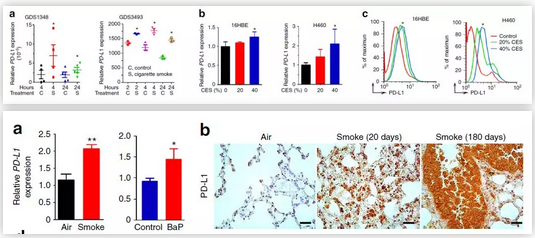
烟草烟雾中的BaP会诱导PD-L1的表达,Luciferase报告基因实验表明,PD-L1基因启动子上存在芳香烃受体(AhR)的结合位点,芳香烃受体(AhR)介导了BaP对PD-L1的过表达。
肺癌小鼠模型实验发现,AhR抑制剂发挥了显著抗肿瘤活性,并与PD-L1抗体发挥协同作用。
这些结果表明,烟草烟雾会通过芳香烃受体(AhR)诱导肺上皮细胞的PD-L1表达,从而逃避T细胞杀伤以促进肿瘤发生,并且表明芳香烃受体(AhR)能够预测患者对免疫疗法的反应,也可以作为一个有吸引力的治疗靶标。
通讯作者

周光飚,中国科学院动物研究所二级研究员,膜生物学国家重点实验室肿瘤分子机理与靶向疗法研究组组长,国家杰出青年科学基金获得者。主要研究空气污染、 吸烟引起肺癌的机理等。
2009 -至今, 中国科学院动物研究所生物膜与膜工程国家重点实验室,研究员
2005 -2009
研究员, 中科院广州生物医药与健康研究院
2003 -2005
博士后, 中国科学院上海生命科学研究院
2000-2003
博士研究生,上海交通大学医学院
1997-2000
硕士研究生,中南大学湘雅医学院
1988-1993
学士,广西医科大学
论文链接:
https://www.nature.com/articles/s41467-019-08887-7
-
科技前沿
-
项目成果

-
项目成果
-
产品技术