基因调控网络深度解读2型糖尿病发展,RFX6基因关键引领早期胰岛细胞缺陷
研究人员通过包括基因表达、遗传风险和功能数据在内的分析,已经开始揭示2型糖尿病(T2D)背后的基因调控网络,强调了转录因子编码基因RFX6的关键作用。
《自然》杂志上周一报道称,研究人员依赖于细胞分类的胰岛细胞的转录组分析,再加上胰腺组织成像和胰岛细胞功能分析,对20名早期患有T2D的基因分型个体和19名未受影响的个体的胰腺样本进行了分析,并将结果与通过先前的全基因组关联研究与T2D风险相关的遗传信号相对比。
使用这种方法,团队找到了富集T2D相关风险变异的调控模块,包括调控一种称为β细胞的胰岛细胞亚群的模块。
结果促使研究人员仔细研究其中一个模块,该模块以转录因子基因RFX6为中心,使用七名捐赠者个体的伪胰岛细胞样本中的基于短发夹RNA的基因敲除。
与先前指出罕见的RFX6编码变异在早发糖尿病风险中发挥作用的研究一致,他们的单核RNA测序和单核ATAC-seq实验表明,缺乏RFX6基因的胰岛细胞导致具有改变染色质可及性的β细胞,这些染色质可及性位点包含先前GWAS中标志的T2D风险变异。
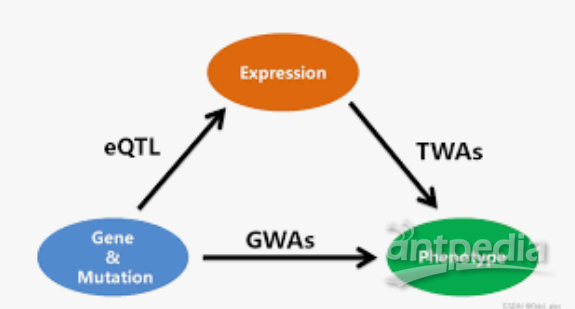
同样,团队对可用的英国生物库数据的分析指出,存在预计会降低RFX6表达的非编码遗传变异时,T2D风险显然上升。
作者写道:“总体而言,我们的结果和先前的信息揭示了与RFX6及其调控网络相关的多层遗传收敛,”他们补充说,“三种不同类别的遗传变异都在糖尿病中收敛于RFX6生物学。”
研究人员推测,在胰岛细胞发育或β细胞维持过程中,RFX6活性的改变可能会随着时间的推移通过与环境、营养和与年龄相关的因素的相互作用而显现出来。他们指出,需要进一步的研究来区分这种可能性与一个模型之间的差异,在该模型中,β细胞的影响是由影响RFX6含有的调控模块的许多常见T2D遗传风险变异的累积遗传效应引起的。
作者写道:“确切的是,引起最初的RFX6失调的原因以及是否可以通过靶向来防止或逆转β细胞中的早期分子和功能缺陷,应该是一个积极研究的领域。”
更广泛地说,他们建议可以使用类似的策略来深入研究其他经过GWAS分析的特征或疾病的调控基础。
“理解复杂的系统性疾病的分子机制需要整合来自多种分子、细胞、器官和个体的信号,因此我们预计,这种方法将是使用GWAS数据识别和验证其他疾病和特征的关键调控网络和主控基因的有用模板。