硬实力!杨辉团队Cell,Nature系列子刊等发表8项研究成果
近一年来中国科学院神经研究所杨辉团队连续取得突破,在Cell, Protein & Cell,Nature Communications ,Nature Cell Biology,Nature Protocol,Nature Methods 等杂志上发表了8项重要研究成果,在基因编辑领域取得重大进展,iNature系统总结了这些研究成果:
【1】CRISPR-Cas9 介导的无缝基因组编辑可以通过同源定向修复 (HDR) 将供体 DNA 整合到 CRISPR-Cas9 靶基因座中来实现,尽管由于外源 DNA 的低效递送而效率相对较低。 Retrons 是细菌-噬菌体防御相关的操纵子,由专门的逆转录酶 (RT) 和相关的非编码 RNA (ncRNA) 组成,可以通过 RT 在保守的鸟苷 (G) 残基处启动来部分逆转录,以产生多拷贝的单链 DNA (msDNA)。retron 与 CRISPR-Cas9 结合可以通过 HDR 在细菌和酵母中通过将引导 RNA (gRNA) 融合到 retron ncRNA 的 3' 端,共价产生多拷贝单链 DNA (msDNA) 来增强精确的基因组编辑。但基于反转录子的基因组编辑系统效率还很低,且尚未证明能在哺乳动物细胞中发挥作用。尽管如此,反转录子在基因组编辑应用中仍显示出独特的优势。2021年8月17日,中科院脑科学与智能技术卓越创新中心杨辉及辉大生物孔祥锋共同通讯在Protein & Cell 在线发表题为“Precise genome editing without exogenous donor DNA via retron editing system in human cells ”的研究论文,该研究通过将 Cas9 与来自不同进化枝的大肠杆菌 RT 融合,并在 retron ncRNA 的 5' 末端连接 gRNA ,进一步改造了 retron,并发现 retron 编辑可以在人类细胞中有效地实现精确的基因组编辑。通过在 HEK293T 细胞中共表达 Cas9-RT 融合和逆转录-ncRNA gRNA (rgRNA),该研究证明内源性基因组位点逆转录编辑介导的 HDR 事件的发生率高达 10%。总之,该研究首次证明了细菌的防御系统反转录子(Retron)可以用于哺乳动物细胞的精确基因组编辑,而且可以避免Cas9带来的DNA双链断裂,可能更加准确和安全。有望为体外和体内基因编辑治疗带来全新的基因编辑系统。
【2】CRISPR-Cas13和CRISPR-Cas12系统中新发现的特征(如“附带效应”或反式切割)已使其能够用于核酸检测。据报道,Cas13a的侧链RNA切割对细胞发育有害。作为CRISPR-Cas12系统的代表性基因编辑器,CRISPR-Cas12a(Cpf1)在未来的治疗应用中具有巨大潜力。然而,当用于哺乳动物细胞中的基因组编辑时,目标激活的Cas12a有在复制,转录和同源性导向的修复过程中裂解瞬时暴露的ssDNA的风险,引起了人们的关注其治疗应用。因此,需要仔细研究由Cas12a的不加区分的ssDNA裂解活性引起的潜在脱靶效应。2021年4月1日,中国科学院神经研究所周昌阳,杨辉及中国农业科学院深圳农业基因组研究所左二伟等共同通讯在Protein & Cell 在线发表题为“Indiscriminate ssDNA cleavage activity of CRISPR-Cas12a induces no detectable off-target effects in mouse embryos”的研究论文,该研究开发了GOAT,无需FACS即可检测基因编辑工具对全基因组的脱靶效应。与GOTI相比,GOAT是一种更简单,成本更低的方法,具有相当的准确性和灵敏度。使用GOAT分析,该研究发现Cas12a(LbCas12a和AsCas12a)的反式ssDNA切割活性在小鼠胚胎中较低,这表明Cas12a在哺乳动物细胞中具有高度特异性。考虑到LbCas12a和AsCas12a具有与spCas9相当的编辑效率,更小的尺寸和更低的错配耐受性,它们在未来的治疗应用中具有广阔的前景和竞争优势。
【3】2021年1月4日,中国科学院神经研究所杨辉及周海波共同通讯在Nature Cell Biology 在线发表题为”Endogenous promoter-driven sgRNA for monitoring the expression of low-abundance transcripts and lncRNAs“的研究论文,该研究开发了一种通用的内源性转录门控开关,该开关在存在内源性启动子的情况下释放单向导RNA。 当内源转录门控开关与开发的高度敏感的CRISPR激活物相关报道分子偶联时,可以可靠地检测内源基因的活性,包括表达水平非常低的基因(相对于Gapdh,<0.001;定量PCR分析) 。值得注意的是,该研究还可以使用这种方法监测在活细胞中低水平表达的典型的长非编码RNA的转录活性。总之,该研究方法提供了一个强大的平台,可以感知细胞功能背后的内源性遗传元素的活性。
【4】2020年11月27日,上海科技大学黄行许,池天及中国科学院神经研究所杨辉共同通讯在Nature Communications 在线发表题为“A Cas-embedding strategy for minimizing off-target effects of DNA base editors”的研究论文,该研究发现只需将将编辑酶插入nCas9的中间,就可以显著降低A> G和C> T编辑器的脱靶效应,而不会破坏靶上编辑。 此外,采用这种Cas嵌入策略,该研究创建了一个高度特定的编辑器,能够对甲基化和富含GC的序列进行高效C> T编辑。
【5】2020年8月14日,中国科学院神经研究所杨辉,中国科学院上海营养与健康研究所李亦学及斯坦福大学Lars M. Steinmetz共同通讯在Nature Protocol 在线发表题为“GOTI, a method to identify genome-wide off-target effects of genome editing in mouse embryos”的研究论文,该研究为GOTI提供了详细的技术方案,包括小鼠交配,两细胞胚胎注射,胚胎第14.5天胚胎消化,荧光激活细胞分选,全基因组测序和数据分析。为了增强GOTI的效用,该研究还包括一个称为GOTI-seq(https://github.com/sydaileen/GOTI-seq)的计算流程,用于测序数据分析,可以生成最终的全基因组脱靶变异体直接从原始测序数据中提取。从小鼠交配到测序,该试验方法通常需要20天,而测序数据分析则需要7天。
【6】2020年5月18日,中国科学院脑科学与智能技术卓越创新中心杨辉,究所隶属于的计算生物学研究所(中国科学院-马普学会计算生物学研究所)李亦学及中国农业科学院深圳农业基因组研究所左二伟共同通讯在Nature Methods 在线发表了题为"A rationally engineered cytosine base editor retains high on-target activity while reducing both DNA and RNA off-targeteffects"的研究论文,该研究根据蛋白结构预测了脱氨酶ssDNA结合的重要氨基酸,在不影响催化活性的情况下,突变相应的氨基酸(APOBEC1上的ssDNA结构域相应氨基酸),从而得到了显著降低DNA脱靶的CBE突变体。
【7】2020年4月8日,中国科学院上海神经所杨辉及周海波共同通讯在Cell 在线发表题为“Glia-to-Neuron Conversion by CRISPR-CasRx Alleviates Symptoms of Neurological Disease in Mice”的研究论文,该项研究通过运用最新开发的RNA靶向CRISPR系统CasRx特异性地在视网膜穆勒胶质细胞中敲低Ptbp1基因的表达,首次在成体中实现了视神经节细胞的再生,并且恢复了永久性视力损伤模型小鼠的视力。同时,该研究还证明了这项技术可以非常高效且特异地将纹状体内的星形胶质细胞转分化成多巴胺神经元,并且基本消除了帕金森疾病的症状。该研究将为未来众多神经退行性疾病的治疗提供一个新的途径。
【8】微生物和病毒之间的竞争性共同进化导致CRISPR-Cas防御传染病的防御系统多样化。2021年5月3日,上海脑科学与类脑研究中心、神经科学国家重点实验室杨辉,周英思和中国农业大学农学院赖锦盛共同通讯在Nature Methods 在线发表题为“Programmable RNA editing with compact CRISPR–Cas13 systems from uncultivated microbes”的研究论文,该研究通过分析宏基因组的terabase数据集,鉴定了来自高盐样品的CRISPR-Cas核糖核酸的两个紧凑家族(775至803个氨基酸(aa)),命名为Cas13X和Cas13Y。该研究设计了Cas13X.1(775 aa),用于哺乳动物细胞系中的RNA干扰实验。该研究发现Cas13X.1可以耐受RNA识别中的单核苷酸错配。此外,由工程化脱氨酶(385氨基酸)和截短的Cas13X.1(445氨基酸)组成的最小RNA碱基编辑器表现出强大的编辑效率和高特异性,可诱导RNA碱基转化。该研究结果表明,天然微生物中存在尚未开发的细菌防御系统,可以有效地在哺乳动物细胞中发挥作用,因此可能对基于RNA编辑的研究有用。

CRISPR-Cas9 介导的无缝基因组编辑可以通过同源定向修复 (HDR) 将供体 DNA 整合到 CRISPR-Cas9 靶基因座中来实现,尽管由于外源 DNA 的低效递送而效率相对较低。Retrons 是细菌-噬菌体防御相关的操纵子,由专门的逆转录酶 (RT) 和相关的非编码 RNA (ncRNA) 组成,可以通过 RT 在保守的鸟苷 (G) 残基处启动来部分逆转录,以产生多拷贝的单链 DNA (msDNA)。逆转录后,msDNA 通常通过 ncRNA 中的启动 G 和 msDNA 的 5' 端之间的 2',5'-磷酸二酯键共价连接到 ncRNA。逆转录过程,其中专门的 RT 识别逆转录 ncRNA 的独特二级结构。此外,通过用所需序列替换逆转录 ncRNA 的可有可无区域,可以在体内生成所需的 msDNA。因此,retron 是体内生成 DNA 供体用于 HDR 介导的精确基因组编辑的有前途的生物来源。
最近,一些研究表明,retron 与 CRISPR-Cas9 结合可以通过 HDR 在细菌和酵母中通过将引导 RNA (gRNA) 融合到 retron ncRNA 的 3' 端,共价产生多拷贝单链 DNA (msDNA) 来增强精确的基因组编辑。在本研究中,通过将 Cas9 与来自不同进化枝的大肠杆菌 RT 融合并在 retron ncRNA 的 5' 末端连接 gRNA ,进一步改造了 retron,并发现 retron 编辑可以在人类细胞中有效地实现精确的基因组编辑。通过在 HEK293T 细胞中共表达 Cas9-RT 融合和逆转录-ncRNA gRNA (rgRNA),该研究证明内源性基因组位点逆转录编辑介导的 HDR 事件的发生率高达 10%。研究人员希望逆转录编辑系统可以帮助推进逆转录的体外和体内治疗应用。
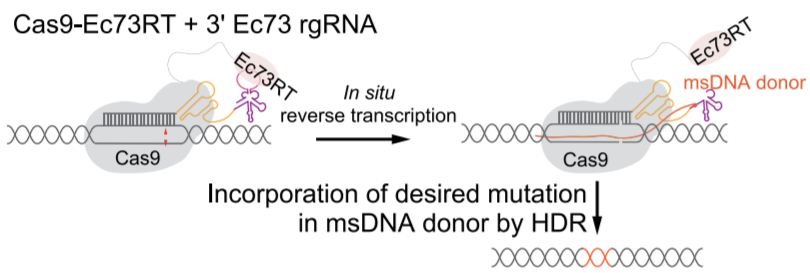
示意图显示Cas9-Ec73 RT融合原位逆转录3'Ec73 rgRNA,生成包含具有同源臂的单链供体序列的msDNA,并将msDNA并入Cas9切割的基因组位点
鉴于可以通过增加供体 DNA 的局部丰度来增强 HDR 介导的精确编辑,而 CRISPEY 策略通过原位表达逆转录-gRNA 嵌合分子显示出在酵母基因组中的高效编辑。因此,该研究试图通过在 gRNA 的 5' 或 3' 端融合逆转录 ncRNA,即逆转录-ncRNA gRNA (rgRNA),对共价连接到 gRNA 的供体 msDNA 进行原位逆转录。该研究首先试图测试人类细胞中 msDNA 的相对丰度。该研究发现所有四个选定的 RT 都能够在人类细胞中表达 msDNA,并且与 5' rgRNA 相比,retron RT 与 3' rgRNA 的结合显示出更高的 msDNA 表达。结果表明,retron RT 在人类细胞中具有逆转录功能。
接下来,该研究探索了逆转录编辑在人类 HEK293T 细胞中的潜力。为了确定 EMX1 和 HEK3 的逆转录编辑介导的 HDR 效率,该研究进行了深度测序。在测试的四个逆转录子中,Ec86、Ec73 和 Ec107 实现了不同程度的精确编辑,并且 Ec73 与 CRISPR-Cas9 结合显示出最高的活性,高达 10%。总之,该研究结果表明 Cas9-Ec73 RT 融合与 3' Ec73 rgRNA 结合可用于人类细胞中有效的精确基因组编辑。此外,该研究检查了与 EMX1 基因座相关的四个报告的 CRISPR-Cas9 脱靶位点,以确定逆转录编辑的脱靶效应。尽管带有 rgRNA 的 Cas9-Ec73RT 在目标位点诱导的插入缺失率与带有 sgRNA 的 Cas9 相似,但带有 rgRNA 的 Cas9-Ec73RT 在四个已知的脱靶位点显示活性降低。
可以采取许多方法来改善人类细胞中的逆转录编辑。首先,鉴定更适合人类细胞基因组编辑的逆转录子。其次,retron-RT 和retron-ncRNA 的工程进化可以用来增强retron 介导的ssDNA 细胞内生产。最后,有证据表明与 Cas9 (D10A) 切口酶 (RDN) 融合的 hRAD51 突变体可以在没有 DSB 的情况下介导精确的基因组编辑。由于消除了 Cas9 诱导的 DSB,可以预期逆转录与 RDN 的组合可能使逆转录编辑更加准确和安全。
该研究由辉大生物科技有限公司研发部孔祥锋博士和脑智卓越中心汪子康博士、张仁霞博士研究生等在杨辉博士的指导下完成。辉大生物科技有限公司研发部施霖宇博士、王兴博士和脑智卓越中心周英思博士对该研究做出了重要贡献。
参考消息:
https://link.springer.com/article/10.1007%2Fs13238-021-00862-7



























