突破!上海交通大学迎来2024年首篇JAMA(IF=121)
辅助和新辅助免疫治疗改善了早期非小细胞肺癌(NSCLC)患者的临床结果。然而,检查点抑制与化疗的最佳组合仍然未知。
2024年1月16日,上海交通大学陆舜团队在国际知名医学期刊JAMA (IF=121)在线发表题为“Perioperative Toripalimab Plus Chemotherapy for Patients With Resectable Non–Small Cell Lung Cancer,The Neotorch Randomized Clinical Trial”的研究论文,该研究的目的是探讨与单独化疗相比,toripalimab联合铂基化疗是否能改善II期或III期可切除NSCLC患者的无事件生存期和主要病理反应。该随机临床试验于2020年3月12日至2023年6月19日在中国50家参与试验的医院招募了II期或III期可切除NSCLC(非鳞状NSCLC无EGFR或ALK改变)患者。该中期分析的数据截止日期为2022年11月30日。患者按1:1的比例随机接受每3周一次240mg的toripalimab或安慰剂联合铂类化疗,术前1个周期,术后1个周期,随后每3周一次toripalimab(240mg)或安慰剂,长达13个周期。
主要结局是无事件生存期(由研究者评估)和主要病理反应率(通过盲法、独立病理审查评估)。次要结局包括病理完全缓解率(通过盲法、独立病理审查评估)和不良事件。该研究发现,在围手术期化疗中加入toripalimab可显著改善可切除的III期NSCLC患者的无事件生存率,并且该治疗策略具有可管理的安全性。

在非小细胞肺癌(NSCLC)患者中,30%的患者最初诊断为可切除的疾病。早期NSCLC患者的主要治疗方法是手术切除,II期或III期NSCLC患者的5年无病生存率约为40%。非小细胞肺癌复发后,5年总生存率为2%-13%。
术后辅助化疗已被证明可以延长可切除非小细胞肺癌患者的生存期。IMpower010研究显示,与单独辅助化疗相比,辅助化疗后使用atezolizumab维持治疗的II至IIIA期非小细胞肺癌患者的无病生存期显著延长,这些患者的肿瘤在1%或更多的肿瘤细胞上表达程序性细胞死亡配体1 (PD-L1)。同样,PEARLS/KEYNOTE-091研究表明,在IB至IIIA期非小细胞肺癌和任何水平的PD-L1表达的患者辅助化疗后,使用派姆单抗维持治疗的无病生存获益。
在转移性非小细胞肺癌患者中,免疫检查点阻断剂联合化疗可提高总生存率,因此已成为转移性非小细胞肺癌患者的标准一线治疗。CheckMate 816研究显示,与单独化疗相比,在新辅助化疗中加入纳武单抗也显著提高了IB至IIIA期NSCLC患者的无事件生存率。

截至2022年11月30日的主要和次要结果(图源自JAMA )
随机临床试验评估了可切除的非小细胞肺癌患者围手术期检查点抑制作用。2期NADIM II随机临床试验显示,与单独化疗相比,围手术期加用nivolumab具有更高的病理完全缓解率和生存率。在KEYNOTE-671研究中,与单独接受化疗的患者相比,在新辅助化疗中加入派姆单抗和辅助派姆单抗可显著改善II期至IIIB期NSCLC患者的无事件生存率。同样,在AEGEAN试验中,与单独化疗相比,围手术期durvalumab联合化疗显著提高无事件生存期和病理完全缓解率。然而,检查点阻断剂在新辅助和辅助治疗阶段联合化疗的最佳策略,以及最佳治疗持续时间仍然未知。

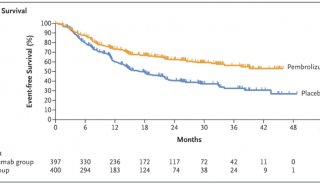
无事件生存率和总生存率(图源自JAMA )
特瑞普利单抗(torpalimab)是一种人源IgG4K单克隆抗体,抗人PD-1,在中国被批准作为转移性非鳞状NSCLC的一线联合化疗药物,有6个已批准适应症,并于2023年10月被美国食品和药物管理局批准用于晚期鼻咽癌的治疗。Neotorch是一项随机、双盲、安慰剂对照的3期试验,评估Torpalimab联合围手术期铂基化疗与单独化疗对可切除的II期或III期NSCLC患者的疗效和安全性。本文报道了预先指定的III期NSCLC患者无事件生存期的中期分析。
在501例随机分组的患者中,404例为III期NSCLC(Torpalimab+化疗组202例,安慰剂+化疗组202例),97例为II期NSCLC,被排除在中期分析之外。中位年龄62岁(IQR, 56~65岁),92%的患者为男性,中位随访时间为18.3个月(IQR, 12.7~22.5个月)。对于无事件生存的主要结局,Torpalimab组的中位长度不可估计(95% CI, 24.4个月-不可估计),而安慰剂组的中位长度为15.1个月(95% CI, 10.6-21.9个月)(风险比,0.40 [95% CI, 0.28-0.57], P < .001)。
torpalimab组的主要病理反应率(另一个主要结局)为48.5% (95% CI, 41.4%-55.6%),而安慰剂组为8.4% (95% CI, 5.0%-13.1%)(组间差异为40.2% [95% CI, 32.2%-48.1%], P < .001)。torpalimab组病理完全缓解率(次要结局)为24.8% (95% CI, 19.0%-31.3%),安慰剂组为1.0% (95% CI, 0.1%-3.5%)(组间差异为23.7% [95% CI, 17.6%-29.8%])。免疫相关不良事件的发生率在torpalimab组中更为频繁。未发现与治疗相关的意外毒性作用。3级或以上不良事件、致命不良事件和导致停止治疗的不良事件的发生率在两组之间具有可比性。总之,该研究发现,在围手术期化疗中加入toripalimab可显著改善可切除的III期NSCLC患者的无事件生存率,并且该治疗策略具有可管理的安全性。
-
科技前沿
-
产品技术

-
焦点事件















