首创GLP-1拮抗剂avexitide斩获美国FDA突破性药物资格
Eiger是一家临床阶段的生物制药公司,致力于加速开发和商业化治疗罕见病及超级罕见病的靶向疗法。近日,该公司宣布,美国食品和药物管理局(FDA)已授予avexitide(前称:exendin 9-39)治疗减肥术后低血糖症(post-bariatric hypoglycemia,PBH)的突破性药物资格(BTD)。值得一提的是,此次BTD也是Eiger公司管线项目在美国FDA方面被授予的第3个BTD。
avexitide是一种靶向、首创的GLP-1拮抗剂,目前正开发作为一种方便的、新颖的液体制剂,通过皮下注射给药治疗PBH。PBH是一种慢性疾病,发生在减肥手术后的患者中,导致餐后血糖水平极低。严重的PBH发作可导致精神状态改变、意识丧失、癫痫发作和昏厥。由于病态肥胖发病率的增加,减肥手术的数量也在增加,导致患PBH的患者数量也在增加。目前,尚无批准治疗PBH的药物,该领域对有效治疗药物存在着迫切且显著的未满足医疗需求。
BTD是FDA在2012年创建的一个新药评审通道,旨在加快开发及审查用于治疗严重或威及生命的疾病并且有初步临床证据表明该药与现有治疗药物相比能够实质性改善病情的新药。获得BTD的药物,在研发时能得到包括FDA高层官员在内的更加密切的指导,保障在最短时间内为患者提供新的治疗选择。
Eiger公司总裁兼首席执行官David Cory表示:“我们的avexitide PBH临床项目在4项II期临床研究中已对54例PBH患者进行了治疗,包括住院治疗和门诊治疗,结果显示治疗PBH具有非常好的疗效。我们期待与FDA就目前正在推进的3个突破性药物项目继续合作,包括lonafarnib治疗丁型肝炎病毒(HDV)感染、lonafarnib治疗早年衰老综合症(Progeria,早衰症)、avexitide治疗PBH。”
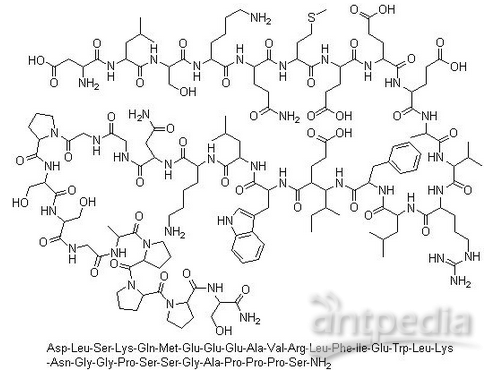
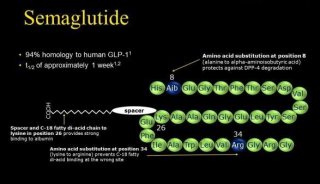
avexitide:艾塞那肽的31个氨基酸片段(图片来源:Eiger公司)
在美国,每年大约开展15万-20万例减肥外科手术,在欧洲每年开展10万例。据估计,在美国和欧盟分别有3万例和2.5万例PBH患者。随着治疗肥胖及相关并发症的减肥外科手术数量的增加,经历PBH的患者数量也在增加,其症状通常在手术后一年或多年出现。PBH在减肥术后患者中的病情严重程度变化很大,轻度至中度低血糖主要通过膳食碳水化合物限制来加以控制,而重度低血糖会导致对饮食改变无反应的神经糖代谢结局(精神状态改变、意识丧失、癫痫发作、昏迷)。严重的PBH可能对患者的生活质量产生显著的负面影响。目前尚无批准治疗PBH的药理学疗法。
胰岛素是机体所分泌用于控制高血糖的主要生理激素,胰岛素分泌的异常增加可导致严重的低血糖症,该病可导致严重的并发症,包括癫痫发作、脑损伤和昏迷。胰高血糖素样肽-1(GLP-1)是一种胃肠(道)激素,在餐后从肠道L细胞释放出来。GLP-1结合至胰腺β细胞上的GLP-1受体并增加胰岛素的释放。在PBH患者中,GLP-1介导的胰岛素分泌被功能失调地放大。
avexitide是一种含有31个氨基酸的肽段,选择性靶向和阻断GLP-1受体,使胰腺胰岛素分泌正常,从而减少餐后低血糖症。avexitide是一种新型的PBH治疗方法。在欧盟,avexitide已被授予治疗非胰岛素瘤性胰岛源性低血糖综合征(NIPHS)的孤儿药资格;在美国,avexitide已被授予治疗高胰岛素性低血糖血症的孤儿药资格。这2种广泛的定义中都包括PBH。
原文出处:Eiger Announces Breakthrough Therapy Designation Granted by FDA for Avexitide for Treatment of Post-Bariatric Hypoglycemia (PBH)