Science :以菌治瘤
尽管嵌合抗原受体(CAR)-T细胞在治疗血液恶性肿瘤方面已取得显着成功,但实体瘤的有效靶向作用仍然有限。与血液恶性肿瘤细胞普遍表达抗原靶标CD19不同,实体瘤上的肿瘤相关抗原具有异质性和缺乏特异性的特点,一方面靶向治疗的选择压力会引起抗原阴性复发,使不表达目的抗原的癌细胞持续增殖,另一方面会导致CAR-T细胞误伤健康组织,且T细胞的浸润性较差。研究表明细菌可以选择性地定殖于免疫豁免肿瘤核心,并能在缺氧的微环境下生存,一些小组便利用携带特定“货物”的工程菌作为瘤内生物反应器,虽然对于大量实体瘤患者而言是安全的,但还未在临床试验中证实其有效性。
近日,来自哥伦比亚大学的Tal Danino团队在Science杂志上发表了一篇题为 Probiotic-guided CAR-T cells for solid tumor targeting 的文章,他们开发了一个益生菌引导的CAR-T细胞 (ProCAR) 系统,简而言之,可定植于肿瘤的益生菌释放能被CAR-T细胞识别的靶标以标记肿瘤组织,募集CAR-T细胞进而诱发原位裂解,该系统已在人类和小鼠癌症的多种异种移植和同源模型中证明是安全有效的。此外,他们还进一步设计了多功能益生菌,可释放趋化因子以增强CAR-T细胞的募集和治疗反应,展示了工程细菌作为CAR-T细胞疗法辅助装置的强大效力。

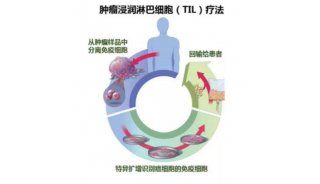
CAR-T难以对付实体瘤的一个主要原因就在于瘤上的肿瘤相关抗原(TAA),为了创建一个不依赖于TAA的CAR-T系统,作者改造了大肠杆菌Nissle1917(EcN),简而言之,在该系统中,EcN可以在肿瘤微环境(TME)中增殖至临界密度后裂解释放CAR靶标(ProTag)至胞外空间,该靶标包含一个可结合肿瘤细胞外基质(ECM)的肝素结合域(heparin binding domain, HBD)以标记肿瘤,同时包含一个可被工程改造后的CAR-T细胞识别的GFP蛋白(定义为GFP CAR-T 细胞, GFP28z),从而实现在抗原未知的情况下对肿瘤的追踪(下图)。

图1. EcN介导的CAR-T靶向杀伤肿瘤示意图。
在体外测试中,该系统表现出对人类不同癌细胞系的细胞毒性,为了测试其在体内的效果,作者在递送GFP CAR-T细胞48小时前,对荷瘤免疫缺陷(NSG)小鼠单次瘤内注射携带ProTag的或对照菌株,仅ProTag菌株能介导有效的抗肿瘤反应,显著减缓肿瘤生长并提高小鼠生存率,且未产生明显副作用。人类三阴性乳腺癌(TNBC)由于缺乏雌激素和孕激素受体及HER2表达,对现有的靶向疗法没有反应,为了进一步评估ProCAR系统对抗原的不依赖性,作者测试了其在人类TNBC小鼠模型中的疗效,该系统实现了持久的抗肿瘤功效,植入后70天没有观察到肿瘤生长,此外,在另一皮下接种SKOV3肿瘤的小鼠模型中也观察到类似表现。
尽管已证明ProCAR系统对免疫功能缺陷小鼠肿瘤抑制有效,但在功能性免疫系统背景下的效果却未知。为此,作者在携带皮下结直肠癌的免疫活性小鼠中进一步测试该系统,向肿瘤注射ProTag菌株后注射自体GFP CAR-T细胞,同样能产生显著的抗肿瘤功效。通过对肿瘤及肿瘤引流淋巴结分离的细胞进行免疫表型分析发现,CD69在肿瘤浸润性CD8+和CD4+T细胞上的表达显著增加,且激活的CD40+ MHCII+单核细胞频率增加,提示瘤内益生菌和活化的CAR-T细胞之间合作可以增强宿主免疫反应,最终带来全身性抗肿瘤益处。在此基础上,该团队构建了一株能释放人CXCL16(驱动T细胞迁移的趋化因子)激活突变体(CXCL16K42A)的菌株(ProCombo),并在荷瘤小鼠体内验证了该菌株对T细胞的募集能力及新系统对肿瘤的控制效果,且不会引起额外的肿瘤外毒性迹象。总的来说,这项工作证明经改造的益生菌与CAR-T细胞合作可以实现不依赖于肿瘤相关抗原的肿瘤靶向和抑制效果。
针对这项研究,来自美国波士顿大学的Eric M. Bressler和Wilson W. Wong在同期杂志上发表了题为Engineered bacteria guide CAR T cells to tumors-T cells and bacteria are engineered to work together to find and destroy tumor cells 的观点文章,他们指出与小鼠相比,人类对内毒性更为敏感,尽管有研究表明静脉注射减毒鼠伤寒沙门氏菌是安全的且能实现肿瘤定植,但在高剂量下会出现菌血症和其他毒性。因此,ProCAR 系统向临床转化的一个关键问题在于在不破坏细菌活力和肿瘤定植的前提下规避革兰氏阴性细菌的潜在毒性。此外,需要注意的是,人类肿瘤的尺寸往往比小鼠肿瘤大20至40倍,未来的研究将需要确认ProTag在不同尺寸肿瘤中的扩散距离。总体来说,这项工作是治疗异质性“冷”肿瘤潜在方法的重要概念验证。

原文链接:
http://doi.org/10.1126/science.add7034