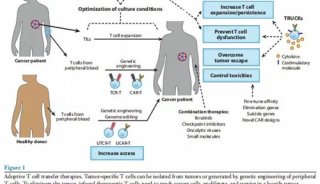
TIL疗法:抗实体瘤“黑马 ” 为攻克多种癌症“加速”
回顾全球药物研发历史,有着明显的时代印记:上世纪50-60年代是“抗生素”;上世纪80-90年代是“慢病药”;而进入21世纪以来,“抗癌药”逐渐走向舞台中央。
今年6月22日,中国首款CAR-T细胞治疗产品获批上市,这也是中国首款获批上市的细胞药物。但是CAR-T细胞治疗产品在应用上却有一定的局限性,目前CAR-T主要应用在血液瘤治疗上,在实体瘤应用上仍没有有效的产品。在这样的背景下,基于肿瘤浸润淋巴细胞的TIL疗法,凭借对抗实体瘤展现出的巨大优势站在了舞台的聚光灯下。目前,全球已有多家企业开始“重金”布局,且已取得积极结果。
何为TIL疗法?
TIL,即肿瘤浸润淋巴细胞,是一种从肿瘤组织中分离出的浸润淋巴细胞。这些淋巴细胞中有一部分是针对肿瘤特异性突变抗原的T细胞,是可以深入到敌军内部、打击能力最强的免疫细胞,被认为是一种机体对肿瘤细胞的特异性免疫反应。
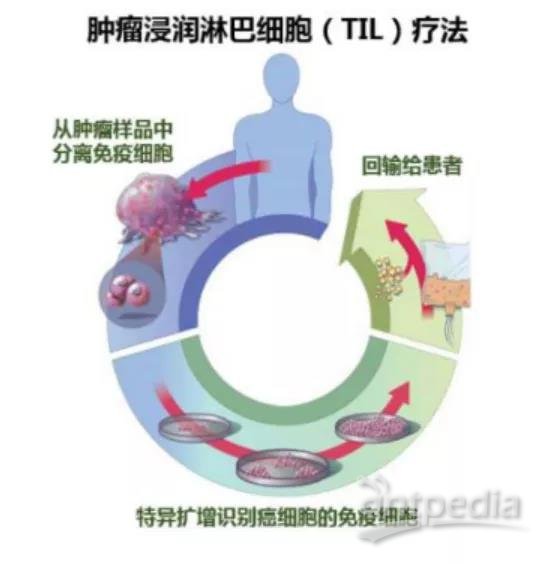
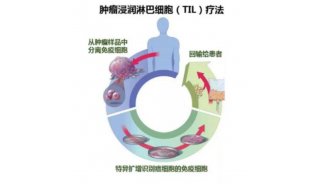
研究发现,肿瘤患者体内的氧气和重要的营养物质会被肿瘤剥夺从而导致TIL细胞进入衰竭状态。而TIL疗法,就是从肿瘤组织中分离出肿瘤浸润的淋巴细胞,在体外培养和大量扩增后回输到病人体内的疗法,通过激活并增援这支“沉睡的军队”,重新“唤醒”免疫系统来清除肿瘤。TIL细胞疗法被认为是当前实体瘤免疫治疗领域最具竞争力和产业化潜力的技术方向之一。
TIL疗法具体过程
TIL疗法有什么神奇之处?
与CAR-T疗法相比,TIL细胞疗法无需经过工程化将CAR转入T细胞中使其具有特异性靶向肿瘤细胞能力,只需要筛选出特定突变的免疫细胞,然后在体外扩增并回输给患者,大大降低了治疗成本。
此外,TIL细胞疗法还具有以下优势:
1.肿瘤浸润性好:本身来自肿瘤,具有合适的趋化因子受体系统,回输后可更好地浸润肿瘤组织;
2.肿瘤特异性强:TIL是非选择的肿瘤特异性杀伤T细胞,靶向多种肿瘤抗原,可克服肿瘤异质性问题;
3.安全性高:经过体内选择,绝大多数TIL仅特异性识别肿瘤抗原,而不识别正常组织,具有良好的安全性。
如此看来,TIL疗法当真可以配的上是抗实体瘤界的“黑马”!
TIL疗法发展的“前世今生”

Steven A. Rosenberg博士(图片来源:Wikipedia)
上世纪80年代后期,美国国家癌症研究所NCI的医学博士Steven A.Rosenberg等人首次发现了TILs可以抑制患者体内的恶性黑色素瘤细胞的转移能力。2012年,肝内胆管癌晚期患者Melinda Bachini成为了TIL治疗后第一位CR(完全缓解)的患者。
2016年末,Rosenberg研究组从患者肺部肿瘤结节(结直肠癌细胞扩散到肺部形成肺转移)中分离出了靶向KRAS G12D突变后新抗原的TIL细胞,扩增回输后使得肿瘤消退。TIL疗法依赖于突变,而不是癌症类型。这一研究为T细胞受体基因疗法治疗表达这一共同突变的多种癌症类型带来了可能。
剑指多种实体瘤 国内外药企争夺“首发”
据不完全统计,目前全球已有多款在研TIL疗法,正在开展针对转移性黑色素瘤、鼻咽癌、头颈部鳞状细胞癌、胆管癌、复发性或难治性卵巢癌、骨肉瘤、宫颈癌、卵巢癌、非小细胞肺癌、脑胶质瘤、胸膜间皮瘤等多种实体瘤的临床试验。
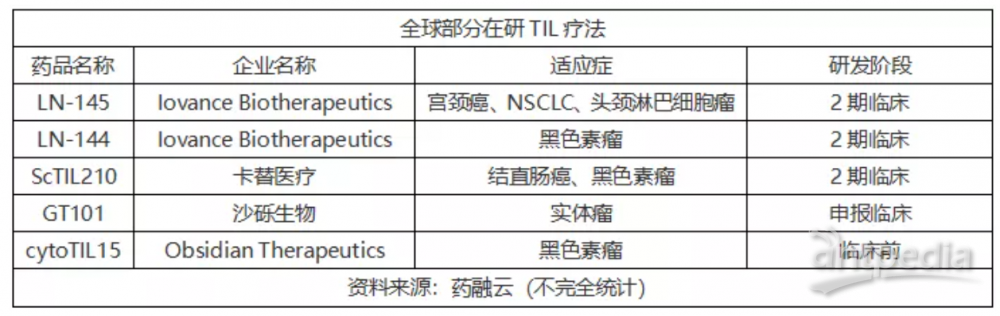
部分在研TIL疗法
舍巴医疗中心
以色列舍巴医疗中心Sheba Medical Center是全球唯一一家FDA批准的,为顽固性卵巢癌患者提供TIL临床实验的医院。其下属的Ella Lemelbaum Institute免疫肿瘤学研究中心正在开展一项利用TIL自体免疫疗法治疗晚期或转移性卵巢癌的突破性临床实验。
Iovance Biotherapeutics
2011年,Iovance与NCI签订合作研发协议,从Rosenberg团队引进TIL技术,通过对TIL的生产工艺进行简化、规模化,以开发出可以商业化的TIL细胞治疗产品。IovanceBiotherapeutics的 lifileucel(LN-144)和LN-145进展较快,目前处于2期临床。其中Lifileucel(LN-144)联合PD-1单抗Pembrolizumab治疗多种实体瘤取得积极结果:针对宫颈癌,ORR(客观缓解率,指肿瘤缩小达到一定量并且保持一定时间的病人的比例)为50.0%(5/10);针对转移性黑色素瘤患,ORR为87.5%(7/8)。
LN-145二期临床试验(IOV-COM-202)的3B队列临床数据显示,在治疗的28例晚期转移性非小细胞肺癌(mNSCLC)患者中,24例患者接受过二线以上系统治疗,且所有患者之前均接受过PD-1/PD-L1免疫治疗。在用LN-145单药治疗一次后,客观缓解率(ORR)为21.4%(n=28,1例CR和5例PR),12例疾病稳定,疾病控制率(DCR)达64.3%。
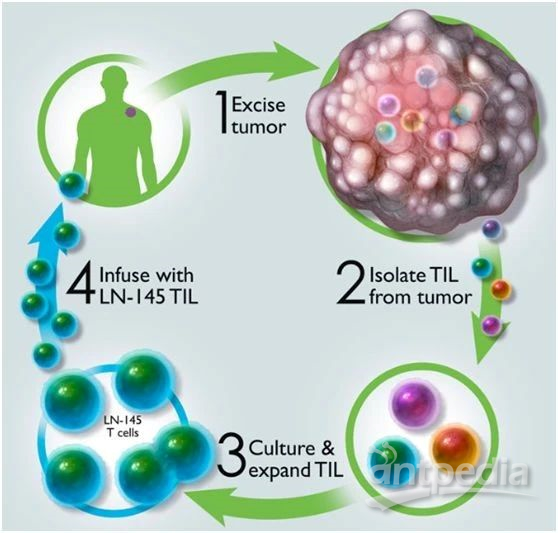
LN-145疗法机理(图片来源:Iovance公司官网)
在规模化生产方面,2019年5月底,Iovance投资7500万美元在费城建立一个13.6万平方英尺的设施(计划于2021年完工)。通过提升内部生产能力,降低运营成本,以扩大其自体TIL产品的商业化生产。同时,扩大与药明康德先进治疗业务部门(WuXi Advanced Therapies Unit)的合作关系,提高innovaTIL-01和innovaTIL-04的研究、生产能力。
西比曼CBMG
2018年10月,西比曼与NCI签订了专利许可协议,成为首家获得NCI授权的中国企业。西比曼将利用NCI获得的非独家、可再次授权的全球性许可,用于下一代新抗原反应性肿瘤浸润淋巴细胞(TIL)疗法的研发、生产以及商业化,用以治疗多种癌症。
2019年,西比曼计划在美国和中国启动TIL在非小细胞肺癌(NSCLC)和其他实体肿瘤中的Ⅰ期临床研究。
北京卡替医疗Chineo Med
ScTIL210,是卡替医疗在传统TIL疗法基础上开发的第四代TIL,无需借助手术组织获取TIL细胞,而是从外周血采集单核细胞,分离肿瘤识别性T细胞——从而大大提升了治疗实施的便捷性,提升其克服肿瘤微环境和增加自我扩增的能力。此外,卡替医疗拥有专利技术增强型肿瘤浸润淋巴细胞(Enhanced TIL)疗法与超级TIL(Super TIL)疗法,将制备周期缩短至5-15天。
超级TIL(Super TIL)疗法是利用辅助性手术获得肿瘤组织,将分离提取的TIL转染免疫检查点-共刺激分子的反向转换和扩增分子后,使得TIL获得了攻克肿瘤微环境障碍的能力,以及在体内近乎无限复制扩增的能力的功能超级增强后的细胞,并凭借TIL对肿瘤的天然的特异识别性,从而同时解决肿瘤识别、克服微环境和高效扩增的三大难题,实现强效抑癌效果。
沙砾生物
GT-101是一款基于患者自体TIL的细胞药物,通过从患者体内获取肿瘤组织并提取TIL,再经过沙砾生物特有的StemTexpTM生产平台扩增至10亿量级后输注回患者体内以对抗肿瘤。沙砾生物预计GT101将于2022年初在中国提交IND申请。
Obsidian
cytoTIL15是Obsidian的先导cytoTIL项目,目前处于临床前开发阶段,用于治疗转移性黑色素瘤和其他实体瘤。其独特之处是使用基因工程,让TIL细胞表达与细胞膜结合的IL-15。这种TIL细胞输入患者体内后不再需要患者接受IL-2的治疗,在提高TIL疗法持久性的同时降低了疗法的毒副作用。而且,使用该公司独特的cytoDRiVE技术, IL-15的表达水平受到FDA批准的小分子药物的控制,提高了疗法的安全性。
此外,多家企业已最大力度地先后完成多次融资以确保TIL疗法研发顺利开展。ObsidianTherapeutic于今年10月完成1.15 亿美元B轮融资;卡替医疗于今年2月完成亿元Pre-B轮融资,10月完成逾亿元Pre-B补充轮融资;君赛生物于2020年2月完成数千万元人民币Pre-A轮融资;沙砾生物于2020年12月完成超过1亿人民币的A轮融资,2021年7月又完成A+轮融资;西比曼生物于今年9月完成1.2亿美元的A轮融资。
TIL疗法尚存局限
作为一种高度差异化、定制化和靶向性的免疫疗法,TIL疗法在有效性、安全性和可及性方面仍存在一定的局限性:
1、能提取淋巴细胞的肿瘤样本难获得;
2、具有抗肿瘤活性、增值能力强的TIL细胞难获得;
3、TIL会被肿瘤微环境抑制;
4、无法保证回输的T细胞在体内能存足够的时间;
5、涉及多种系统用药、回输后副反应的管理;
6、TIL细胞的体外扩增缺乏标准流程,现有操作程序成本高、耗时长。
展望——距离第一款TIL疗法产品上市已“近在咫尺”
任何一种新的治疗策略的研发过程都不是一帆风顺的,在TIL疗法的发展历程中,质疑和争议始终伴随左右。作为一种高度差异化、定制化和靶向性的免疫疗法,除了居高不下的成本,研究者仍面临着技术、安全性甚至规章制度等方面的障碍,需要更多的、进一步的实验室和临床研究来切实优化TIL这一免疫治疗策略。不过该疗法已在全球范围内开展了多项各类肿瘤临床试验,显示出了可喜的试验结果,距离第一个TIL疗法上市已“近在咫尺”,相信在不久的将来,我们就能看到该疗法的出现在选择项目表上。
参考资料:
[1]https://mp.weixin.qq.com/s/XK8_uTdJ6bQ9HPmmEHRq9A
[2]https://m.chunyuyisheng.com/m/topic/493236/
[3]https://www.iovance.com/clinical/immunotherapy-for-solid-tumors/
[4]http://care.39.net/a/210910/9429588.html
[5]https://www.sohu.com/a/333746755_120060272
[6]https://zhuanlan.zhihu.com/p/359627865
[7]https://www.iyiou.com/news/202102261014869
-
科技前沿
-
科技前沿