液相色谱仪液体样品预处理技术--固相萃取仪器结构、操作
自1970年发明固相萃取技术以来,其发展非常迅猛,出现了多种形式的萃取装置,包括SPE柱(SPE cartridge)、尖形SPE管(SPE pipette tip)、SPE盘(SPE disk)以及SPE板(SPE plate)等。
SPE柱(如图1所示)的使用最为普遍,简单的SPE柱就是一根直径为数毫米的小玻璃柱,或用聚丙烯、聚乙烯、聚四氟乙烯等塑料或不锈钢制成的柱子。柱下端有一孔径为20μm的烧结筛板,用以支撑吸附剂。在筛板上填装一定量的吸附剂,然后在吸附剂上再加一块筛板,以防止加样品时破坏柱床。基于对纯度的考虑,一般选用无添加剂且含有微量杂质的医用聚丙烯作为柱体材料,以免在萃取过程中污染试样。为了降低SPE空白中的杂质,可选用玻璃、纯聚四氟乙烯作为柱体材料。筛板材料是另一可能的杂质来源,制作筛板的材料有聚丙烯、纯聚四氟乙烯、不锈钢和钛等。金属筛板不含有机杂质,但易受酸的腐蚀。由于柱体、筛板和填料都可能向试样中引进杂质,因此在建立和验证SPE方法时,必须做空白萃取实验。
SPE的另一种形式是SPE盘(如图2所示),外观上与膜过滤器十分相似。盘式萃取器是含有填料的纯聚四氟乙烯圆片,或载有填料的玻璃纤维片。填料占SPE盘总量的60%~90%,盘的厚度约1mm。SPE柱和盘式萃取器的主要区别在于床厚度与直径之比,对于等重的填料,盘式萃取的截面积比柱式萃取大10倍左右,因而允许液体样品以较高的流量流过。
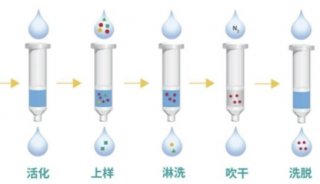
当所需处理的样品量较大时,如医药中间体的回收等,可采用板式SPE的固相萃取装置。图3给出了SPE板的结构,上下两块板上装有多个SPE小柱,待处理的液体依靠重力、压力、真空或离心力的作用通过萃取板,同时在收集板上进行样品的收集。典型的固相萃取一般分为以下五个基本步骤:
①根据检测量的大小以及待检物质的化学、物理性质,选择合适的吸附柱。
②活化填料。有利于吸附剂和目标物质相互作用,提高回收率。一般采用甲醇来活化,另外甲醇还能起到除杂的作用。每一活化溶剂的用量为(1~2)m/100mg固定相。
③进样。使样品流经吸附柱并被吸附。为了保留分析物,尽可能使用最弱的样品溶剂,并允许采用大体积(0.5~1L)的上样量。
④冲洗。用水或者是适当的缓冲溶液对吸附柱进行冲洗,将杂质冲洗掉。通常冲洗溶剂体积为0.5~0.8ml/100mg固定相。⑤洗脱。选择适当的洗脱剂进行洗脱,收集洗脱液,然后进行浓缩、检验,或者是直接进行在线检测。洗脱溶剂用量一般为0.5~0.8ml/100mg固定相。

图1 SPE柱装置示意图

图2 SPE盘

图3 SPE板简图
固相萃取(solid phase extraction,SPE)是一下种由柱色谱发展而来的样品预处理技术,所用的填料粒径(>40μm)大于HPLC填料粒径(3~10μm)。SPE与HPLC的差别是柱压低、塔板数少、分离效率较低、一次性使用,因此只能分离保留性质有很大差别的化合物。由于SPE实现了选择性的提取、分离、浓缩三位一体的过程,操作时间短、样品量小、干扰物质少,因此可用于挥发性和非挥发性组分的预处理,并具有很好的重现性。
吸附剂是固相萃取的核心,吸附剂选用的好坏直接关系到能否实现萃取操作,以及萃取效率,同时新型吸附剂的研发也是固相萃取技术发展和应用的关键所在。早期的吸附剂多为活性炭、氧化铝等强吸附性材料。常用的固相吸附材料有正相、反相和离子交换吸附剂三种正相吸附剂主要包括硅酸镁、氨基、氰基、双醇基硅胶、氧化铝等,适用于极性化合物的萃取;反相吸附剂包括键合硅胶C18、键合硅胶C8、芳环氰基等,适用于非极性至一定极性化合物的萃取;离子交换吸附剂包括强阳离子吸附剂(苯磺酸、丙磺酸、丁磺酸等)和强阴离子吸附剂(三甲基丙基胺、氨基、二乙基丙基胺等),适用于阴阳离子型有机物的萃取。目前国内外已经研制出多种复合型吸附剂。聚合二乙烯苯-N-乙烯吡咯烷酮及其盐是一类性能独特的反相吸附剂,独有的亲水和亲脂性质保持其在水中湿润,能同时萃取极性物质和非极性物质。以氯甲基化的高分子树脂PS-DVB(苯乙烯-联苯乙烯共聚物)与二亚乙基三胺反应制成的新型的阴离子交换聚合树脂能同时萃取离子型和非离子型化合物;将碳化吸附剂与PS-DVB合用,能同时萃取强极性化合物和离子型化合物;将未封尾的C18硅胶与单官能团的C18硅胶混合,可以扩大C18柱的极性范围。
免疫亲和型吸附剂是基于抗体抗原相互作用的原理而研制出来的新型固相吸附剂。首先备一种专属性的抗体,然后将其固定在琼脂糖或硅胶上,当样品通过吸附床层时发生抗原-抗体结合,从而专属性地将目标组分分离出来。这种吸附剂是目前已知选择性最强的固定吸附剂。近年来,这种吸附剂越来越多地被应用于医学、生物学以及环境分析等领域。分子印迹型吸附剂是一类新型的高选择性吸附剂,能从复杂的生物基质中选择性地提取出微量分析物。表1中给出了常用的SPE固定相及应用条件。
表1 SPE固定相及应用条件
分离机制 | 典型固定相 | 被到物类型 | 装载溶剂 | 洗脱溶剂 | |
正相 | 吸附 | 硅胶,氧化铝,硅酸镁 | 弱至中等极性 | 低P'(己烷,CHCI3) | 高P'(如甲醇,乙醇) |
极性键合相 | 氰基,氨基,二醇基 | 中等至强极性 | 低P(己烷,CHCI3) | 高P'(如甲醇,乙醇) | |
反相 | (非极性键合相)疏水性 | 十八烷基硅氧烷 八烷基硅氧烷 | 疏水性强 (强非极性) | 高P'(如H2O,CH3OH/H2O,H3CN/H2O) | 低P'(已烷,CHCI3) |
疏水性中等 | 环己基,苯基,联苯基 | 中等非极性 | 高P'(如H2O,CH3OH/H2O,H3CN/H2O) | 中等P'(如二氯甲烷,乙酸乙酯) | |
疏水弱 | 丁基,乙基,甲基 | 弱极性至中等非极性 | 高P'(如H2O)至中等P'(如乙酸乙酯) | 高P'(如乙腈,甲醇) | |
阴离子交换弱 | 氨基,1',2'氨基 | 离子(可电离),酸性 | 水或缓冲液(pH=pKa+2) | (A)缓冲液(pH=pKa-2) (B)使吸附剂与被测物pH为中性 (C)高离子强度的缓冲液 | |
阴离子交换强 | 季铵 | 离子(可电离),酸性 | 水或缓冲液(pH=pKa+2) | (A)缓冲液(pH=pKa-2) (B)吸附剂与被测物pH为中性 (C)高离子强度的缓冲液 | |
阳离子交换弱 | 羧酸 | 离子(可电离),碱性 | 水或缓冲液(pH=pKa-2) | (A)缓冲液(pH=pKa+2) (B)吸附剂与被测物pH为中性 (C)高离子强度的缓冲液 | |
阳离子交换强 | 烷基磺酸,芳磺酸 | 离子(可电离),碱性 | 水或缓冲液(pH=pKa-2) | (A)缓冲液(pH=pKa+2) (B)使被测物pH为中性 (C)高离子强度的缓冲液 |
在固相萃取中,选择洗脱剂时首先应考虑其对固定相的适应性和对目标物质的溶解度,其次是传质速率的快慢。洗脱正相吸附剂吸附的目标组分时,一般选用非极性有机溶剂(如正己烷、四氯化碳等);洗脱反相吸附剂吸附的目标物质时,一般选用极性有机溶剂(如甲醇、乙腈、一氯甲烷等);对于离子交换吸附剂,常采用的洗脱剂是高离子强度的缓冲液。
为了提高回收率,洗脱剂多选用小分子有机溶剂,同时增大洗脱剂用量。这样可使吸附剂上的目标组分尽可能地被洗脱下来,但同时可能会引进一些杂质,给分析带来干扰。值得注意的是,以甲醇为洗脱剂洗脱树脂时,如果甲醇体积过大,则会引起树脂的充分溶胀,目标物质深入到树脂的内部间隙,很难再被洗脱,导致洗脱不完全,回收率降低。
在固相萃取过程中,应当注意以下影响因素。
①吸附剂的选择:实验时尽量选择与目标化合物极性相似的吸附剂,其用量大小与目标物性质(极性、挥发性)及其在水样中的浓度直接相关;吸附剂最好是多孔、比表面积大的固体颗粒,表面积越大,吸附能力越强,但是相应孔径会减小,应根据实际情况综合考虑;吸附剂必须具有较小的空白值,以减少吸附剂引起的污染和干扰;萃取吸附过程必须可逆并且具有较高的回收率,吸附剂必须能够快速地吸附分析物,并且能够在适当的溶剂条件下快速释放分析物,同时具有恒定的回收率,保证整个分析结果更加可靠、准确;吸附剂必须要具有很好的化学稳定性,具有较强的耐酸碱腐蚀能力,在各种淋洗剂条件下不会发生溶胀作用;吸附剂必须与样品溶液表面有很好的界面接触,只有样品与吸附剂表面充分接触才能够保证定量萃取。
②溶剂的选择:在固相萃取中,萃取固定相的活化、上样富集、淋洗杂质、分析物洗脱的过程中,都涉及溶剂的选择问题。溶剂选择最重要的是溶剂强度,这是保证固相萃取成功的关键表2给出了常见正相型和反相型固相萃取中有机溶剂的极性和强度大小关系。
表2 正相型和反相型固相萃取中常用溶剂的性质
极性 | 溶剂强度 | 溶剂 | 是否溶于水 | |
非极性
极性 | 强反相
弱反相 | 弱正相
强正相 | 正己烷 | 否 |
异辛烷 | 否 | |||
四卤化碳 | 否 | |||
三卤甲烷 | 否 | |||
二卤甲烷 | 否 | |||
四氢呋喃 | 是 | |||
乙醚 | 否 | |||
乙酸乙酯 | 差 | |||
丙酮 | 是 | |||
乙腈 | 是 | |||
异丙醇 | 是 | |||
甲醇 | 是 | |||
水 | 是 | |||
乙酸 | 是 |
对于固定相活化溶剂,一般先使用强的溶剂去除固定相上的杂质,然后选择与上样溶剂强度一致的活化溶剂,以保证样品能够在固定相上充分保留。需注意的是,固定相在活化过程和活化结束后都要保持湿润,否则会使固定相干裂或者进入气泡,导致柱效降低、回收率降低以及重现性变差。
对于上样溶剂的选择,要尽可能选择弱强度的溶剂,保证样品能够充分地保留在固相萃取柱上,还可以采用大量上样方法,提高富集倍数。如果上样溶剂强度过高,样品不能保留或者弱保留,则回收率低。
对于洗脱溶剂,要选择溶剂强度比较大的,保证保留在固定相上的样品洗脱下来,对大多数化合物来说,乙腈是一种比甲醇和乙醇更好的洗脱溶剂。另外,选择的洗脱溶剂要与后续的分析条件相适应。还有就是要选择黏度小、纯度高、毒性小并且不与样品和固定相发生反应以及不会干扰样品后续检测的溶剂。如果单一的洗脱溶剂效果不理想,也可考虑使用混合溶剂进行洗脱。
③固定相容量:在上样过程中,要注意样品的含量不要超过萃取柱容量,如果超过萃取柱容量,过量的样品不会在萃取柱上保留而丢失,导致回收率下降。
④流速控制:流速的控制对固相萃取至关重要,流速过大将引起萃取柱的穿漏,流速小则处理速度太慢。萃取柱预处理过程中流速适中,保证溶液充分湿润吸附剂即可,上样和洗脱过程则要求流速尽量慢些,以使分析物尽量保留在柱内或达完全洗脱,否则会导致分析物流失,影响回收率的大小。尤其是离子交换过程进行比较缓慢,应采用较低的流速(0.5~2.0ml/min)。