国家自然基金技术经验系列资料PCR技术及常见问题解决方案
技术原理
PCR技术又称聚合酶链反应(Polymerase Chain Reaction)技术,是一种在体外扩增核酸的技术。该技术模拟体内天然DNA的复制过程。其基本原理是在模板、引物、4种dNTP和耐热DNA聚合酶存在的条件下,特异扩增位于两段已知序列之间的DNA区段的酶促合成反应。每一循环包括变性、退火、延伸三步反应。每一循环的产物作为下一个循环的模板,如此循环30次。PCR技术的特异性取决于引物与模板结合的特异性。
实验用品
DNA模板(cDNA),5’primer 引物,3’primer 引物,dNTP ,Taq酶,酶的相应Buffer,双蒸灭菌水(pH8.0)。
实验步骤
1. 引物处理
(1)将装有引物的EP管 12000rpm 离心2min;
(2)向管中加入PH8.0的灭菌水,体积(µL)为10×nmol数, 稀释为100µM;
(3)实验时取5µM 引物,与 45µL双蒸灭菌水(PH8.0)混匀使用。
2. 反应体系(50µL)

3. 反应条件
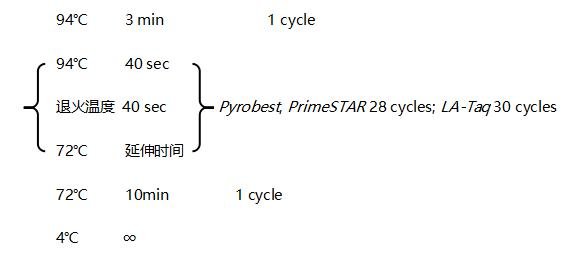
(1)体系中试剂按从多到少顺序加入PCR管中;
(2)94℃ 3 min后,中止PCR反应,迅速加入Taq酶,注意不要将枪头碰到PCR管壁,应迅速将枪头插入PCR管底部,不必按下枪,酶在热的环境中会自动进入反应液中;
(3)加完酶后迅速盖好PCR仪的盖子,继续反应。
4. 电泳检测
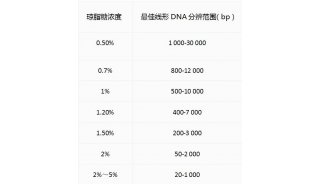
(1)依据目的基因分子量配制1%-2%琼脂糖凝胶;
(2)PCR产物中加6×loading buffer 10µL,混匀;
(3)混匀的sample加入胶孔中,115V 电压下电泳;
(4)buffer跑到凝胶位置一半附近时,停止电泳;
(5)将凝胶放在紫外成像系统中,观察目的条带。
PCR产物的非特异性扩增解决方案
1、假阳性
出现的PCR扩增条带与目的靶序列条带大小不一致,有时其条带更整齐,亮度更高。 原因可能是引物设计不合适。选择的扩增序列与非目的扩增序列有同源性,因而在进行PCR扩增时,扩增出的PCR产物为非目的性的序列。靶序列太短或引物太短,容易出现假阳性。
解决对策
重新设计引物
2、非特异性扩增带
指 PCR扩增后出现的条带与预计的大小不一致,或者同时出现特异性扩增带与非特异性扩增带。非特异性条带的出现,原因包括:一,引物与靶序列不完全互补、或引物聚合形成二聚体。二,镁离子浓度过高、退火温度过低,PCR循环次数过多。而且,酶量过多有时也会出现非特异性扩增。
解决对策
①必要时重新设计引物
②减低酶量或调换另一来源的酶
③降低引物量,适当增加模板量,减少循环次数
④适当提高退火温度或采用降落PCR
3、片状拖带或涂抹带
PCR扩增有时出现涂抹带或片状带或地毯样带。其原因往往由于酶量过多或酶的质量差,dNTP浓度过高,Mg2+浓度过高,退火温度过低,循环次数过多引起。
解决对策
①减少酶量,或调换另一来源的酶
②减少dNTP的浓度
③适当降低镁离子浓度
④增加模板量,减少循环次数
PCR污染解决方案
PCR反应的最大特点是具有较大扩增能力与极高的灵敏性,但令人头痛的问题是易污染,极其微量的污染即可造成假阳性的产生。
污染原因
(1)样本间交叉污染:样本污染主要有收集标本的容器被污染,或样本放置时,由于密封不严溢于容器外,或容器外粘有样本而造成相互间交叉污染; 样本核酸模板在提取过程中,由于吸样枪污染导致标本间污染;
(2)PCR试剂的污染:主要是由于在PCR试剂配制过程中,由于加样枪、容器、双蒸水及其它溶液被PCR核酸模板污染。 一个好的实验室,要时刻注意污染的监测,考虑有无污染、是什么原因造成的污染,以便采取措施,防止和消除污染。
解决对策
(1)操作时不慎将样品或模板核酸吸入枪内或粘上枪头是一个严重的污染源。加样或吸取模板核酸时要十分小心,吸样要慢,吸样时尽量一次性完成,忌多次抽吸;
(2)预混和分装PCR试剂:所有的PCR试剂都应小量分装,-20℃保存以减少重复加样次数,避免污染;
(3)操作人员使用一次性手套、吸头、小离心管一次性使用;
(4)减少PCR循环次数,只要PCR产物达到检测水平就可以。
-
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章
-
厂商文章







