项目文章STTT(IF 38)| 四川大学雷鹏教授团队利用脂质组+蛋白组揭示凝血酶调控卒中引起的神经元铁死亡机制

缺血性卒中对人类来说是一种严重的疾病风险,尤其在老龄化人群中尤为显著。以往的干预治疗方式只能通过去除血栓来实现,并且对于缺血性卒中后神经元死亡的机制仍存在争议。在以往的研究中,铁死亡越发被认为是各种器官缺血后细胞程序性死亡的一种机制。代谢组学的发展,尤其脂质组学技术的进步,为了解铁死亡中脂质过氧化导致的程序性细胞坏死的过程提供有力的技术支撑,也是科研研究热点之一。
近期,来自四川大学生物治疗国家重点实验室的雷鹏教授研究团队在Signal Transduction and Targeted Therapy(IF 38.104)上发表题为“Thrombin induces ACSL4-dependent ferroptosis during cerebral ischemia/reperfusion”的文章,该研究采用多组学方法确定了凝血酶和ACSL4基因/蛋白及其亲铁性磷脂酰乙醇胺脂质产物,在啮齿类动物大脑中动脉闭塞处显著改变,并揭示凝血酶-ACSL4轴可能是改善缺血性卒中期间铁死亡神经元损伤的关键治疗靶点。

研究材料
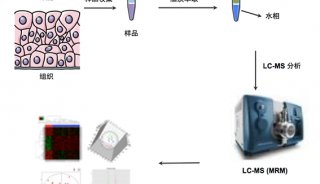
小鼠海马组织、人血清样本
技术路线
步骤1:多组学联合分析揭示凝血酶诱导铁死亡过程;
步骤2:凝血酶诱导的铁死亡过程可能与缺血性卒中有关;
步骤3:证实脑缺血再灌注损伤中发生铁死亡过程,并分析引发铁死亡的必要条件;
步骤4:临床研究中关于缺血性脑卒中后血小板活化起因;
步骤5:ACSL4介导凝血酶神经毒性,调控其表达可改变急性缺血性脑损伤小鼠预后。
研究结果
1. 多组学联合分析揭示凝血酶诱导铁死亡过程
结合有磷脂酰乙醇胺(PEs)的花生四烯酸(AA)特别容易受到亚铁过氧化作用的影响,研究人员通过对正常小鼠与缺血性卒中后小鼠的海马组织进行脂质组学分析,找到了四种显著减少的磷脂即PC (36:4), PE (42: 8), PE (38: 6p), 和PE (40: 7),并在进一步的分析中发现其脂肪酸侧链中均含有AA,作者也通过蛋白质组学分析研究了缺血性卒中后导致AA升高的蛋白表达情况。基于差异表达蛋白的富集,以及蛋白质间的相互作用(PPI)网络分析,找到有关血小板激活、信号转导和聚集是上调最多的途径,并找到了上调最多的蛋白质——凝血酶原。

图1 缺血/再灌注导致磷脂侧链上花生四烯酸的释放

图2 急性缺血/再灌注后凝血酶在脑组织中显著上调
2. 凝血酶诱导的铁死亡过程与缺血性卒中有关
由于凝血酶具有促进纤维蛋白产生和凝血的作用,因此是缺血性脑卒中的主要药物靶点之一。作者研究证实凝血酶剂量依赖性地诱导N27神经元细胞死亡,并伴有AA和脂质过氧化物升高的现象。而凝血酶诱导的细胞死亡可以通过铁死亡抑制剂利普罗他汀-1、谷胱甘肽前体N-乙酰-L-半胱氨酸以及胞浆型磷脂酶(cPLA2α)抑制剂darapladib来预防。同时作者也研究了凝血酶抑制剂达比加群(dabigatran)对缺血再灌注氧糖剥夺(OGD)模式细胞的保护作用,证实凝血酶升高是缺血性卒中后AA所动员的上游信号。这些实验强调了凝血酶诱导铁死亡的可能性,并且该过程可能与缺血性卒中有关。

图3 凝血酶诱导了神经元细胞的铁死亡过程
3. 证实脑缺血再灌注损伤中发生铁死亡过程,并分析引发铁死亡的必要条件
为了分析缺血性脑卒中引发铁死亡的必要条件,作者对MCAO模型鼠(小鼠和大鼠)再灌注后,产生卒中的脑区与对照脑区中的海马体和皮质层进行多组生理生化指标的测定。研究发现产生卒中的脑区中,受影响的海马和皮质区域的脂质过氧化物(LPO)以及脂质过氧化物的分解产物丙二醛(MDA)水平明显高于对照脑区。并且再灌注后立即给药的铁死亡诱导剂(GPx4抑制剂RSL3及Erastin)显著加重了模型鼠的脑损伤。而铁死亡抑制剂(liproxstatin-1 和ferrostatin-1)有效减弱了模型鼠的脑损伤,但这些抑制剂并不能挽救永久性的神经元损伤。同时作者也在氧糖剥夺细胞模型中证实了神经元细胞铁死亡的发生。

图4 脑缺血再灌注损伤中的氧依赖性铁死亡过程
4. 临床研究中关于缺血性脑卒中后血小板活化起因
凝血功能的激活是缺血性脑卒中神经元损伤的主要原因,因此抑制凝血酶可能预防和治疗脑梗死,并降低脑卒中后残余神经功能缺损的程度。该研究中共收集了59份临床血清样本,包括27例健康对照和32例缺血性脑卒中病例。对这些血清样本进行基于TMT标记的蛋白质组学分析,在去除高丰度蛋白后共鉴定到584个蛋白质。在缺血性卒中病例血清样本中共发现28个蛋白上调,21个蛋白下调。基因集富集分析显示显著改变的通路,包括纤维蛋白凝块形成共同途径和淋巴-非淋巴细胞免疫调节相互作用,但脑卒中患者血清凝血酶原丰度并未高于健康对照,提示脑组织中上升的凝血酶并非来源于血液,抗凝血酶药物引起的有效作用很可能源于脑组织中凝血酶相关功能被抑制。

图5 缺血性卒中后血小板活化
5. ACSL4介导凝血酶神经毒性,调控其表达可改变急性缺血性脑损伤小鼠预后
酰基辅酶A合成酶长链家族成员4 (ACSL4)是一种参与脂质代谢的重要酶,通过将游离的AA转化为花生四烯酰辅酶A生成脂质氢过氧化物进而参与铁死亡。该研究通过实验证实ACSL4的下调是大脑应对卒中的早期调控手段,凝血酶可能通过促进ACSL4诱导的铁死亡过程导致神经元细胞死亡,同时ACSL4的降低可能有助于对抗凝血酶诱导的铁死亡造成的细胞损伤。为了进一步验证ACSL4在MCAO模型鼠中是否影响脑缺血再灌注的预后,对小鼠进行原位AAV注射进行基因表达(过表达或敲除ACSL4)调控干预。结果表明,ACSL4 OE小鼠在缺血再灌注后脑损伤程度加重,而ACSL4 KO对小鼠缺血后再灌注损伤中具有保护作用。

图6 凝血酶诱导急性脑缺血/再灌注后 ACSL4 的下调

图7 调控ACSL4表达改变急性缺血性脑损伤小鼠预后
小编小结
该研究发现凝血酶通过ACSL4促进缺血性脑卒中后诱导的细胞铁死亡过程,通过抑制该通路可能为治疗提供新的途径。本研究首次阐明了凝血酶在细胞铁死亡中的作用,并且证明了铁死亡过程在缺血性疾病中的重要性。通过蛋白质组学、脂质组学和免疫化学,作者发现凝血酶及其在AA代谢中的下游因子ACSL4,是参与急性缺血性脑损伤中导致细胞铁死亡的关键蛋白,从而对缺血性脑卒中驱动铁死亡的生物学机制有了更新的认识。

中科优品推荐
代谢线产品促销活动火热进行中~
非靶代谢plus | 450元/样 |
H650医学高通量靶向代谢组 | 850元/样 |
空间代谢组(100um) | 7700元/cm2 |
做空间代谢组送非靶代谢组 | 买一送一 |
注:非靶代谢plus:小样本量可享受急速周期,两周即可交付。



我知道你
在看
哦