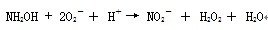| 实验步骤 | 一、材料仪器设备及试剂
1. 材料:花生、绿豆、大豆黄化幼苗的下胚轴及其他植物叶片。
2. 仪器设备:高速冷冻离心机,分光光度计,恒温水浴锅,研钵,试管,移液管,试管架,移液管架,洗耳球等。
3. 试剂配制:
50 mmol·L-1磷酸缓冲液(pH7.8)
1 mmol·L-1盐酸羟胺
17 mmol·L-1对氨基苯磺酸(以冰醋酸 :水 = 3 :1配制)
7 mmol·L-1 α-萘胺(以冰醋酸 :水 = 3 :1配制)
50nmol· ml-1NaNO2母液
二、实验步骤
1. 提取液制备
称取1g植物叶片放入冰浴的研钵中,加入50mmol·L-1磷酸缓冲液(pH7.8)5 ml, 研磨成匀浆,在1000r/min,4℃下离心10min,取上清液再以15000r/min,4℃下离心20min,第二次上清液即为样品提取液。
2. 亚硝酸根标准曲线的制作
2.1系列浓度NaNO2溶液的配制
取50nmol· ml-1NaNO2母液,分别稀释成0、10、20、30、40和50、nmol· ml-1的标准稀释液。
2.2取7支试管,编0~6号,分别加10、15、20、30、40、50、nmol· ml-1NaNO2标准稀释液1 ml,0号管加蒸馏水1 ml,然后各管再加50mmol·L-1磷酸缓冲液1 ml,17 mmol·L-1对氨基苯磺酸1 ml和7 mmol·L-1 α-萘胺1 ml,置于25℃显色20min后,以0号管作空白对照,在530nm波长处测定吸光度(A)值。
2.3 标准曲线绘制
以1~6号管亚硝酸根(NO2-)浓度为横坐标,吸光度值作纵坐标,绘制标准曲线。
3. O2-含量测定
取4支试管,编0~3号,1~号管分别加入样品提取液0.5 ml(三个重复),0号管加蒸馏水0.5 ml,然后各管加入50mmol·L-1磷酸缓冲液0.5 ml,1 mmol·L-1盐酸羟胺1 ml,混匀,置于25℃ 1 h后,各管再加入17 mmol·L-1对氨基苯磺酸1 ml和7 mmol·L-1α-萘胺1 ml,混匀,置于25℃显色20min,以0号管为空白对照,在530nm波长处测定吸光度(A)值。
三、结果计算
根据所测得的A530值,从标准曲线上查得样品中NO2-浓度,按公式(1)即可计算出样品中NO2-浓度。然后依据羟胺与O2-的上述反应,从NO2-对O2-进行化学计量,按公式(2)计算,即将按公式(1)计算得到的NO2-浓度乘2,得O2-浓度。也可根据被测样品与羟胺反应的时间和样品中蛋白质含量,按公式(3)求得O2-的生产率。
 展开 |
|---|