化疗/化学动力治疗药物取得新进展
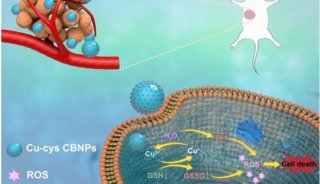
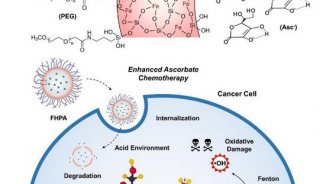
肿瘤的化学动力疗法(chemodynamic therapy,CDT)利用药物将内源性H2O2通过Fenton反应转化为高细胞毒性的活性氧(reactive oxygen species,ROS)以杀死肿瘤细胞。因其不依赖于外界刺激和局部氧浓度,CDT成为了抑制深部缺氧性肿瘤生长的理想候选疗法。目前阻碍CDT进一步发展的关键是如何在肿瘤部位产生足量的内源性H2O2。
在临床上广泛使用的铂类化疗药物被证实不仅具有良好的化疗效果,还能够特异性激活癌细胞内的烟酰胺腺嘌呤双核苷酸磷酸盐氧化酶(NOX)进而将O2转化为O2·-,O2·-再由超氧化物歧化酶(SOD)转化为H2O2。因此,顺铂介导的化疗可与CDT复合使用,顺铂介导H2O2的形成,CDT药物将H2O2转化为ROS。尽管这一思路在理论上十分高效,并且有化疗/化学动力治疗复合药物的相关报道,但它们的药物制备通常涉及复杂的化学合成过程,化疗和化学动力治疗的药物比例也不能得到有效的控制。

近日,来自澳门大学的王瑞兵教授和新加坡国立大学的陈小元教授团队利用超分子聚合引发的纳米自组装现象制备了新型化疗/化学动力治疗药物,克服了上述困难。超分子聚合所用单体是铂(IV)配合物(化疗药物)、二茂铁(化学动力治疗药物)和β-环糊精共价连接形成的分子。通过二茂铁和β-环糊精的主客体的相互作用头尾连接形成线性超分子聚合物,当上述线性聚合物用带有二茂铁端基的聚乙二醇封一端后,就会形成两亲性超分子聚合物,进而自组装成胶束纳米药物。相比于之前的制备方法,超分子聚合诱导的纳米自组装具有如下优势:1)超分子聚合流程简单,调价温和,纳米药物可以一步制备;2)可以添加不带铂(IV)配合物的单体进行共聚,调节化疗和化学动力治疗药物的比例。上述纳米药物在肿瘤位点通过高渗透长滞留作用(EPR)富集,在H2O2作用下二茂铁氧化成形成亲水的二茂铁盐(H2O2则转变为ROS),促进超分子聚合物解聚,释放出更多的二茂铁端基和铂(IV)配合物;铂(IV)配合物还原成顺铂,促进H2O2的生成,进一步加速聚合物解聚,进而实现自增强。

上述方案不仅具有优异的疗效,更大大简化了纳米药物的制备流程,因而推进了CDT疗法的实用化。