核酸研究揭秘m6A调控胃癌细胞EMT过程
1.METTL3的临床相关性
TCGA数据库中胃癌数据的搜索结果显示METTL3在胃癌组织中高表达且与较差的临床预后相关,这一趋势在对60例病人的qPCR验证结果中保持一致,且METTL3的表达量与分期分级呈一定相关性。重要的是,METTL3在弥散型胃癌(diffuse-type GC)样本中的表达量要高于肠型(intestinal-type GC)样本。整体水平的甲基化显示,胃癌样本中mRNA的m6A修饰水平要高于对照样本。免疫组化结果显示METTL3主要分布于细胞核。KM曲线、单因素、多因素等分析都说明METT3是一个胃癌重要的临床预后相关因子,在GC样本中高表达,并与GC的发生发展相关。
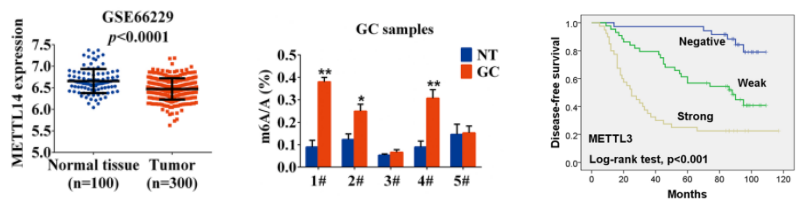
图1 METTL3高表达与临床相关性
2.METTL3是EMT过程必不可少的
免疫组化染色结果提示METTL3和N-cadherin、Vimentin表达呈正相关,与E-cadherin呈负相关。对AGS细胞系的相关检测表明,METTL3和EMT表型、间充质标志物的重要marker蛋白呈正相关。 过表达、敲除实验都能伴随着N-cadherin、Vimentin以及E-cadherin的相关性变化的同时,也能引起GC细胞整体水平m6A的变化。这些结果都表明METTL3实质上能够促进GC细胞的EMT过程发生发展。
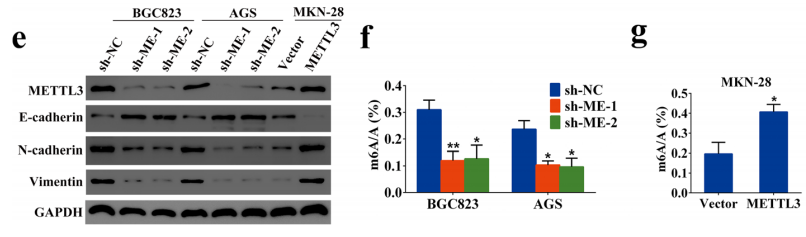
图2 METTL3的干预可以改变EMT相关marker的改变
3.体内体外实验证明METTL3促进细胞侵袭与转移
METTL3介导的EMT过程是否能引起GC细胞的转移?划痕实验与transwell实验证明METTL3表达的下调能够明显的阻碍BGC823细胞的迁移能力与侵袭能力,而上调能够明显增强MKN-28细胞的转移能力与异位表达。尾静脉注射的裸鼠在体实验证明BGC823-shRNA细胞的转移能力要明显弱于对照细胞,反之亦然。无论体内体外实验都说明METTL3可以增强胃癌细胞的侵袭和转移能力。
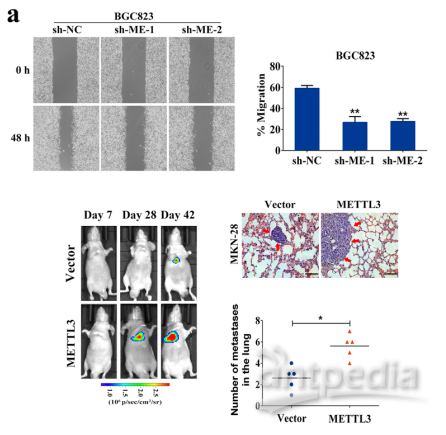
图4 体内体外证明METTL3具有增强转移、侵袭能力
4. RNA-seq&m6A MeRIP-seq发现ZMYM1是METTL3的重要靶点
Mettl3的强大功能在之前的结果当中已经被证实,但是它的靶点分子有哪些?RNA-seq转录组测序首先明确在METTL3敲除以后哪些基因发生了差异性表达,测序结果显示798个基因显著下调,662个基因显著上调。相同背景的样本使用m6A MeRIP-seq甲基化测序发现9465和8794个m6A位点是组内特异的,GO分析发现差异甲基化的基因功能主要富集在半包桥小体组装(hemidesmosome assembly)、中心体定位(centrosome localization)等功能,暗示m6A修饰可能会带来染色体方面的影响。信号通路富集结果显示多个肿瘤相关的信号通路(肾癌、甲状腺癌以及HIF信号通路)都被有效富集,m6A经典motif也有显著富集。 把850个甲基化水平下调的甲基化基因和798个下调的靶基因进行联合分析把目标锁定在其中13个基因,在这13个基因当中最终选择带有两个甲基化修饰位点的ZMYM1作为下游靶标,这两个甲基化修饰位点都存在于终止密码子附近,在METTL3敲低以后甲基化水平都下调。目前,ZMYM1的生物学功能并不清楚,接下来需要做的工作就是搞清楚ZMYM1的功能以及甲基化的调控作用。
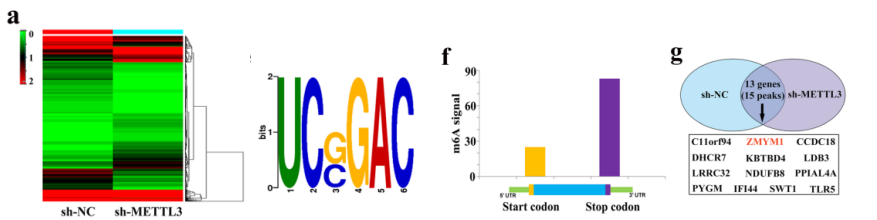
图5 差异甲基化和差异表达RNA的联合分析
5. ZYMY1与METTL3相关性探索
无论在蛋白水平还是RNA水平,METTL3的敲除的可以显著下调ZMYM1的表达,而METTL3的过表达可以上调ZMYM1表达,实验证明ZMYM1和METTL3呈正相关,METTL3正相关调控ZMYM1。
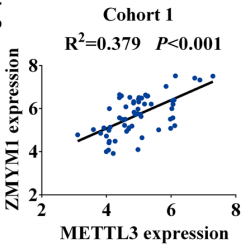
图5 METTL3和ZYMY1相关性分析
6. METTL3通过依赖于HuR结合增强ZMYM1 mRNA稳定性
MeRIP-qPCR首先用于对ZMYM1 mRNA甲基化区域的验证。在确定了ZMYM1 mRNA的甲基化位点确实存在之后,通过METTL3的过表达或敲除之后能够明显改变该位点的甲基化水平,进一步说明该m6A位点受METTL3的调控。通过对ZMYM1甲基化位点的单碱基突变,过表达或者敲除METTL3对该甲基化位点的调控作用就消失了。由于HuR蛋白和METTL3一样主要分布在细胞核当中,并且一直被认为是一个由METTL3募集的间接m6A Reader蛋白,作者选择重点关注HuR和RNA分子之间的相互结合,HuR和ZYMY1的结合区域恰巧在m6A修饰位点附近,在ZMYM1发生去甲基化(沉默METTL3)以后,HuR和METTL3的结合大大减弱,这一系列实验证明METTL3对ZMYM1的影响是通过m6a修饰从而结合HuR蛋白来进行的。
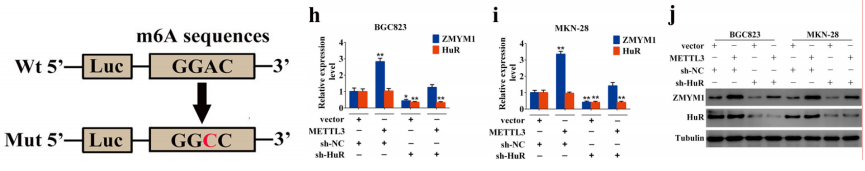
图6 甲基化位点的碱基突变策略以及影响HuR蛋白相互结合
7. ZMYM1复合物在核内抑制E-cadherin从而影响EMT过程
由于锌指蛋白结构有调控转录活性特性的特点,猜想ZMYM1同样在细胞核内有调控转录活性的作用。实验证明ZMYM1能够通过MYM型锌指结构同CtBP/LSD1/CoREST复合物结合,进而增强对靶基因的转录抑制作用。免疫共沉淀Co-IP实验证实了ZYMY1与CtBP/LSD1/CoREST复合物结合的存在形式。而这种复合物的存在可以有效的靶向抑制E-cadherin的转录。直接对ZMYM1的过表达或者敲除实验也证明ZMYM1能够改变胃癌细胞的迁移与侵袭行为,METTL3正是通过调控m6A影响HuR蛋白结合的方式来改变METTL3的表达量,进而促进胃癌细胞的EMT过程。
总结
RNA甲基化作为当下生命科学的研究领域最热主题被广泛研究,在多种疾病当中均有显著调控作用,花样繁多的作用方式可以从RNA分子核内转录到核外成熟从而影响其分子一生。这项研究成果让读者从新的角度来解释甲基化对肿瘤EMT的影响。