Celltrion单抗药物Regkirona获欧盟批准:治疗高危COVID-19患者
根据百度《新型冠状病毒肺炎疫情实时大数据报告》,截止2021年11月17日01时,全球累计确诊超过2.5亿例(2.5480亿),死亡超过512万例。
近日,韩国生物制药公司Celltrion Group宣布,欧盟委员会(EC)已批准Regkirona(regdanvimab,CT-P59),用于治疗不需要补氧、有增加的风险发展为严重疾病的COVID-19成人患者。目前,Regkirona尚未获得美国FDA批准,但Celltrion公司正在与FDA讨论提交紧急使用授权(EUA)申请。
Regkirona是欧盟授予上市许可的首批单克隆抗体药物之一。在同一周,欧盟批准罗氏/再生元抗体鸡尾酒疗法Ronapreve(casirivimab和imdevimab,前称:REGN-COV2):(1)用于治疗不需要补氧、有增加的风险发展为严重疾病的COVID-19成人和青少年(年龄≥12岁,体重≥40公斤)患者;(2)用于年龄≥12岁、体重≥40公斤的人群,预防COVID-19(暴露前或暴露后预防)。

Regkirona和Ronapreve的审批决定是在欧洲药品管理局(EMA)人用医药产品委员会(CHMP)在11月11日发表积极审查意见之后立即做出的,反映了EMA和EC在COVID-19疫情期间将缩短安全有效高质量疗法审查时间作为优先事项。通常情况下,如果CHMP对药品发布了积极的审查意见,EC通常会在1-2个月内作出审查决定。
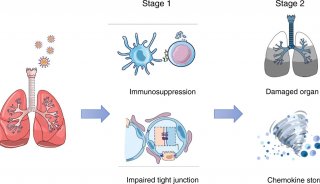
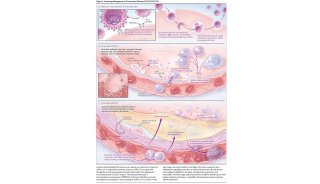
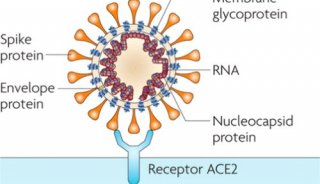
单克隆抗体是一种蛋白质,旨在附着到一个特定的靶点,在这种情况下是新型冠状病毒(SARS-CoV-2)的棘突蛋白,其作用是阻断病毒进入人类细胞的途径。
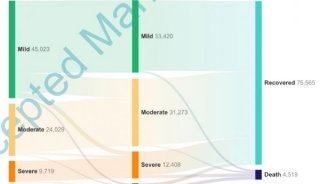
欧盟批准Regkirona,基于全球3期临床试验的数据。该试验涉及美国、西班牙、罗马尼亚等13个国家1315人,评估了Regkirona的疗效和安全性。数据显示,对于有高风险发展为严重COVID-19的患者,Regkirona治疗将COVID-19相关住院或死亡风险显著降低了72%。
原文出处:Celltrion’s Monoclonal Antibody Treatment regdanvimab, Approved by the European Commission for the Treatment of COVID-19
-
企业风采
-
科技前沿
-
焦点事件
-
项目成果
-
产品技术

-
科技前沿
-
科技前沿
-
项目成果
-
焦点事件