罗氏美罗华获FDA批准首个儿科适应症 治疗2种血管炎
罗氏(Roche)旗下基因泰克近日宣布,美国食品和药物管理局(FDA)已批准Rituxan(美罗华,通用名:rituximab,利妥昔单抗),与糖皮质激素(GCC)联合使用,用于2岁及以上儿童,治疗伴肉芽肿性多血管炎(GPA)和显微镜下多血管炎(MPA)。值得一提的是,Rituxan是首个也是唯一一个获FDA批准治疗2岁及以上儿科患者GPA和MPA的药物。
GPA和MPA是2种罕见的、可能危及生命的血管炎,影响中小血管。该适应症通过FDA的优先审查程序获得批准,同时也标志着Rituxan的首个儿科适应症。
此次批准,基于PePRS研究的数据。这是评估Rituxan治疗GPA或MPA儿科患者的首个全球性研究。该研究是一项全球性、开放标签、单臂、IIa期研究,共入组了25例年龄6-17岁的重度、新诊或复发性活动性GPA或MPA患者,评估了静脉注射Rituxan(每4周一次)联合口服糖皮质激素(GCC)剂量递减方案的安全性、药效学/药代动力学和探索性疗效。入组研究的25例患者,19例GPA,6例MPA,疗效采用儿童血管炎活动评分(PVAS)进行评估。
结果显示,有56%的患者在治疗第6个月达到PVAS缓解,92%的患者在治疗第12个月达到PVAS缓解,100%的患者在第18个月达到PVAS缓解。安全性方面,Rituxan在儿童GPA和MPA患者中的安全性在类型、性质和严重程度上与成人GPA、MPA、类风湿性关节炎、寻常型天疱疮患者中已知的Rituxan安全性一致。
罗氏首席医疗官兼全球产品开发主管Sandra Horning博士表示:“Rituxan现在被批准为首个也是唯一一个治疗GPA和MPA儿童患者的药物,这是2种在儿童中罕见的、可能危及生命的血管疾病。今天的批准是我们一直以来致力于与FDA密切合作为有严重未满足医疗需求的罕见病儿科患者开发药物方面的一个重大进展。”
Rituxan是一种治疗性单克隆抗体,靶向结合正常和恶性B细胞表面的CD20抗原,随后调动人体天然防御,攻击和杀死被标记的B细胞。之前,Rituxan已获批治疗成人的4种自身免疫性疾病,包括:类风湿性关节炎(RA)、GPA、MPA、寻常型天疱疮(PV)。对于GPA和MPA成人患者,Rituxan联合糖皮质激素(GCC)是唯一获FDA批准的治疗方案。自2006年以来,在全球范围内,已有超过90万患者接受Rituxan治疗自身免疫性疾病。
GPA和MPA是2种抗中性粒细胞胞浆抗体(ANCA)相关性血管炎(AAV)。AAV是一种血管炎,主要影响小血管。一般来说,GPA和MPA都影响肾脏、肺、鼻窦和各种其他器官的小血管,但这些疾病可能对每个患者造成不同的影响。GPA和MPA均被认为是罕见的疾病,全球估计患病率为每百万人口23-160例。儿童期发病的GPA和MPA病例更为罕见,并与严重的、潜在危及生命的症状有关。
-
产品技术
-
企业风采

-
企业风采

-
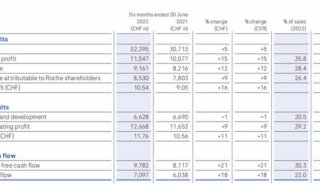
财报
-
焦点事件

-
焦点事件
-
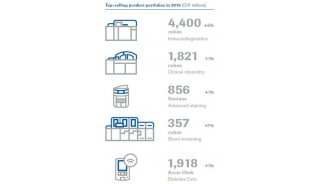
财报
-
焦点事件