VPS18被 RDN 特异性抑制以治疗获得性耐药性癌症
多药耐药性 (MDR) 仍然是成功治疗癌症的主要挑战。许多赋予治疗诱导的耐药性的机制已被广泛研究,以探索如何对抗 MDR。在这方面,溶酶体隔离已被证明是一种通过“脱靶”效应导致耐药性的机制,其中疏水性和弱碱性化学治疗剂被困在溶酶体中,将它们与靶标隔离。破坏溶酶体酸化的方法,调节酸性鞘磷脂酶 (ASM) 并增加溶酶体膜通透性已被开发以克服耐药性。
2021年6月7日,山东大学娄红祥及苑辉卿共同通讯在Signal Transduction and Targeted Therapy (IF=13.49)上在线发表了题为“Targeting of VPS18 by the lysosomotropic agent RDN reverses TFE3-mediated drug resistance”的研究论文,该研究证明了 TFE3/溶酶体/MRP2 通过溶酶体隔离机制在 MDR 发展中的新功能。溶酶体 VPS18 对癌症和耐药性发展的贡献可以作为潜在的治疗靶点进行探索,它被一种新型化合物 RDN 特异性抑制以治疗获得性耐药性癌症。

多药耐药性 (MDR) 仍然是成功治疗癌症的主要挑战。许多赋予治疗诱导的耐药性的机制已被广泛研究,以探索如何对抗 MDR。在这方面,溶酶体隔离已被证明是一种通过“脱靶”效应导致耐药性的机制,其中疏水性和弱碱性化学治疗剂被困在溶酶体中,将它们与靶标隔离。破坏溶酶体酸化的方法,调节酸性鞘磷脂酶 (ASM) 并增加溶酶体膜通透性已被开发以克服耐药性。 转录因子 E3 (TFE3) 和 TFEB 成为溶酶体生物发生和自噬过程的主要调节因子,以响应细胞应激,因此,中断 TFE3/TFEB 介导的作用在癌症中具有巨大的治疗潜力。
在本研究中,揭示了一种新机制,通过该机制,TFE3/溶酶体激活对治疗剂的反应,如多西紫杉醇 (Doc),通过促进多药耐药相关蛋白 2 (MRP2) 的溶酶体定位和增强溶酶体中的药物螯合来促进 MDR ,该研究还确定溶酶体液泡蛋白分选 18 (VPS18) 作为一种新型溶酶体药物 RDN(一种天然双联苄基 riccardin D 的氨甲基化衍生物)逆转化学抗性的潜在靶标。
该研究最初评估了 Doc 诱导的多药耐药 PC3/Doc 癌细胞中基因表达的变化。与溶酶体和线粒体途径代谢相关的基因的表达谱在抗性细胞中特别改变。溶酶体相关参数的检查表明,溶酶体和自噬体的数量在不同抗性细胞系中显著增加。因此,溶酶体激活是不同抗肿瘤药物治疗的结果。
鉴于 TFEB 和 TFE3 在调节溶酶体生物发生中的重要性,因此该研究确定了这两个因素在治疗诱导的向溶酶体的代谢转变中的参与。结果清楚地表明,临床药物显著激活 TFEB 和 TFE3,尤其是 TFE3,在体外和体内促进 TFE3 核易位(具有高度磷酸化的活性形式)。接下来确定了治疗激活的 TFE3/溶酶体是否有助于耐药性。TFE3 下调显著恢复了 PC3/Doc 细胞对 Doc 或 Dox 的敏感性,而 TFE3 的过表达显著增加了 PC3 细胞对药物的耐受性,表明 TFE3 在赋予 MDR 中的作用。因此,溶酶体介导的 Doc 或 Dox 捕获会导致脱靶效应,从而降低其抗肿瘤功效。
为了探索溶酶体药物螯合的潜在机制,该研究测试了 ABC 家族转运蛋白是否充当细胞膜泵并在介导 MDR 中发挥关键作用。筛选测定将 MRP2(ABCC2)鉴定为溶酶体耐药性的重要介质。尽管 MRP2 主要位于细胞膜上,但大量 MRP2 存在于细胞质中,并显示与抗性细胞中的溶酶体相关膜蛋白 2(LAMP2)共定位。进一步的研究确定 MRP2 作为 TFE3 的靶标,它可以在化学处理后通过 MRP2 启动子中的 E-box 基序转录增强 MRP2 表达。因此,治疗驱动的 TFE3 激活刺激了 MRP2 在溶酶体中的表达和定位,促进了溶酶体介导的药物捕获和耐药性。

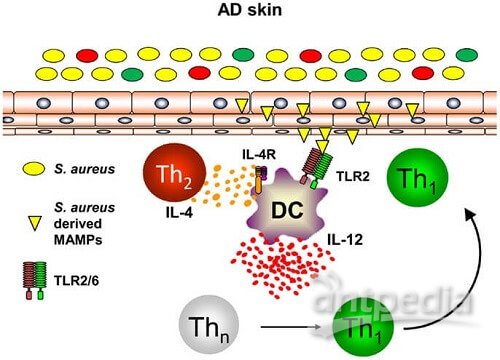
文章模式图(图源自STTT )
该研究接下来确定靶向 TFE3/溶酶体轴是否有效逆转 MDR。结果表明 RDN 与 VPS18 的 RING 结构域结合,导致 VPS-C 核心复合物和溶酶体功能的破坏。为了探讨 VPS18 是否是一个重要的病理效应物,该研究首先检测了 VPS18 在癌症中的水平。结果表明,VPS18在几种癌症中的表达高于邻近的非癌组织,包括前列腺癌(PRAD)、膀胱癌(BLCA)、肝癌(LIHC)和肺癌(LUAD)。高水平的 VPS18 与恶性癌症的不良预后相关。VPS18 敲低显著抑制了小鼠的癌细胞增殖和肿瘤生长。重要的是,该研究观察到 VPS18 表达可被不同的化疗药物诱导,并且在耐药细胞中显著增加。VPS18 沉默显著增加了耐药细胞对 Doc 和 Dox 的敏感性,而 VPS18 的过表达抑制了化疗药物对细胞增殖的功效。因此,VPS18 成为肿瘤预后的新分子指标和逆转溶酶体介导的耐药性的靶点。
总之,该研究提供的证据证明了 TFE3/溶酶体/MRP2 通过溶酶体隔离机制在 MDR 发展中的新功能。溶酶体 VPS18 对癌症和耐药性发展的贡献可以作为潜在的治疗靶点进行探索,它被一种新型化合物 RDN 特异性抑制以治疗获得性耐药性癌症。
-
仪器推荐
-
仪器推荐

-
仪器推荐

-
仪器推荐

-
仪器推荐
 询底价 Tel:400-6699-117 转 4029
询底价 Tel:400-6699-117 转 4029