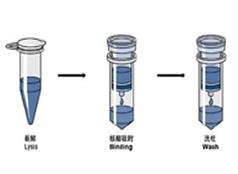
TRIzol法同时提取RNA、DNA、蛋白质(二)
DNA的分离
准备试剂:乙醇0.1M柠檬酸钠(含10%乙醇)、 75%乙醇、8mM NaOH
操作步骤:
1. 样品加氯仿分层后,移去上层水相,用乙醇沉淀中间层和有机相中的DNA。每使用1mlTRIzol加0.3ml无水乙醇混匀,室温放置3分钟,2~8℃不超过2000×g离心5分钟。
2. 移去上清,(如需分离蛋白质,可保留,进一步操作见后)用含10%乙醇的0.1M柠檬酸钠洗涤DNA沉淀。每用1mlTRIzol加入1ml柠檬酸钠,室温放置30分钟,2~8℃2000×g离心5分钟,弃上清,重复一次。可以再重复一次。
3. 用75%乙醇再洗一遍DNA沉淀,每用1ml TRIzol加入1.5~2 ml75%乙醇,室温放置10~20分钟(不时颠倒混合)2~8℃2000×g离心5分钟, 弃上清。
4. 室温放置晾干DNA 5~15分钟,用8mM NaOH溶解DNA。从50~70mg组织或107细胞中分离的DNA溶于300~600μl 8mM NaOH,DNA的浓度通常为0.2~0.3μg/μl。提取的DNA沉淀不易溶于水和Tris缓冲液中,建议用弱碱溶解,8mMNaOH的pH值为9,溶解DNA后可用TE,HEPES调节pH。从某些样品(尤其是组织)中提取的DNA中可能包含一些胶状不溶物可>12000×g离心10分钟除去。
DNA的定量:取一份溶于8mMNaOH的DNA加水测A260值。一单位A260值相当于50μg/ml双链DNA。根据DNA产量可估计细胞数,人、大鼠、小鼠、1×106二倍体细胞含DNA的量分别为7.1μg,6.5μg,5.8μg。
预期产量:1mg组织或1×106细胞提取DNA分别为肝和肾3~4μg 骨骼肌,脑组织,胎盘2~3μg 人,大鼠,小鼠培养细胞(1×106)5~7μg 成纤维细胞5~7μg。
应用:
1.用于PCR 溶于8mM NaOH的DNA用0.1M HEPES调pH至8.4,取0.1~1μg DNA用作模板。
2.酶切反应用HEPES或1mM EDTA调节pH至适当值。每μg DNA使用3~5单位的酶,80~90%的DNA是可消化的。
1ml 8mM NaOH溶解的DNA样品pH值调节
Final pH 0.1M HEPES(μl) Final pH 1M HEPES(μl)
8.4 86 7.2 23
8.2 93 7.0 32
8.0 101
7.8 117
7.5 159
注意事项:
1. DNA在中间层和有机相中时可在2~8℃保存过夜。
2.DNA沉淀在75%乙醇中2~8℃可保存几个月。
3.DNA在8mM NaOH溶液中4℃可放置过夜,如长期保存需用HEPES调节pH至7~8并且加EDTA至1mM,可置于4℃或-20℃长期保存。
常见问题分析:
得率低:
A.样品匀浆和裂解的不彻底。
B.最终得到的DNA沉淀没有完全溶解。
A260/A280<1.70 :
A. 检测吸光度时,RNA样品没有溶于水,而溶于了TE中。
B.酚除去的不彻底,可用0.1M柠檬酸钠(含10%乙醇)再洗一遍DNA沉淀。
DNA降解:
A.组织取出后没有马上处理或冷冻。
B.待提取RNA的样品没有保存于-60至-70℃,而保存在了-5至-20℃。
C.样品匀浆时使用了高速匀浆仪。
RNA污染:
A.氯仿分层后水相去除的不干净。
B.DNA沉淀用0.1M柠檬酸钠(含10%乙醇)洗的不彻底。
蛋白质的提取
准备试剂:异丙醇、含0.3M盐酸胍的95%乙醇、无水乙醇、1%SDS。
操作步骤:
1.取沉淀DNA后剩余的上清,用异丙醇沉淀蛋白质。每使用1ml TRIzol加1.5ml异丙醇,室温放置10分钟,2~8℃12000×g离心10分钟弃上清。
2.用含0.3M盐酸胍的95%乙醇洗涤蛋白质沉淀。每使用1mlTRIzol加2ml洗涤液,室温放置20分钟,2~8℃7500×g离心5分钟,弃上清,重复两次。用2ml无水乙醇同样方法再洗一次。
3.真空抽干蛋白质沉淀5~10分钟,用1%SDS溶解蛋白质,反复吸打,50℃温浴使其完全溶解,不溶物2~8℃10000×g离心10分钟除去。分离得到的蛋白质样品可用于Western Blot或-5至-20℃保存备用。
注意事项:
1.蛋白质沉淀可保存在含0.3M盐酸胍的95%乙醇或无水乙醇中2~8℃一个月以上或-5至-20℃一年以上。
2.用0.1% SDS在2~8℃透析三次,10000×g离心10分钟取上清即可用于Western Blot。
常见问题分析:
得率低:
A.样品裂解或匀浆处理不彻底。
B.最后得到的蛋白质沉淀未完全溶解。
蛋白质降解:组织取出后没有马上处理或冷冻。
电泳时条带变形:蛋白质沉淀洗涤不充分。
操作步骤:
1. 用Trizol试剂匀浆细胞和组织的方法同RNA提取步骤。
2. 在细胞匀浆中加入氯仿,每1ml Trizol的起始用量加入0.2ml氯仿。剧烈震荡30秒钟后室温放置2~3分钟。
3. 4℃下10,000g离心10分钟。
4. 小心吸取并丢弃上层水相(该水相中富含细胞总RNA,如果需要提取RNA,则收集该水相)。
5. 在剩下的中间层及有机相中加入无水乙醇,每1ml 起始Trizol用量加入0.3ml无水乙醇。颠倒充分混匀后室温放置2~3分钟。
6. 4℃下2,000g离心5分钟。
7. 小心吸取并收集上层的酚醇有机相(沉淀为DNA),转移到一个新的离心管中,加入异丙醇,每1ml 起始Trizol用量加入1.5ml异丙醇。轻轻混匀后室温放置10分钟。
8. 4℃下12,000g离心10分钟。
9. 丢弃上层液相,沉淀即为蛋白质。用清洗液(盐酸胍溶于95%乙醇中,终浓度为0.3M)清洗沉淀3次。每1ml 起始Trizol用量加入2ml清洗液清洗。在每次清洗过程中,先将沉淀保留于清洗液中20分钟(室温下),然后在4℃下7,500g离心5分钟。最后一次清洗后,丢弃上层液相,将沉淀悬浮于2ml乙醇中,涡旋震荡15秒后在室温下放置20分钟,然后在4℃下7,500g离心5分钟。
10. 丢弃上层液相,将沉淀真空干燥5~10分钟。然后将沉淀溶解于1% SDS(十二烷基硫酸钠)中。可于50℃水浴中用tip头反复吹打以助溶。不溶物在4℃下10,000g离心10分钟去除。收集上清,转移到新的收集管中。该上清中的蛋白样品可直接用于Western Blotting实验或保存于-20℃。
附注:
1. 蛋白沉淀保存于清洗液(盐酸胍溶于95%乙醇中,终浓度为0.3M)中,或保存于乙醇中,在4℃下可保存至少一个月,在-20℃下可至少保存一年。
2. 在上述步骤7中收集的酚醇有机相,可用0.1% SDS透析三次,透析后4℃下10,000g离心10分钟。上清液可直接用于Western Blotting实验。如果采用这种实验方案,可提高蛋白的回收效率。
3. 如果蛋白溶液中的SDS浓度高于0.1%,则不宜采用考马斯亮兰染色法(Bradford)法对蛋白定量。因为蛋白溶液中可能含有痕量酚,也不宜采用紫外分光光度法定量蛋白质。采用上述方法提取的蛋白,可以用lowry法或BCA法进行蛋白定量。