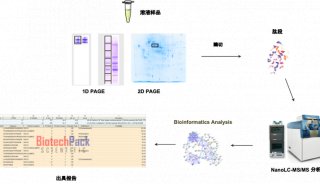
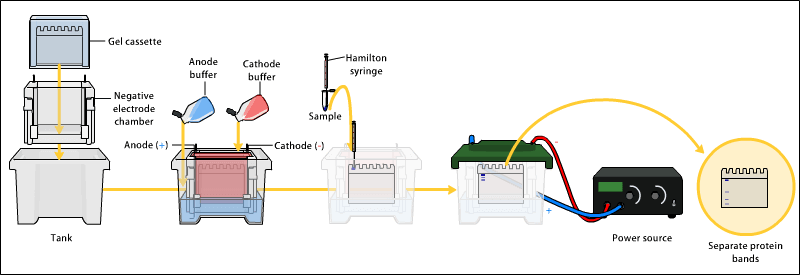
蛋白质分离和分析——凝胶蛋白质染色
| 实验步骤 |
基 本 方 案 1 考马斯亮蓝染色检测范围为〇.3〜lMg 每蛋白质条带。 材 料(带 V 项 目 见 附 录 1)聚丙烯酰胺凝胶(单 元 12. 3) 考马斯亮蓝、银染用固定液 考马斯亮蓝染液 甲醇/乙酸脱色液 7 % (V /V ) 水乙酸 Whatman 3M M 滤 纸(可选) 干 胶 仪(可选) 1 . 将聚丙烯酰胺凝胶放入塑料容器中,加 入 3〜5 倍胶体积的固定液,室温下摇床上振荡 2 h。 2 . 弃去固定液,加入考马斯亮蓝染液振荡 4 h 。 3 . 弃去染色液,用 50m l 左右固定液清洗凝胶。 4 . 弃去固定液,加入甲醇/乙酸脱色液振荡 2 h 。 5 . 弃去脱色液,加入新鲜脱色液继续脱色,直至凝胶背景和条带清晰。可将凝胶储存于 7 % 水乙酸中,或者储存于含水密封塑料袋中, 4°C 可储存一年左右。 6 . 若有需要,可将凝胶拍照。 7 . 若有需要,制成干胶可永久保存凝胶。将凝胶置于两张 Whatman 3M M 滤纸上并用塑料纸覆盖,在 80°C 干胶仪中干燥 1〜2 h 。 基 本 方 案 2 银染材 料聚丙烯酰胺凝胶(单 元 12. 3) 考马斯亮蓝、银染用固定液 甲醇/乙酸脱色液 10% (V /V ) 戊 二 醛 溶 液(从 5 0 % 储存液现配; Kodak) 硝酸银溶液 显色液 K o d a k 快速固定液 A Whatman 3M M 滤 纸(可选) 干 胶 仪(可选) 注 :操作时戴好手套,避免指纹留于凝胶上。 1.将凝胶放入塑料容器中并加入 5 倍胶体积的固定液,室温下摇床上缓慢振荡 30 min以上。 2 . 弃去固定液,加 入 5 倍胶体积的甲醇/乙酸脱色液固定凝胶,缓 慢 振 荡 60m i n 以上。 3 . 弃去脱色液,加 入 5 倍胶体积的 1 0 % 戊二醛溶液,在通风橱中缓慢振荡 30 min。 注意:戴手套并在通风橱中操作。 4 . 弃去戊二醛溶液,用水清洗凝胶 4 次以上,每次水洗时间 30m i n 以上,最好最后一次能清洗过夜。 5 . 弃去洗液,用 5 倍胶体积的硝酸银溶液染色(覆盖胶)15 min,剧烈振荡。 注意:染色后马上弃去硝酸银溶液并用清水冲洗。 6 . 把凝胶放入另一塑料容器中,用去离子水清洗 5 遍 ,每次缓慢振荡 lmin。 7 . 将 25m l 显色液用 500m l 水稀释,把凝胶放入另一容器中,加入足够量显色液剧烈振荡 。显影至目的条带清晰而背景无色,若显色液变成棕色,可更换新鲜显色液。 8 . 将凝胶放入 K o d a k 快速固定液 A 中 5 min,若有需要,可用浸润的棉球擦去凝胶表面残留的银。 9 . 弃去快速固定液,并用清水彻底清洗凝胶(4 或 5 次)。 10.尽快将凝胶拍照。 11.制成干胶可长期保存(见基本方案 1 ,步 骤 7),或者将凝胶储存于密封的塑料袋中(可 保 存 6〜1 2 个月)。 基 本 方 案 3 SYPRO Orange 或 SYPRO Red 荧光染色检测范围为 1〜2n g 每蛋白质条带。 SYPRO Orange 染料推荐使用氩激光扫描器,而 SYPRO Red 染料使用绿 H e -N e 或 N d /Y A G 激光扫描器。这两种染料都需要紫外或宽带照明的激发并在有适当胶情况下,用 C C D 照相系统显色。 材 料VSYPR O Orange 或 SYPRO Red 荧光染液 7.5% (V /v)乙酸 0.1% (V /v) Tween 20 1 . 使 用 SDS-PAGE 电 泳 分 离 蛋 白 质(单 元 12.3),但 电 泳 缓 冲 液 中 S D S 的浓度为0 . 0 5 % ,而非一般情况下的 0 . 1 % 。需 用新鲜配制的 SD S 储存液来配制电泳缓冲液。 2 . 将 SYPRO Omnge 或 SYPRO R ed 荧光染液倒入一个清洗干净的小玻璃皿中。一或两块标准大小的凝胶使用 50m l 左右染色液,大型凝胶则需 500〜750m l 染色液。 对 于 低 浓 度 凝 胶 和 小 分 子 质 量 蛋 白 质 而 言 ,将 染 色 液 的 乙 酸 浓 度 从 7. 5 % 提高到1 0 % ,可 以 使 得 凝 肢 上 蛋 白 质 有 更 好 的 保 持 力 而 不 降 低 灵 敏 度 。 3 . 将凝胶放入染色液中,用铝箔盖住玻璃皿使凝胶避光,或者可将凝胶置于密封的塑料袋中染色,染色液的体积不变。在室温下缓慢振荡 1 〇 〜6 〇 min。 4 . 回收染色液并可重复使用(最 多 4 次)。用 7. 5 % 乙酸彻底冲洗凝胶(< lmin),若有需要,也可将凝胶在染色液中避光过夜。 5 . 将凝胶在 0.1%Tween 2 0 溶液中温育脱色过夜,或者更换数次 7. 5 % 乙酸来脱色。 6 . 将凝胶拍照观察。 基 本 方 案 4 SYPRO Ruby 荧光染色SYPRO Ruby 染料可使糖蛋白、脂蛋白、钙结合蛋白、纤维蛋白和其他难以染色的蛋白质染色,但不影响蛋白质的后续 E d m a n 测序或质谱分析,将凝胶置于塑料支持物上也不影响 SYPRO Ruby 染色。 材 料单向或双向聚丙烯酰胺、 I E F 凝 胶(单 元 12. 3) 双向聚丙烯酰胺凝胶 SYPRO Ruby 染色用固定液 IE F 凝胶固定液: 4 0 % (V A O 甲醇/10% (m /V ) 三氯乙酸 n/ SYPRO Ruby 蛋 白 质 凝 胶 染 色(分子探针) 1 0 % (V /V ) 甲 醇(或乙醇)/ 7 % V /V ) 乙酸 2 % (V /V ) 甘油 旋转摇床 la. 单向聚丙烯酰胺凝胶:直接跳至步骤 2 (无需固定)。 lb. 双 向 聚 丙 烯 酰 胺 凝 胶 :将 聚 丙 烯 酰 胺 凝 胶 用 适 量 S Y P R O R u b y 染色固定液固定 3 〇 min 乙 醇 和 乙 酸 的 结 合 会 形 成 乙 酸 乙 酯 ,这 是 一 种 毒 性 物 质 ,并 且 会 影 响 蛋 白 质 的质 谱 分 析 。 lc. IE F 凝 胶 :用 4 0 % 甲醇/ 1 0 % 三 氯 乙 酸 溶 液 固 定 3 h 后 ,用 蒸 馏 水 冲 洗 三 遍 ,每遍 IOmin 2 . 将凝胶转移至适当大小的聚丙烯或 P V C 平皿中,加入未经稀释的适量 S Y P R O Ruby蛋白质凝胶染色液,连续温和振荡。如 在 50r/m i n 转速的旋转摇床上,为使蛋白质呈现最大灵敏度,单向或双向凝胶需温育 3 h 以上,而 I E F 凝胶则需温育过夜。 3 . 为了降低背景荧光和增强灵敏度,将凝胶转至干净的染色皿中并用 1 0 % 甲 醇(或乙醇) / 7 % 乙酸溶液清洗 30 min,聚丙烯酰胺凝胶清洗一次即可, I E F 凝胶则需清洗三次。 4 . 可 选(永久保存):将凝胶置于 2 % (v/ V ) 甘油中室 温 下 孵 育 30 min,用干胶仪使染色好的凝胶干燥。 5 . 将凝胶拍照并观察结果。 备 选 方 案 1 聚丙烯酰胺凝胶上磷蛋白的特异性荧光染色检测范围为 1〜16n g 磷蛋白每条带。对于单体磷蛋白而言,信号强度与磷酸基团的数量有关,并与超过三个数量级呈线性关系。 材 料包含目的蛋白的样品 甲醇,质谱级 三氯甲焼,质谱级 I X S D S 样品缓冲液 磷 蛋 白 标 准 品(PeppermintStick 磷蛋白分子质量标准品, Molecular Probes; 也可见表 12. 4.1) 磷蛋白凝胶用固定液 Pro-Q Diamond 麟蛋白凝胶染色液(Molecular Probes) V 磷蛋白凝 胶 脱 色 液(也可购于 Molecular Probes 公司) 聚 苯 乙 烯 染 色 皿(如称重皿) 旋转摇床 2 . 再次离心,弃去浮在表面的物质。用 Speedvac 蒸汽机干燥沉淀物,用 标 准 I X 电泳样品缓冲液重悬沉淀。 3 . 将样品与磷蛋白标准品、磷酸化和非磷酸化对照一起电泳(单 元 12. 3),为了检测到少量磷蛋白,使用和典型考马斯亮蓝染色相近的蛋白质量(见基本方案 1)。 5 a . 将 凝 胶 在 IOOrnl 左右水中温和振荡 10 min,重复清洗一次。 6a.将凝胶置入 50 ml Pro-Q Diamond 磷蛋白凝胶染色液中避光孵育 75〜120 min。 7 a . 在室温下将凝胶置于 80m l 磷蛋白凝胶脱色液中避光孵育 3 h 左右 ,其中更换两次脱色 液(如 赙 育 3 次 ,每 次 60 min)。用适当的仪器将凝胶成像并存档。 |
|---|