全小分子化合物组合,为角膜盲治疗提供新思路
人体由百万亿级数量的细胞组成。每个人都是从一个受精卵发育为数百种成熟的终末细胞,形成我们保持生命健康的基本单元。这些不同种类的成熟终末细胞,既往传统的观点认为无法相互转化“变身”。近日,来自我国眼科学界的最新研究发现,皮肤细胞竟然可以化身为神经嵴,进而变成角膜内皮细胞!更为重要的是,只是简单地通过几个小分子化合物组合即可高效助力完成“变身戏法”。

角膜疾病是目前人类失明的重要原因之一,全球约有超过1000万病人遭受因角膜疾病引起的失明,即角膜盲。其中,角膜内皮细胞(corneal endothelial cell,CEC)作为单层功能细胞,其特有的离子泵功能是维持角膜透明度的关键。然而,CEC在体内不可再生,年龄的增长或外伤、手术、炎症等多种因素均可造成内皮细胞的损伤或丢失,引起内皮功能失代偿,出现角膜水肿、混浊失去透明性,最终导致患者失明。角膜移植术是让角膜盲患者复明的唯一手术方式,目前主要以健康捐赠的角膜组织代替受损角膜为主要治疗手段。然而,由于供体角膜极度短缺,不到1.3%需要角膜移植的患者能够接受移植,严重限制了手术开展和患者复明。
随着组织工程和细胞工程技术的不断发展,人多能干细胞来源的CEC成为移植种子细胞的理想来源,但目前存在诱导时间长、效率低、体外扩增能力弱以及潜在致瘤风险等问题,在实际应用过程中会受到诸多限制。近年来,用小分子化合物将体细胞重新编程成所需的功能细胞类型的转分化策略,由于其安全和高效率等优点引起了人们的广泛关注,在细胞替代治疗中展示出重要的临床应用前景。目前,国内外尚无完全小分子化合物转分化CEC的技术报道。
2021年6月4日,首都医科大学附属北京同仁医院、北京市眼科研究所所长金子兵研究团队,在Science Advances在线发表研究论文Conversion of mouse embryonic fibroblasts into neural crest cells and functional corneal endothelia by defined small molecules,在国际上首次报道利用全小分子化合物组合,将成纤维细胞转分化为神经嵴和功能性角膜内皮细胞,为角膜内皮的临床细胞治疗提供了全新的科学思路。

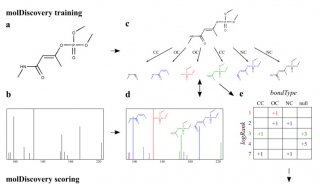
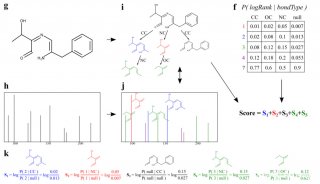
在该研究中,CEC的诱导策略主要由两个步骤组成,首先是将小鼠成纤维细胞诱导为中间态的神经嵴细胞(neural crest cell,NCC),同时借助特异性荧光报告体系筛选出高效的小分子化合物诱导组合,该步骤获得的NCC不论在形态、基因表达和分化能力上都具备典型的NCC特征,并且可以通过小分子化合物的诱导进一步分化为CEC,研究人员将得到的该类细胞定义为化合物诱导性CEC(chemically induced CEC,ciCEC)。研究结果显示,诱导产生的ciCEC呈现典型的单层、鹅卵石样形态,并与原代细胞表现出一致的基因表达特征和自我更新能力。同时,这些ciCEC可以在特定的小分子化合物培养基中长期传代培养,并仍然保留CEC特征,提示ciCEC具有强大的体外扩增能力。
随后,研究人员通过在体移植实验进一步验证ciCEC的功能,将ciCEC移植到角膜内皮缺失的新西兰兔眼中后,能够显著逆转角膜的透明度。进一步的检查发现,实验组兔子眼角膜的水肿情况得到明显改善,并且移植的ciCEC细胞在宿主体内能够稳定地整合。这些结果都证明小分子化合物诱导的CEC细胞具备发挥正常功能的潜力。
该方法是国内外首次报道的全小分子化合物诱导神经嵴和角膜内皮的技术体系,对于神经嵴下游所有组织细胞的再生具有重要价值。角膜病专家、首都医科大学附属北京同仁医院主任医师接英表示,这项技术对于未来建立可用于临床治疗角膜内皮盲病人带来全新的希望,为获得充足的可用于移植的角膜内皮提供了新技术,具有重要的开创性意义。